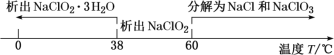-
ICl的冰醋酸溶液可用于测定油脂的不饱和溶液,其原理为 +ICl
+ICl
 。ICl制备装置图如下,(夹持装置及加热仪器已省略);
。ICl制备装置图如下,(夹持装置及加热仪器已省略);
已知:ICl的熔点为27℃,沸点为97.4℃,易水解,且能发生反应ICl(1)+Cl2(g)=ICl3(1)。
(1)盛装浓盐酸的仪器名称是________;装置C中的试剂名称是________。
(2)装置B的作用是_________;不能用装置F代替装置E,理由是________。
(3)用ICl的冰醋酸溶液测定某油脂(M=880)的不饱和度。进行如下两个实验。
实验1:将4.40g该油渍样品溶于四氯化碳后形成l00mL溶液,从中取出十分之一,加入20mL某浓度的ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用1.00mol/L的Na2S2O3标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其他操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
① 滴定过程中可用_________作指示剂。
② 滴定过程中需要不断振荡,否则会导致V1_______(填“偏大”或“偏小”)。
③ 若V1=15.00mL,V2=20.00mL,则该油脂的不饱和度为___________。
-
水合肼 是无色、有强还原性的液体,实验室制备水合肼的原理为
是无色、有强还原性的液体,实验室制备水合肼的原理为 据此,某学生设计了下列实验.
据此,某学生设计了下列实验.
(制备NaClO溶液)实验装置如图甲所示 部分夹持装置已省略
部分夹持装置已省略
已知:3NaClO


(1)配制 溶液时,所需玻璃仪器除量筒外还有______
溶液时,所需玻璃仪器除量筒外还有______ 填字母
填字母 。
。
A.容量瓶  烧杯
烧杯  移液管
移液管  玻璃棒
玻璃棒
(2)装置Ⅰ中发生的离子反应方程式是______;Ⅱ中玻璃管a的作用为______;为了提高NaClO的产率,需对Ⅰ中产生的 进行净化,所用试剂是______;Ⅱ中用冰水浴控制温度在
进行净化,所用试剂是______;Ⅱ中用冰水浴控制温度在 以下,其主要目的______。
以下,其主要目的______。
(制取水合肼)实验装置如图乙所示
(3)仪器A的名称为______;反应过程中,如果分液漏斗中溶液的滴速过快,部分 参与A中反应并产生大量氮气,产品产率因此降低,请写出降低产率的相关化学反应方程式______;充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品。
参与A中反应并产生大量氮气,产品产率因此降低,请写出降低产率的相关化学反应方程式______;充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品。
(测定肼的含量)
(4)称取馏分 ,加水配成
,加水配成 溶液,在一定条件下,用
溶液,在一定条件下,用 的
的 溶液滴定.已知:
溶液滴定.已知:
 滴定时,可以选用的指示剂为______;
滴定时,可以选用的指示剂为______;
 实验测得消耗
实验测得消耗 溶液的平均值为
溶液的平均值为 ,馏分中
,馏分中 的质量分数为______。
的质量分数为______。
-
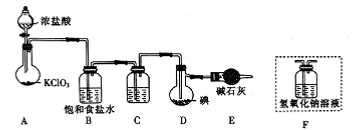
高碘酸钾(KIO4)溶于热水,微溶于冷水和氢氧化钾溶液,可用作有机物的氧化剂。制备高碘酸钾的装置图如下(夹持和加热装置省略)。回答下列问题:

(1)装置I中仪器甲的名称是___________。
(2)装置I中浓盐酸与KMnO4混合后发生反应的离子方程式是___________。
(3)装置Ⅱ中的试剂X是___________。
(4)装置Ⅲ中搅拌的目的是___________。
(5)上述炭置按气流由左至右各接口顺序为___________(用字母表示)。
(6)装置连接好后,将装置Ⅲ水浴加热,通入氯气一段时间,冷却析岀高碘酸钾晶体,经过滤,洗涤,干燥等步骤得到产品。
①写出装置Ⅲ中发生反应的化学方程式:___________。
②洗涤时,与选用热水相比,选用冷水洗涤晶体的优点是___________。
③上述制备的产品中含少量的KIO3,其他杂质忽略,现称取ag该产品配制成溶液,然后加入稍过量的用醋酸酸化的KI溶液,充分反应后,加入几滴淀粉溶液,然后用1.0mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液的平均体积为bL。
已知:KIO3+5KI+6CH3COOH===3I2+6CH3COOK+3H2O
KIO4+7KI+8CH3 COOH===4I2+8CH3COOK+4H2O
I2+2Na2S2O3===2NaI+N2S4O6
则该产品中KIO4的百分含量是___________(Mr(KIO3)=214,Mr(KIO4)=230,列出计算式)。
-
高碘酸钾(KIO4)溶于热水,微溶于冷水和氢氧化钾溶液,可用作有机物的氧化剂。制备高碘酸钾的装置图如下(夹持和加热装置省略)。回答下列问题:
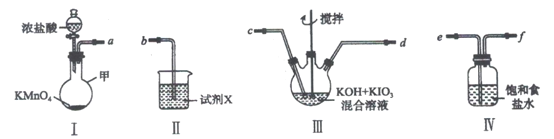
(1)装置I中仪器甲的名称是___________。
(2)装置I中浓盐酸与KMnO4混合后发生反应的离子方程式是___________。
(3)装置Ⅱ中的试剂X是___________。
(4)装置Ⅲ中搅拌的目的是___________。
(5)上述炭置按气流由左至右各接口顺序为___________(用字母表示)。
(6)装置连接好后,将装置Ⅲ水浴加热,通入氯气一段时间,冷却析岀高碘酸钾晶体,经过滤,洗涤,干燥等步骤得到产品。
①写出装置Ⅲ中发生反应的化学方程式:___________。
②洗涤时,与选用热水相比,选用冷水洗涤晶体的优点是___________。
③上述制备的产品中含少量的KIO3,其他杂质忽略,现称取ag该产品配制成溶液,然后加入稍过量的用醋酸酸化的KI溶液,充分反应后,加入几滴淀粉溶液,然后用1.0mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液的平均体积为bL。
已知:KIO3+5KI+6CH3COOH===3I2+6CH3COOK+3H2O
KIO4+7KI+8CH3 COOH===4I2+8CH3COOK+4H2O
I2+2Na2S2O3===2NaI+N2S4O6
则该产品中KIO4的百分含量是___________(Mr(KIO3)=214,Mr(KIO4)=230,列出计算式)。
-
ClO2又称百毒净,可用于水的净化和纸浆、纺织品的漂白。用如下图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质。
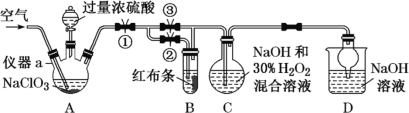
已知:①高氯酸:沸点90 ℃,浓度低于60%比较稳定,浓度高于60%遇含碳化合物易爆炸。
②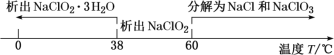
回答下列问题:
(1)仪器a的名称为_______。实验开始前,胶塞及导管接口必须包锡箔纸,其原因是__________。
(2)写出装置A制备ClO2同时生成高氯酸的化学方程式:___________。
(3)关闭止水夹②,打开止水夹①③,通空气一段时间,装置C中生成NaClO2,离子方程式为______。若关闭止水夹③,打开止水夹②,B中可观察到的现象为_______。
(4)从装置C反应后的溶液中获得NaClO2晶体,常采用减压蒸发结晶。采用减压蒸发的原因是______,减压蒸发时,当有较多晶体析出时,再_____(填操作方法),洗涤,干燥。即可得NaClO2。
(5)城市饮用水处理新技术用NaClO2、高铁酸钠替代Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,NaClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是________。
(6)ClO2很不稳定,需随用随制,产物用水吸收可得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样量取V0mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用cmol·L−1Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V1mL。
已知:2ClO2+10I−+8H+=2Cl−+5I2+4H2O,2Na2S2O3+I2=Na2S4O6+2NaI,计算该ClO2的浓度为________g/L(用含字母的代数式表示,计算结果化简)。
-
氯化亚铜(CuCl)在生产中广泛用作催化剂、杀菌剂、脱色剂。某兴趣小组采用加热分解氯化铜晶体(CuCl2·xH2O)的方法制备CuCl,其装置如下(夹持仪器省略)。

已知:
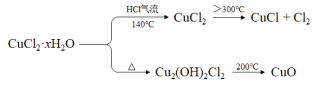
完成下列填空:
(1)在实验过程中,可以观察到C中试纸的颜色变化是___________________________。
(2)实验过程中需要全程通入干燥的HCl,其作用是___________________________。
(3)反应结束后,取出CuCl产品进行实验,发现其中含有少量的杂质,根据已知信息
① 若杂质是CuCl2,则产生的原因可能是____________________________________。
② 若杂质是CuO,则产生的原因可能是_____________________________________。
(4)为测定原料CuCl2·xH2O中结晶水的数目x,可采取如下方案:
a.用电子天平称取一定质量氯化铜晶体 b.在______(填仪器名称)中充分灼烧
c.在干燥器中冷却 d.称量所得黑色固体质量
e.重复b ~ d操作直至_____________________
① 完成上述实验操作步骤。
② 若氯化铜晶体质量为3.384 g,最终得到黑色固体质量为1.600 g,则x =________(精确到0.1)。
③ 若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。____________________________
-
氯化亚铜(CuCl)在生产中广泛用作催化剂、杀菌剂、脱色剂。某兴趣小组采用加热分解氯化铜晶体(CuCl2·xH2O)的方法制备CuCl,其装置如下(夹持仪器省略)。

已知:
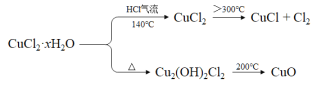
完成下列填空:
(1)在实验过程中,可以观察到C中试纸的颜色变化是___________________________。
(2)实验过程中需要全程通入干燥的HCl,其作用是___________________________。
(3)反应结束后,取出CuCl产品进行实验,发现其中含有少量的杂质,根据已知信息
① 若杂质是CuCl2,则产生的原因可能是____________________________________。
② 若杂质是CuO,则产生的原因可能是_____________________________________。
(4)为测定原料CuCl2·xH2O中结晶水的数目x,可采取如下方案:
a.用电子天平称取一定质量氯化铜晶体 b.在______(填仪器名称)中充分灼烧
c.在干燥器中冷却 d.称量所得黑色固体质量
e.重复b ~ d操作直至_____________________
① 完成上述实验操作步骤。
② 若氯化铜晶体质量为3.384 g,最终得到黑色固体质量为1.600 g,则x =________(精确到0.1)。
③ 若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。____________________________
-
由SO2和O2制备SO3(熔点16.8℃,沸点44.8℃)的模拟装置如下图所示)(加热和夹持装置省略):
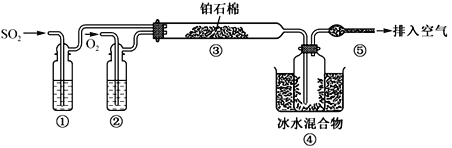
下列说法正确的是
A. 装置①中的试剂为饱和NaHSO3溶液
B. 实验室可用铜与稀硫酸在加热条件下制取SO2
C. 裝置③反应管中的铂石棉用作反应的催化剂
D. 从装置⑤逸出的气体有过量的SO2和O2
-
由SO2和O2制备SO3(熔点16.8℃,沸点44.8℃)的模拟装置如下图所示)(加热和夹持装置省略):

下列说法正确的是
A. 装置①中的试剂为饱和NaHSO3溶液
B. 实验室可用铜与稀硫酸在加热条件下制取SO2
C. 裝置③反应管中的铂石棉用作反应的催化剂
D. 从装置⑤逸出的气体有过量的SO2和O2
-
三氯化碘(ICl3)在药物合成中用途非常广泛。已知ICl3能使湿润的淀粉KI试纸变蓝。实验室可用如图装置制取ICl3(夹持装置省略)。

(1)制备氯气选用的药品为漂白精固体[主要成分为Ca(ClO)2]和浓盐酸,相关反应的化学方程式为_________。
(2)试剂X、Y分别是_______、_______。
(3)装置B的作用是:_______;装置E的作用是:_______。
(4)氯气与单质碘需在温度稍低于70℃下反应,则装置D适宜的加热方式为______。
(5)某同学欲测定ICl3 样品中ICl3的纯度,他准确称取ICl3样品10.00g于烧杯中,加入适量水和过量KI晶体,充分反应(样品中杂质不反应),反应的化学方程式为__________,将所得溶液配制成100mL待测液,取25.00mL待测液,用2.000mol·L-1的Na2S203标准液滴定(I2 +2S2O32-=2I-+S4O62-),以淀粉溶液作指示剂,达到终点时的现象为_______,重复滴定3次,测得消耗Na2S203溶液体积的平均值为20.00mL。该样品中ICl3的质量分数为_______。
+ICl
。ICl制备装置图如下,(夹持装置及加热仪器已省略);