-
钛镍形状记忆合金(TiNi)被广泛用于人选卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题
(l)写出基态Ni原子的电子排布式:_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为______,中心原子的轨道杂化类型是__________。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是_______。②原子半径r(Cl)_____ (填“>”、“<”或“=”,下同)r(Mg),离子半径r(O2-)______r(Mg2+)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为_________。
(5)一种钛镍合金的立方晶胞结构如右图所示。该合金中Ti的配位数为_______。
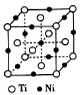
-
钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是______。
②原子半径r(Cl)_____r(Mg),离子半径r(O2-)______r(Mg2+)(填“>”、“<”或“=”)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为__________,提供孤对电子的成键原子是_________。(填元素符号)
(5)一种钛镍合金的立方晶胞结构如图所示:
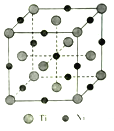
①该合金中Ti的配位数为________。
②若合金的密度为d g/cm3,晶胞边长a=________pm。(用含d的计算式表示)
-
钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是______。
②原子半径r(Cl)_____r(Mg),离子半径r(O2-)______r(Mg2+)(填“>”、“<”或“=”)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为__________,提供孤对电子的成键原子是_________。(填元素符号)
(5)一种钛镍合金的立方晶胞结构如图所示:
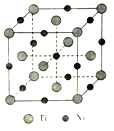
①该合金中Ti的配位数为________。
②若合金的密度为d g/cm3,晶胞边长a=________pm。(用含d的计算式表示)
-
钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是______。
②原子半径r(Cl)_____r(Mg),离子半径r(O2-)______r(Mg2+)(填“>”、“<”或“=”)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为__________,提供孤对电子的成键原子是_________。(填元素符号)
(5)一种钛镍合金的立方晶胞结构如图所示:
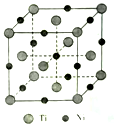
①该合金中Ti的配位数为________。
②若合金的密度为d g/cm3,晶胞边长a=________pm。(用含d的计算式表示)
-
金属钛及其化合物被广泛应用于飞机、火箭、导弹、人造卫星、宇宙飞船、舰艇、军工、医疗以及石油化工等领域,人们称钛为“21世纪金属”。自然界中钛的一种存在形式为金红石(主要成分是TiO2)。回答下列问题:
(1)基态钛原子的价电子排布式为__________________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的元素分别是_________________(填元素符号)。
(2)钛的硬度大于铝,其原因是_________________________。
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①TiCl4熔点为-24℃,沸点为136.4℃,室温下为无色液体,可溶于甲苯和氯代烃,固态TiCl4属于___________晶体。
②LiBH4由Li+和BH4-构成,BH4-的空间构型是______,B原子的杂化轨道类型是___________。
(4)用锌还原TiCl4的盐酸溶液,经后续处理可制得绿色的晶体[TiCl(H2O)5]Cl2·H2O。该晶体所含元素中,电负性最大的元素是___________,与Ti形成配位键的配体是___________,1mol该配合物中含有σ键的数目为___________。
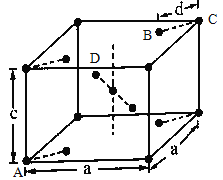
(5)TiO2晶胞是典型的四方系结构,其晶胞结构如图所示(晶胞中相同位置的原子相同),其中A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,_____,______),钛氧键的键长d=___________(用代数式表示)。
-
下列说法不正确的是
A. 液氯可以储存在钢瓶中
B. 碳酸钠在医疗上是治疗胃酸过多的一种药剂
C. 硅晶体是半导体材料,广泛应用于电子工业的各个领域
D. 钠和钾的合金在常温下是液体,可用于快中子反应堆作热交换剂
-
Ga、As、Al、C的相关化合物在化工和医学领域有着广泛的应用。回答下列问题:
(1)写出基态Ga原子的核外电子排布式:_________,有_____个未成对电子。
(2)合金砷化镓在现代工业中被广泛应用,Ga、As电负性由大到小排序为______________。
(3)1个丙二烯分子中σ键总数为___个,C原子的杂化方式为______。分子中的大π键可以用符号пmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为п66),则丙二烯中的大π键应表示为____________。
(4)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:
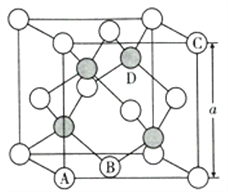
①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0, 0, 0);B为(1/2,1/2,0);C为(1,0,1)。则D原子的坐标参数为_________________。
②已知氮化镓晶胞的边长为a nm,其密度为d g/cm3,则阿伏加德罗常数NA =____(用a、d表示)
-
下列说法中正确的是( )
A.合金的熔点一般比组成合金的各成分金属高
B.玻璃、陶瓷、水泥都是常见的硅酸盐材料
C.玻璃钢是由玻璃纤维和钢组成的复合材料
D.光导纤维的主要成分是硅,可广泛用于通信和医疗领域
-
下列说法中正确的是
A.合金的熔点一般比组成合金的各成分金属高
B.玻璃、陶瓷、水泥都是常见的硅酸盐材料
C.玻璃钢是由玻璃纤维和钢组成的复合材料
D.光导纤维的主要成分是硅,可广泛用于通信和医疗领域
-
磷酸二氢钾在工农业和医学领域具有广泛的应用。以下是工业上制备磷酸二氢钾的两种方法。回答下列问题:
I.直接法
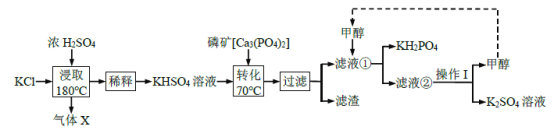
(1)气体X 为_______(填化学式)。
(2)写出“转化”步骤发生反应的离子方程式_________。
(3)滤液①中加入甲醇的作用是_____________。
(4)操作I 为__________。
II.电解法
电解法制取KH2PO4 的原理如图所示,一定条件下,还可得到NaClO3

(5)在_____室(填标号)可得到KH2PO4;写出产生ClO3-的电极反应式_____________。
III.纯度分析
测定产品纯度的反应原理为KH2PO4+NaOH=KNaHPO4+H2O
(6)取产品3.00 g,加入15 mL 蒸馏水溶解,加入指示剂,用0.5000 mol·L-1 NaOH 标准溶液滴定至终点,消耗40.00 mL,该产品的纯度为________(结果保留三位有效数字)。







