-
氮及其化合物在生产、生活中有着重要作用。
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德•埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如下(

 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):
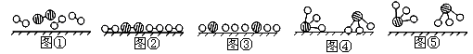
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示 。
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。酸性KMnO4溶液与NaNO2反应的离子方程式是:MnO4-+NO2-+X Mn2++NO3-+H2O(未配平),X表示的粒子是 。酸性高锰酸钾 (“能”或“不能”)鉴别食盐中是否存在NaNO2,理由是___________________
Mn2++NO3-+H2O(未配平),X表示的粒子是 。酸性高锰酸钾 (“能”或“不能”)鉴别食盐中是否存在NaNO2,理由是___________________
-
氮及其化合物在生产、生活中有着重要作用。
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德•埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如下(

 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):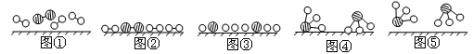
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示_________________。
(2)NaNO2是一种食品添加剂(有毒性,市场上常误与食盐混淆)。酸性KMnO4溶液与NaNO2反应的离子方程式是:MnO4-+NO2-+X Mn2++NO3-+H2O (未配平)。下列有关叙述正确的是____________。
Mn2++NO3-+H2O (未配平)。下列有关叙述正确的是____________。
a.NaNO2属于硝酸盐 b.生成1 mol NaNO3需消耗0.4 mol KMnO4
c.反应过程中溶液的pH减小 d.X表示的粒子是OH-
(3)工业生产以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3(g)+CO2(g)  CO(NH2)2(l)+H2O(l)。
CO(NH2)2(l)+H2O(l)。
①已知该反应平衡常数K195℃<K165℃,则该反应的△H____________0(填“>”“=”或“<”)。
②T1℃时,在2 L的密闭容器中充入NH3和CO2模拟工业生产,若原料气中的NH3和CO2的物质的量之比(氨碳比) = x,如图是CO2平衡转化率(α) 与氨碳比(x)的关系。
= x,如图是CO2平衡转化率(α) 与氨碳比(x)的关系。

其它条件不变时,α随着x增大而增大的原因是________________________;图中的B点处NH3的平衡转化率为________________。
③当x=2,上述反应至5 min时各物质的浓度不再发生变化,测得体系压强变为开始时的 。反应结束后,分离得到90 g尿素。
。反应结束后,分离得到90 g尿素。
计算0~5 min内该反应的平均速率υ(CO2)= ______________,该反应的平衡常数K=___________,达到平衡后NH3的物质的量浓度为____________。
-
如图1所示是工业生产硝酸的流程:

合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金网.请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨.2007年化学家格哈德•埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如图2所示. 、
、 、
、 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______.
(2)合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g),写出该反应的化学平衡常数表达式K=______.在一定温度和压强下,将H2 和N2 按3:1(体积之比)混合后进入合成塔,反应达到平衡时,平衡混合气中NH3 的体积分数为15%,此时H2 的转化率为______.
(3)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1 266.8kJ/mol
N2(g)+O2(g)=2NO(g)△H=+1 80.5kJ/mol,氨催化氧化的热化学方程式为______.
(4)吸收塔中通入空气的目的是______.
-
(12分) 1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体表面合成氨的反应过程,示意如下图:
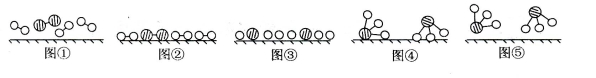
(1)图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______,__ ____。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g); ΔH= - 1266.8 kJ/mol
N2(g) + O2(g) = 2NO(g) ; ΔH = + 180.5kJ/mol, 氨催化氧化的热化学方程式为___ _______。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
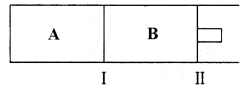
①当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为_____ _______;保持温度和压强不变,向此容器中通入0.36molN2,平衡将____ ______(填“正向”、“逆向”或“不”)移动。
②向A、B两容器中均通入xmolN2和ymolH2,初始A、B容积相同,并保持温度不变。若要平衡时保持N2在A、B两容器中的体积分数相同,则x与y之间必须满足的关系式为__ __。
-
(共6分)瑞典皇家科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德·埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为_________。
(2)当催化剂中Fe2+与Fe3+物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为_________(用小数表示)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:
2Fe2O3 +C=4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。
-
2007年诺贝尔化学奖授予德国科学家格哈德•埃特尔,以表彰他在表面化学研究领域作出的开拓性贡献.物质接触表面发生的化学反应对工业生产运作至关重要.同时,表面化学研究有助于我们理解各种不同的过程.以下事实或现象与表面化学无密切关系的是( )

A.熔化的铝不易滴落下来
B.利用铁的表面作为催化剂用氮气和氢气合成氨
C.常温下,可以用铁、铝制做的容器来盛装冷的浓硫酸
D.CuSO4溶液中加入BaCl2溶液时产生白色沉淀
-
2007年诺贝尔化学奖授予德国化学家格哈德·埃特尔,以表彰其在固体表面化学研究领域作出的开拓性贡献。下图是氢气与氮气在固体催化剂表面合成氨的反应过程示意图,下列有关合成氨反应的叙述中不正确的是( )

A.过程②需吸收能量,过程③则放出能量
B.常温下该反应难以进行,是因为常温下反应物的化学键难以断裂
C.在催化剂的作用下,该反应的△H变小而使反应变得更容易发生
D.该过程表明,在化学反应中存在化学键的断裂与形成
-
2007年诺贝尔化学奖获得者格格德•埃特尔在表面化学研究领域作出了开拓性贡献.研究气体在固体表面反应的化学已经成为化学科学的一个重要分支,它涉及生产生活中的许多重要领域.下列不属于气体与固体作用的表面化学研究领域的是( )
A.合成氨工业是将氮气和氢气在铁催化剂的表面转化成氨气
B.汽车中装有的催化器,能将尾气中一氧化碳和氮氧化物转化为二氧化碳和氮气
C.在燃料电池中,氢气和氧化剂在催化剂表面反应所产生的能量转化为电能
D.加酶洗衣粉的乳化作用能将衣物纤维表面的油渍洗去
-
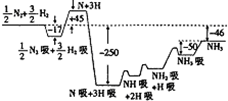
2007年度诺贝尔化学奖获得者格哈德•埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ•mol-1.(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题:
(1)合成氨反应的机理为
①______;
②N:N2吸 2N
2N 2N吸
2N吸
③______;
④NH吸+H吸 NH2吸;
NH2吸;
⑤NH2吸+H吸 NH3吸
NH3吸 NH3.
NH3.
(2)T=673K时,合成氨反应的热化学方程为______.
(3)液氨与水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为:
2NH3 NH4++NH2-(某温度下其离子积常数为10-30).液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=______.
NH4++NH2-(某温度下其离子积常数为10-30).液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=______.
(4)盐酸肼(N2H4Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似.写出盐酸肼第一步水解反应的离子方程式______.
-
2007年诺贝尔化学奖得主——德国科学家格哈德·埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究,催生了汽车尾气净化装置。净化装置中的催化转化器,可将CO、NO、NO2和碳氢化合物等转化无害的物质,有效降低尾气对环境的危害。下列有关说法不正确的是

A.催化转化器中的铂催化剂可加快CO氧化
B.铂表面做成蜂窝状更有利于提高催化效果。
C.在铂催化下,NO、NO2可被CO还原成N2
D.碳氢化合物在铂催化下,被CO直接氧化成CO2和H2O
分别表示N2、H2、NH3):

Mn2++NO3-+H2O (未配平)。下列有关叙述正确的是____________。
CO(NH2)2(l)+H2O(l)。
= x,如图是CO2平衡转化率(α) 与氨碳比(x)的关系。

。反应结束后,分离得到90 g尿素。







