-
下列关于金属单质及其化合物的叙述正确的是
①赤铁矿的主要成分是Fe3O4
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
⑤ Fe3+与KSCN产生血红色沉淀
⑥Na2O2既可作呼吸面具中,又可漂白织物、麦杆、羽毛等
⑦铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
⑧明矾常作为消毒剂
⑨氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得到相同的物质
A.④⑥⑧ B.①③④⑥⑦
C.②④⑥⑦⑨ D.①②③⑤⑧
高三化学选择题中等难度题查看答案及解析
-
钛是继铁、铝后的第三金属,二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.用钛铁矿制取二氧化钛,(钛铁矿主要成分为FeTiO3,其中Ti元素化合价为+4价,含有Fe2O3杂质。)主要流程如下:
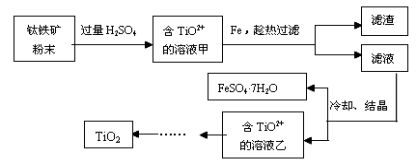
(1)Fe2O3与H2SO4反应的离子方程式_________________。
(2)加Fe的作用是______________________。
Ⅱ.由金红石(含TiO2大于96%)为原料生产钛的流程如下:
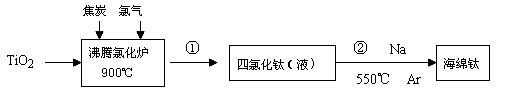
(3)反应②的方程式是 ,该反应需要在Ar气氛中进行的原因是 。
Ⅲ.科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺。
(4)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氧化钙,原理如右图所示 该方法阴极获得钛的电极反应为 。
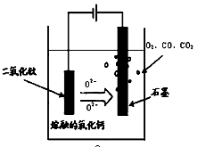
(5)阳极产生的CO2经常用氢氧化钠溶液来吸收,现有0.4mol CO2用200ml 3mol/L的NaOH溶液将其完全吸收,溶液中的离子浓度由大到小的顺序为 。
高三化学填空题极难题查看答案及解析
-
下列关于铁的叙述正确的是
①铁能被磁铁吸引,但纯铁易腐蚀 ②在人体的血红蛋白中含有铁元素 ③铁位于元素周期表中第4周期第ⅧB族 ④铁能在纯氧气中剧烈燃烧,但不能在空气中燃烧 ⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3 ⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.②⑤ B.①③ C.②④ D.④⑥
高三化学选择题中等难度题查看答案及解析
-
下列关于铁的叙述正确的是( )
①铁能被磁铁吸引,但纯铁易被腐蚀 ②在人体内的血红蛋白中含有铁元素 ③铁位于元素周期表中第四周期第ⅧB族 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3 ⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②④ C.②⑤ D.④⑥
高三化学选择题中等难度题查看答案及解析
-
下列关于铁的叙述正确的是
①铁能被磁铁吸引,但纯铁易被腐蚀
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④工业上可用铁制容器储存、运输浓硝酸和浓硫酸
⑤向KI-淀粉溶液中加入FeCl3溶液,溶液变蓝,是因为Fe3+能与淀粉发生显色反应
⑥不能通过化合反应制得FeCl2和Fe(OH)3
A. ①③ B. ②④ C. ②⑤ D. ④⑥
高三化学单选题简单题查看答案及解析
-
下列关于铁的叙述正确的是( )
①铁能被磁铁吸引,但纯铁易被腐蚀 ②在人体内的血红蛋白中含有铁元素 ③铁位于元素周期表中第四周期第ⅧB族 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3 ⑥不能通过化合反应制得FeCl2和Fe(OH)3
A. ①③ B. ②④ C. ②⑤ D. ④⑥
高三化学单选题中等难度题查看答案及解析
-
下列关于铁的叙述正确的是 ( )。
①铁能被磁铁吸引,但纯铁易被腐蚀
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3
⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②④ C.②⑤ D.④⑥
高三化学选择题中等难度题查看答案及解析
-
铬是一种重要的金属元素,具有多种价态,单质铬是硬度最大的金属,熔点为
。回答下列问题:
工业上以铬铁矿
主要成分是
为原料冶炼铬的流程如图所示:

中铬元素的化合价为_________。
高温氧化时发生反应的化学方程式为________________。
操作a由两种均发生了化学反应的过程构成,其分别是_________、铝热反应。
是两性氢氧化物,请写出其电离方程式_________________。
铬元素能形成含氧酸及含氧酸盐,若测得浓度为
的铬酸
溶液中含铬元素的微粒浓度分别为
、
、
,试推测
溶液呈________
填“酸”“碱”或“中”
性,原因是______________。
水中的铬元素对水质及环境均有严重的损害作用,工业上用下述方法来进行无害化处理并获得有价值的产品。
电解处理含有
的污水:用铁作电极电解污水,
被阳极区生成的离子还原成
,生成的
与阴极区生成的
结合生成
沉淀而除去。则阴极上的电极反应式为_______,若要处理
浓度为
的污水,理论上需要消耗_______kg的铁。
转化为有价值的产品磁性铁铬氧体
:先向含
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气
氧化部分
并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。写出
在酸性条件下被
还原为
的离子方程式__________,若处理含
不考虑其他含铬微粒
的污水时恰好消耗
,则当铁铬氧体中
时,铁铬氧体的化学式为_______________。
高三化学工业流程困难题查看答案及解析
-
铁是自然界分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是Fe2O3)等。
(1)写出赤铁矿炼铁的主要化学方程式________;
(2)红热的铁能跟水蒸气反应,有一种产物是可燃性气体,则其反应式为
________;
在常温下,铁跟水不起反应。但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。刷油漆是重要的防腐蚀措施之一,油漆防腐蚀的主要原理是________。
(3)铁元素是人体的重要营养元素,举一例说明铁元素在人体中的重要作用。
________。
高三化学填空题中等难度题查看答案及解析
-
铁是世界上用量最大的金属,铁及其化合物在生活、生产中有广泛应用。
请回答下列问题:
⑴ Fe3O4是磁铁矿的主要成分,Fe3O4可用于制造录音磁带和电讯器材等。高温下,铝粉能与Fe3O4发生铝热反应,该反应的化学方程式为 。34.8g Fe3O4与足量稀硝酸反应,被还原HNO3的物质的量为 mol。
⑵ FeCl3溶液是一种黄色透明液体,可用作止血剂,其原因是
;向煮沸的蒸馏水中加入几滴饱和FeCl3溶液,继续煮沸得到红褐色的Fe(OH)3胶体,鉴别FeCl3溶液与Fe(OH)3胶体的方法是 。
⑶ 高铁酸钠(Na2FeO4)是一种绿色水处理剂,具有杀菌消毒和聚沉水中杂质的作用,它的杀菌消毒原理是 。高铁电池是一种新型可充电电池,高铁电池的总反应为3Zn+2Na2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4NaOH。该电池充电时阳极的电极反应式为 。
⑷ 铁红是一种重要的红色颜料,其主要成分是Fe2O3,将一定量的铁红溶于130mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L气体(标准状况),向反应后溶液中加入几滴KSCN溶液,溶液不变红色,则参加反应的铁粉质量为 。
高三化学填空题简单题查看答案及解析