-
六氟化硫分子呈正八面体,难以水解,在高电压下仍有良好的绝缘性,在电器工业有着广泛用途,但逸散到空气中会引起强温室效应.下列有关SF6的推测正确的是( )
A.SF6易燃烧生成二氧化硫
B.SF6中各原子均达到 8 电子稳定结构
C.高温条件下,SF6微弱水解生成H2SO4和HF
D.SF6是极性分子高三化学选择题中等难度题查看答案及解析
-
六氟化硫分子呈正八面体,难以水解,在高电压下仍有良好的绝缘性,在电器工业有着广泛用途,但逸散到空气中会引起强温室效应。下列有关SF6的推测正确的是( )
A.SF6易燃烧生成SO2
B.SF6是极性分子
C.SF6中各原子均达到八电子稳定结构
D.高温条件下,SF6微弱水解生成H2SO4和HF
高三化学选择题简单题查看答案及解析
-
六氟化硫分子呈正八面体,常温下难以水解,在高电压下仍有良好的绝缘性,在电器工业有着广泛用途,但逸散到空气中会引起强温室效应。下列有关SF6的推测正确的是
A.SF6易燃烧生成二氧化硫
B.SF6中各原子均达到8电子稳定结构
C.高温条件下,SF6微弱水解生成H2SO4和HF
D.SF6是极性分子
高三化学选择题中等难度题查看答案及解析
-
六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是
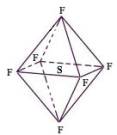
A.SF6中各原子均达到8电子稳定结构
B.SF6易燃烧生成SO2
C. SF6分子是含有极性键的非极性分子
D.SF6是原子晶体
高三化学选择题中等难度题查看答案及解析
-
(14分)空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)一定条件下CO2可制得Na2CO3、NaHCO3等。
①等物质的量浓度的Na2CO3、NaHCO3溶液,碱性前者 后者(填“>”“<”或“=”)。
②有下列五种物质的量浓度均为0.1mol/L的电解质溶液,将其稀释相同倍数时,其中pH变化最大的是 (填字母编号)。
A.Na2CO3
B.NaHCO3
C.NaAlO2
D.CH3COONa
E.NaOH
(2)已知反应Fe(s)+CO2(g)
FeO(s)+CO(g) ΔH=a kJ/mol,测得在不同温度下,
该反应的平衡常数K随温度的变化如下:
温度(℃)
300
500
700
K
3.00
3.47
4.40
上述反应中a_______0(填“>”、“<”或“=”);在2L密闭容器中300℃下进行反应,若Fe和CO2的起始量均为4 mol,当达到平衡时CO2的转化率为________。
(3)目前工业上可以用CO2和H2在230℃、催化剂条件下反应生成甲醇蒸汽和水蒸气。下图为恒压容器中0.5 mol CO2和1.5 mol H2反应转化率达80%时的能量变化示意图。则该反应的热化学方程式为 。
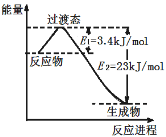
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是制备HCOOH的示意图,根据要求回答问题:
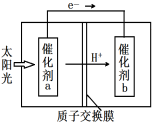
①催化剂b表面的电极反应式为 。
②经测定,若每分钟通过质子交换膜的H+的物质
的量为40mol,则每小时可产生O2 Kg。
高三化学填空题极难题查看答案及解析
-
空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)一定条件下CO2可制得Na2CO3、NaHCO3等。
①等物质的量浓度的Na2CO3、NaHCO3溶液,碱性前者____后者(填“>”“<”或“=”)。
②有下列五种物质的量浓度均为0.1mol/L的电解质溶液,将其稀释相同倍数时,其中pH变化最大的是__(填字母编号)。
A.Na2CO3
B.NaHCO3
C.NaAlO2
D.CH3COONa
E.NaOH
(2)已知反应Fe(s)+CO2(g)
FeO(s)+CO(g) ΔH=a kJ/mol,测得在不同温度下,
该反应的平衡常数K随温度的变化如下:
温度(℃)
300
500
700
K
3.00
3.47
4.40
上述反应中a_______0(填“>”、“<”或“=”);在2L密闭容器中300℃下进行反应,若Fe和CO2的起始量均为4 mol,当达到平衡时CO2的转化率为________。
(3)目前工业上可以用CO2和H2在230℃、催化剂条件下反应生成甲醇蒸汽和水蒸气。下图为恒压容器中0.5 mol CO2和1.5 mol H2反应转化率达80%时的能量变化示意图。则该反应的热化学方程式为__________。
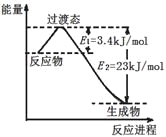
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是制备HCOOH的示意图,根据要求回答问题:
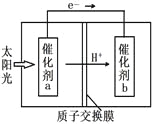
①催化剂b表面的电极反应式为__________。
②经测定,若每分钟通过质子交换膜的H+的物质的量为40mol,则每小时可产生O2_____kg。
高三化学综合题中等难度题查看答案及解析
-
SO2在生产、生活中有着广泛的用途。
(l)请你列举一个SO2在生活中的用途 。
(2)SO2在工业上常用于硫酸生产:2SO2(g)+02(g)
2SO3(g),该反应在一定条件下进行时的热效应如图1所示,则其逆反应的活化能为____。
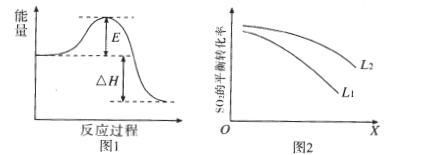
(3)图2中L、X表示物理量温度或压强,依据题中信息可判断:①X表示的物理量是____,理由是____ ;②L1____L2(填“>”,“<”或“:”)。
(4)在容积固定的密闭容器中,起始时充入0.2molSO2和0.1 molO2反应体系起始总压强0.1 MPa。反应在一定的温度下达到平衡时SO2的转化率为90%。该反应的压强平衡常数Kp=____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)利用原电池原理,也可用SO2和O2来制备硫酸,该电池用多孔材料作电极。请写出该电池负极的电极反应式 。
高三化学填空题困难题查看答案及解析
-
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
(1)钢铁锈蚀是目前难以解决的现实问题,电化学腐蚀最为普遍.写出在潮湿空气中钢铁锈蚀时发生还原反应的电极反应式:______.铁锈的主要成分是______(填写化学式),将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并未检测出Fe3+,用离子方程式说明原因:______.
(2)爱迪生蓄电池的反应式为:Fe+NiO2+2H2OFe(OH)2+Ni(OH)2;高铁酸酸钠(Na2FeO4)是一种新型净水剂.用下面装置可以制取少量高铁酸钠.
①此装置中爱迪生蓄电池的负极是______(填“a”或“b”),该电池工作一段时间后必须充电,充电时生成NiO2的反应类型是______.
②写出在用电解法制取高铁酸钠时,阳极的电极反应式______.
③你认为高铁酸钠作为一种新型净水剂的理由可能是______.
A.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
B.高铁酸钠具有强氧化性,能消毒杀菌
C.高铁酸钠在消毒杀菌时被还原生成Fe3+,水解产生氢氧化铁胶体能吸附悬浮杂质.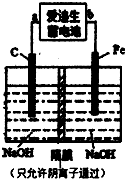
高三化学解答题中等难度题查看答案及解析
-
铁和铁的化合物在工业生产和日常生活中都有广泛的用途。请回答下列问题:
(1)钢铁锈蚀是目前难以解决的现实问题,电化学腐蚀最为普遍。写出在潮湿空气中钢铁锈蚀时发生还原反应的电极反应式:________________________________。
铁锈的主要成分是____________(填写化学式),将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并未检测出Fe3+,用离子方程式说明原因:_____________________。
(2)爱迪生蓄电池的反应式为Fe+NiO2+2H2O
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。

①此装置中爱迪生蓄电池的负极是________(填“a”或“b”),该电池工作一段时间后必须充电,充电时生成NiO2的反应类型是__________。
②写出在用电解法制取高铁酸钠时,阳极的电极反应式__________________________。
③你认为高铁酸钠作为一种新型净水剂的理由可能是______。
A.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
B.高铁酸钠具有强氧化性,能消毒杀菌
C.高铁酸钠在消毒杀菌时被还原生成Fe3+,水解产生氢氧化铁胶体能吸附悬浮杂质
高三化学综合题中等难度题查看答案及解析
-
大豆异黄酮(结构如图)是一种近年来引起营养与医学界广泛关注的物质,它对于人体健康有着重要的作用.关于大豆异黄酮的叙述错误的是( )
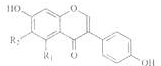
A.可以和溴水反应
B.分子中有两个苯环
C.在碱性条件下容易发生水解
D.1mol大豆异黄酮可以和2molNaOH反应高三化学选择题中等难度题查看答案及解析