-
(10分)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
元素
Al
B
Be
C
Cl[
F
Li
X的数值
1.5
2.0
1.5
2.5
2.8
4.0
1.0
元素
Mg
Na
O
P
S
Si
X的数值
1.2
0.9
3.5
2.1
2.5
1.7
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系_____________________________________________。
(3)请你预测Br与I元素的X数值的大小关系________。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
高二化学填空题中等难度题查看答案及解析
-
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出12种元素的X的数值:
元素
Al
B
Be
C
Cl
F
Li
X的数值
1.5
2.0
1.5
2.5
2.8
4.0
1.0
元素
Mg
Na
O
P
S
Si
N
X的数值
0.9
3.5
2.1
2.5
1.7
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系______________________________。
(3)请你预测Br与I元素的X数值的大小关系________。
(4)某有机物结构简式为:
,在S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
(5) 预测元素周期表中,X值最小的元素位置________(放射性元素除外)。
高二化学填空题中等难度题查看答案及解析
-
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出14种元素的X的数值:
元素
Al
B
Be
C
Cl
F
Li
X的数值
1.5
2.0
1.5
2.5
3.0
4.0
1.0
元素
Mg
Na
O
P
S
Si
N
X的数值
1.2
0.9
3.5
2.1
2.5
1.8
3.0
试结合元素周期律知识完成下列问题(放射性元素除外):
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。判断下列物质是离子化合物还是共价化合物?
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是______________; ②属于共价化合物的是______________.
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系_____________________________________________。
(3)请你预测Br与I元素的X数值的大小关系______________________________。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_____原子(元素符号)。
(5)上表中元素形成的AB型化合物中,离子性最强的是_____________________
(6)请你预测周期表中X的数值最小的元素的位置________周期,______族
高二化学填空题中等难度题查看答案及解析
-
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
元素
Al
B
Be
C
Cl
F
Li
X的数值
1.5
2.0
1.5
2.5
2.8
4.0
1.0
元素
Mg
Na
O
P
S
Si
X的数值
1.2
0.9
3.5
2.1
2.5
1.7
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系_________________________________ 。
(3)请你预测Br与I元素的X数值的大小关系________。
(4)某化合物分子中含有S—N键,你认为该共用电子对偏向于_____原子(填元素符号)。
高二化学填空题中等难度题查看答案及解析
-
下列有关物质性质的比较正确的是 ( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高
②元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强.
⑤还原性:S2->Se2->Br->Cl-⑥酸性:HClO4>H2SO4>H3PO4>H2SiO3
A.①③ B.②④ C.③⑥ D.⑤⑥
高二化学选择题简单题查看答案及解析
-
回答下列问题。
(1)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质,下面给出14种元素的电负性。
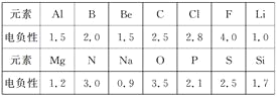
①判断下列化合物中属于离子化合物的是________(填字母);
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
②已知PCl3、NCl3均能发生水解反应,PCl3水解反应的化学方程式为__________________________;NCl3水解产物为____________________。
(2)观察Li、Be、Mg、Al在元素周期表中的位置回答:
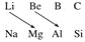
①铍的最高价氧化物的水化物是________(填“酸性”、“碱性”或“两性”)化合物,证明这一结论的有关离子方程式是_____________________________________________________;
②根据Mg在空气中的燃烧情况,Li在空气中燃烧生成产物为__________(用化学式表示)。
(3)现有核电荷数小于20的元素A,其电离能数据如下:(I1表示原子失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:1×102kJ·mol-1)
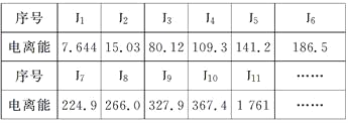
①外层电子离核越远,能量越高,电离能越__________(填“大”或“小”);阳离子电荷数越高,失去电子时,电离能越________(填“大”或“小”);
②上述11个电子分属________个电子层;
③失去了11个电子后,该元素还有________个电子;
④该元素最高价氧化物对应水化物的化学式是______________________________________。
高二化学综合题中等难度题查看答案及解析
-
回答下列问题。
(1)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质,下面给出14种元素的电负性。
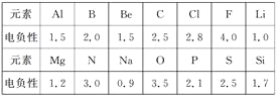
①判断下列化合物中属于离子化合物的是________(填字母);
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
②已知PCl3、NCl3均能发生水解反应,PCl3水解反应的化学方程式为__________________________;NCl3水解产物为____________________。
(2)观察Li、Be、Mg、Al在元素周期表中的位置回答:
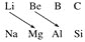
①铍的最高价氧化物的水化物是________(填“酸性”、“碱性”或“两性”)化合物,证明这一结论的有关离子方程式是_____________________________________________________;
②根据Mg在空气中的燃烧情况,Li在空气中燃烧生成产物为__________(用化学式表示)。
(3)现有核电荷数小于20的元素A,其电离能数据如下:(I1表示原子失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:1×102kJ·mol-1)
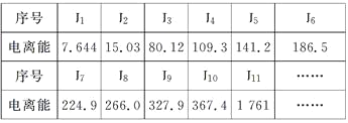
①外层电子离核越远,能量越高,电离能越__________(填“大”或“小”);阳离子电荷数越高,失去电子时,电离能越________(填“大”或“小”);
②上述11个电子分属________个电子层;
③失去了11个电子后,该元素还有________个电子;
④该元素最高价氧化物对应水化物的化学式是______________________________________。
高二化学综合题中等难度题查看答案及解析
-
元素化学性质发生周期变化性质变化的根本原因是
A.元素的原子半径呈周期性的变化
B.元素的化合价呈现周期性变化
C.元素原子核外电子排布呈现周期性变化
D.元素的金属性和非金属性呈周期性变化
高二化学选择题简单题查看答案及解析
-
元素性质的周期性变化不包括
A.原子半径 B.化合价 C.原子核外电子结构 D.金属性和非金属性
高二化学单选题中等难度题查看答案及解析
-
元素的性质呈周期性变化的根本原因是 ( )
A.元素原子量的递增,量变引起质变
B.元素的原子半径呈周期性变化
C.元素的金属性和非金属性呈周期性变化
D.元素原子的核外电子排布呈周期变化
高二化学选择题简单题查看答案及解析