近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。
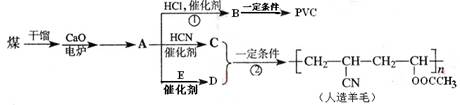
请回答下列问题:
⑴写出反应类型 反应①________
反应②________。
⑵写出结构简式 PVC________ C________。
⑶写出AD的化学反应方程式________。
⑷与D互为同分异构体且可发生碱性水解的物质有________种(不包括环状化合物),写出其中一种的结构简式________。
高三化学推断题中等难度题
近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。

请回答下列问题:
⑴写出反应类型 反应①________
反应②________。
⑵写出结构简式 PVC________ C________。
⑶写出AD的化学反应方程式________。
⑷与D互为同分异构体且可发生碱性水解的物质有________种(不包括环状化合物),写出其中一种的结构简式________。
高三化学推断题中等难度题
高三化学解答题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
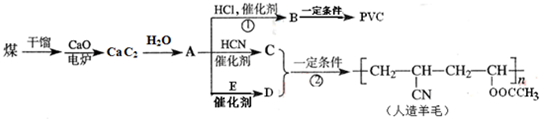
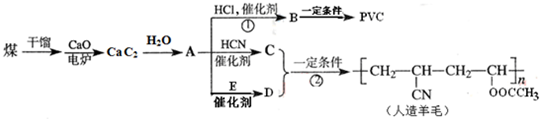
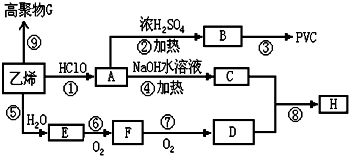
近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。

请回答下列问题:
⑴写出反应类型 反应①________
反应②________。
⑵写出结构简式 PVC________ C________。
⑶写出AD的化学反应方程式________。
⑷与D互为同分异构体且可发生碱性水解的物质有________种(不包括环状化合物),写出其中一种的结构简式________。
高三化学推断题中等难度题查看答案及解析
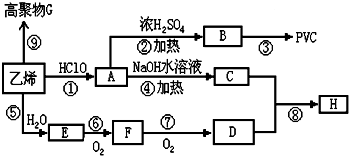
近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以烃A为原料生产人造羊毛的合成路线。
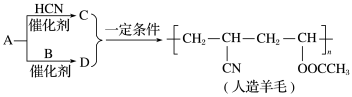
下列说法正确的是 ( )
A.合成人造羊毛的反应属于缩聚反应
B.A生成C的反应属于加成反应
C.A生成D的反应属于取代反应
D.烃A的结构简式为CH2===CH2
高三化学选择题简单题查看答案及解析
近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好,以煤为原杵在不同条件下可合成下列物质(部分条件未标出),C是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:
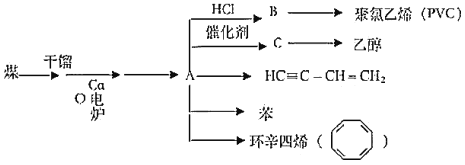
(1)写出A的电子式_____;C的空间构型为平面结构,键角约为_____。
(2)写出乙醇在Cu催化下与O2反应时的方程式_____。
(3)B中所含官能团的名称是_____。
(4)若分别完全燃烧等质量的HC=C—CH=CH2和乙炔,所需氧气的量_____(选填“前者多”“后者多”“一样多”)。
(5)苯乙烯(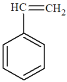 )与环辛四烯互为同分异构体,写出由苯乙烯合成聚苯乙烯的化学方程式_____。
)与环辛四烯互为同分异构体,写出由苯乙烯合成聚苯乙烯的化学方程式_____。
(6)异丙苯(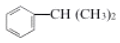 )是苯的同系物。由苯与2—丙醇反应制备异丙苯属于_____反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为_____。
)是苯的同系物。由苯与2—丙醇反应制备异丙苯属于_____反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为_____。
(7)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的结构简式是_____。
高三化学填空题简单题查看答案及解析
化学与生产、生活、科技等密切相关,下列说法正确的是( )
A.由石油制取乙烯、丙烯等化工原料不涉及化学变化
B.“神州七号”的防护层中含聚四氟乙烯,制备聚四氟乙烯的单体属于不饱和烃
C.浓硫酸可用于干燥SO2、C2H4、O2等气体
D.用CO2合成可降解的聚碳酸酯塑料,可以实现“碳”的循环利用
高三化学单选题简单题查看答案及解析
有机化学与材料、生活和环境密切相关。下列说法正确的是
A. 利用植物秸秆可以生产香料乙酸乙酯
B. 从煤焦油中提取苯和苯的同系物,可采取的方法是萃取
C. 用石油裂解产物通过加聚反应直接制备PVC(聚氯乙烯)
D. 油脂在氢氧化钠溶液中加热发生皂化反应,最终生成高级脂肪酸和丙三醇
高三化学选择题中等难度题查看答案及解析
丙烯(C3H6)是石油化工行业重要的有机原料之一,主要用于生产聚丙烯、二氯乙烯、异丙烯等产品。
(1)丙烷脱氢制备丙烯。由图可得C3H8(g)C3H6(g)+H2(g) ΔH=___kJ/mol。
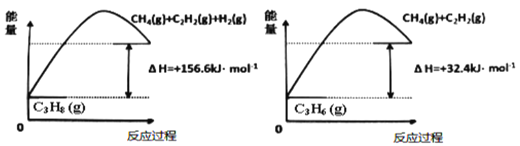
①为了同时提高反应速率和反应物的平衡转化率,可采取的措施是___。
②目前在丙烷脱氢制丙烯时常加入适量的O2,让其同时发生下列反应:
2C3H8(g)+O2(g)2C3H6(g)+2H2O(g) ΔH=-235kJ/mol,通入O2的目的是___。
(2)以C4H8和C2H4为原料发生烯烃歧化反应C4H8+C2H42C3H6(g) ΔH>0。
①某温度下,上述反应中,正反应速率为v正=k正c(C4H8)c(C2H4)、逆反应速率为v逆=k逆c2(C3H6),其中k正、k逆为速率常数,该反应使用WO3/SiO2为催化剂,下列说法中正确的是___。
A.催化剂参与了歧化反应,但不改变反应历程
B.催化剂使k正和k逆增大相同的倍数
C.催化剂降低了烯烃歧化反应的活化能,增大了活化分子百分数
D.速率常数的大小与反应历程无关系
②已知t1min时达到平衡状态,测得此时容器中n(C4H8)=amol,n(C2H4)=2amol,n(C3H6)=bmol且平衡时C3H6的体积分数为25%。再往容器内通入等物质的量的C4H8和C2H4,在新平衡中C3H6的体积分数___25%。(填“>”、“<”、“=”)
(3)工业上可用丙烯加成法制备1,2—二氯丙烷(CH2ClCHClCH3),主要副产物为3—氯乙烯(CH2=CHCH2Cl),反应原理为
Ⅰ.CH2=CHCH3(g)+Cl2(g)CH2ClCHClCH3(g)
Ⅱ.CH2=CHCH3(g)+Cl2(g)CH2=CHCH2Cl(g)+HCl(g)
一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g)。在催化剂作用下发生反应I、Ⅱ,容器内气体的压强随时间的变化如下表所示。
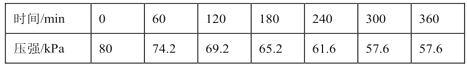
①用单位时间内气体分压的变化来表示反应速率,即v=,则前120min内平均反应速率v(CH2ClCHClCH3)=___kPa•min-1。
②该温度下,若平衡时HCl的体积分数为12.5%,反应Ⅰ的平衡常数Kp=__kPa-1。(Kp为以分压表示的平衡常数,保留小数点后2位。)
高三化学综合题困难题查看答案及解析
高三化学解答题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析