-
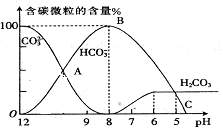
常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40 mL,溶液的pH值逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如右下图所示:
 回答下列问题:
回答下列问题:
(1)在同一溶液中,H2CO3、HCO3-、 CO32- ________(填:“能”或“不能”)大量共存。
(2)当pH=7时,溶液中各种离子其物质的量浓度的大小关系是:_________________。
 (3)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh==2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH=_ _ ___。
(3)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh==2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH=_ _ ___。
(4)若将0.1mol/LNa2CO3溶液与0.1mol/LNaHCO3溶液等体积混合,则混合后的溶液中c(CO32-) c(HCO3-)((填“大于”、“小于”或“等于”)。溶液中c(OH-)—c(H+)=[用 c(HCO3-)、 c(H2CO3)、c(CO32- )的关系式表示]
-
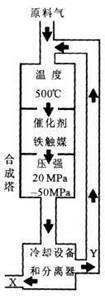
常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.请回答下列问题:
(1)用等式表示Na2CO3溶液中所有阳离子和阴离子浓度的关系:________.
(2)写出Na2CO3溶液中加入少量盐酸的离子方程式________.
(3)当混合液的pH=________时,开始放出CO2气体.
(4)在20mL 0.1mol/LNa2CO3溶液中加入BaCl2粉末3.328×10-7 g时开始产生沉淀X,则KSP(X)=________.

-
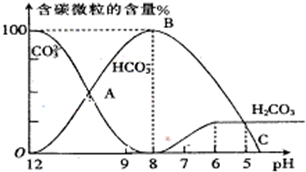
I.常温下在20mL0.1mol∙L-1Na2CO3溶液中逐滴加入0.1mol∙L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是______.
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=______左右最理想.
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是______.
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh= =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A H++HA- HA-
H++HA- HA- H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是______,c(H2A)最大的是______,c(A2-)最大的是______.
-
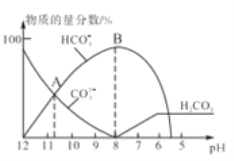
常温下,在10mL0.1mol/LNa2CO3溶液中逐滴加入0..1mol/LHCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是
A.常温下,水解常数Kh(CO32-)的数量级为10-4
B.当溶液是中性时,溶液的总体积大于20mL
C.在0.1mol/LNa2CO3溶液中:c(OH-)>c(H2CO3)+c(HCO3-)+c(H+)
D.在B点所示的溶液中,离子浓度最大的是HCO3-
-
常温下,在10mL0.1mol/LNa2CO3溶液中逐滴加入0..1mol/LHCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是
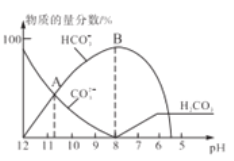
A. 常温下,水解常数Kh(CO32-)的数量级为10-4
B. 当溶液是中性时,溶液的总体积大于20mL
C. 在0.1mol/LNa2CO3溶液中:c(OH-)>c(H2CO3)+c(HCO3-)+c(H+)
D. 在B点所示的溶液中,离子浓度最大的是HCO3-
-
常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是
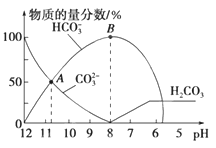
A.在0.1 mol•L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B.当溶液的pH为7时,溶液的总体积为20mL
C.在B点所示的溶液中,浓度最大的阳离子是Na+
D.在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-)
-
常温下,在10mL0.1mol·L−1 Na2CO3溶液中逐滴加入0.1mol·L−1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示,下列说法不正确的是
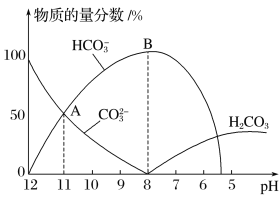
A.溶液的pH为7时,溶液的总体积大于20mL
B.在B点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+c(Cl-)
C.在A点所示的溶液中:c(Na+)=c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
D.已知CO32-水解常数为2×10-4,当溶液中c(HCO3-)=2c(CO32-)时,溶液的pH=10
-
常温下,在10mL0.1mol·L−1 Na2CO3溶液中逐滴加入0.1mol·L−1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示,下列说法不正确的是
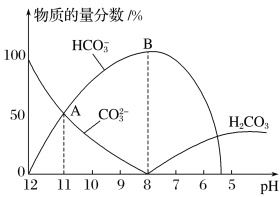
A.溶液的pH为7时,溶液的总体积大于20mL
B.在B点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+c(Cl-)
C.在A点所示的溶液中:c(Na+)=c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
D.已知CO32-水解常数为2×10-4,当溶液中c(HCO3-)=2c(CO32-)时,溶液的pH=10
-
常温下,在10mL0.1mol·L−1 Na2CO3溶液中逐滴加入0.1mol·L−1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示,下列说法不正确的是
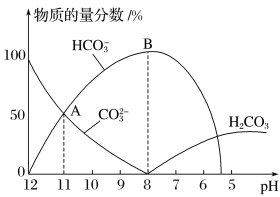
A.溶液的pH为7时,溶液的总体积大于20mL
B.在B点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+c(Cl-)
C.在A点所示的溶液中:c(Na+)=c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
D.已知CO32-水解常数为2×10-4,当溶液中c(HCO3-)=2c(CO32-)时,溶液的pH=10
-
25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.0×10-11。常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入40mL0.1mol/L'HCl溶液,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
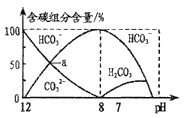
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
B. a点时:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. 当pH=7时,溶液中c(Na+)=c(HCO3-)+2c(CO32-)
D. 当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
 回答下列问题:
回答下列问题: (3)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh==2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH=_ _ ___。
(3)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh==2×10-4,当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH=_ _ ___。







