-
以煤为原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)= 2H2O(g)△H=-483.6kJ/mol
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式_________;
(2)向1L密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g) CH3OCH3(l)+H2O(l)△H=+71kJ/mol
CH3OCH3(l)+H2O(l)△H=+71kJ/mol
①该反应能否_________自发进行(填“能”、“不能”或“无法判断”)
②下列叙述能说明此反应达到平衡状态的是_________.
a.混合气体的平均相对分子质量保持不变 b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变 d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H键断裂
(3)CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H<0 在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g)△H<0 在一定条件下,某反应过程中部分数据如下表:
| 反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 恒温 恒容 (T1℃、 2L) | 0min | 2 | 6 | 0 | 0 |
| 10min | | 4.5 | | |
| 20min | 1 | | | |
| 30min | | | 1 | |
①0~10min内,用H2O(g)表示的化学反应速率v(H20)=_________mol/(L·min)
②达到平衡时,该反应的平衡常数K=_________(用分数表示),平衡时H2的 转化率是_________。
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1_________T2(填“>”、“<”或“=”),理由是_________。在其他条件不变的情况下,若30min时向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡_________移动(填“正向”、“逆向”或“不”).
(4)用甲醚(CH3OCH3)作为燃料电池的原料,请写出在碱性介质中电池负极反应式_________.
-
以煤为原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)= 2H2O(g)△H=-483.6kJ/mol
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式_________;
(2)向1L密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g) CH3OCH3(l)+H2O(l)△H=+71kJ/mol
CH3OCH3(l)+H2O(l)△H=+71kJ/mol
①该反应能否_________自发进行(填“能”、“不能”或“无法判断”)
②下列叙述能说明此反应达到平衡状态的是_________.
a.混合气体的平均相对分子质量保持不变
b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H键断裂
(3)CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H<0在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g)△H<0在一定条件下,某反应过程中部分数据如下表:
| 反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 恒温 恒容 (T1℃、 2L) | 0min | 2 | 6 | 0 | 0 |
| 10min | | 4.5 | | |
| 20min | 1 | | | |
| 30min | | | 1 | |
①0~10min内,用H2O(g)表示的化学反应速率v(H20)=_________mol/(L·min)
②达到平衡时,该反应的平衡常数K=_________(用分数表示),平衡时H2的 转化率是_________。
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1_________T2(填“>”、“<”或“=”),理由是_________。在其他条件不变的情况下,若30min时向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡_________移动(填“正向”、“逆向”或“不”).
(4)用甲醚(CH3OCH3)作为燃料电池的原料,请写出在碱性介质中电池负极反应式_________.
-
合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
(1)已知:2H2(g)+O2(g) 2H2O(g) ΔH=-483.6 kJ·mol-1。则4NH3(g)+3O2(g)
2H2O(g) ΔH=-483.6 kJ·mol-1。则4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=______kJ·mol-1。
2N2(g)+6H2O(g) ΔH=______kJ·mol-1。
(2)如图所示,合成氨反应中未使用催化剂时,逆反应的活化能Ea(逆)=__kJ·mol-1;使用催化剂之后,正反应的活化能为___kJ·mol-1(已知:加入催化剂后,反应分两步进行,反应的活化能是两个过程中需要吸收能量较大的反应的活化能)。
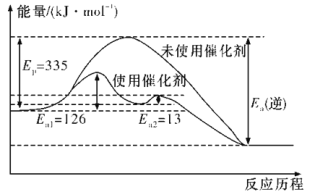
(3)从平衡视角考虑,工业合成氨应该选择常温条件,但实际工业生产却选择500 ℃左右的高温,试解释其原因: ____________________________。
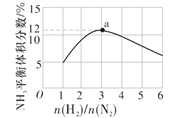
(4)如图表示500 ℃、60 MPa条件下,原料气投料比与平衡时NH3的体积分数的关系。根据图中a点数据计算N2的平衡体积分数为__。
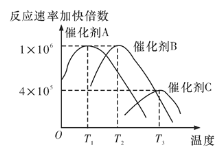
(5)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行实验,所得结果如图所示(其他条件相同),则实际生产中适宜选择的催化剂是__(填“A”“B”或“C”),理由是________。
(6)如图是当反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃反应达到平衡时,混合物中NH3的物质的量分数随总压强的变化曲线。
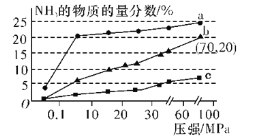
①曲线a、b对应温度较高的是___(填“a”或“b”)。
②列出b点平衡常数的计算式Kp=____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;不要求计算结果)。
-
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g)=2H2O(l) △H=-483.6 kJ· mol–1,
则氢气的燃烧热为483.6kJ· mol–1
B.己知2C(s)+2O2(g)=2CO2(g) △H1 2C(s)+O2(g)=2CO(g) △H2,
则△H1<△H2
C.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
D.已知Ni(CO)4(s)=Ni(s) + 4CO(g) △H>0,则该反应在任何条件下均不能自发进行
-
已知2H2(g)+O2(g) =2H2O(l)△H=—571.6kJ·mol—1,2H2(g)+O2(g)=2H2O(g)△H=—483.6kJ·mol—1。下列说法正确的是
A.1molH2O(l)变成1mo1H2O(g),吸收88 kJ能量
B.1 molH2O(g)分解成H2(g)和O2 (g),吸收241.8kJ能量
C.2 molH2(g)和1molO2(g)的总能量小于2molH2O(l)的能量
D.可以寻找特殊催化剂使H2O分解,同时放出能量
-
已知热化学反应方程式:2H2(g)+O2(g)═2H2O(g)△H1=-483.6kJ/mol
则对于热化学方程式:2H2O(l)═2H2(g)+O2(g)△H2
下列说法正确的是( )
A.热化学方程式中化学计量数表示分子个数
B.该反应的△H2=+483.6 kJ/mol
C.|△H2|<|△H1|
D.|△H2|>|△H1|
-
下列说法正确的是
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ· mol-1,则氢气的燃烧热为
241.8 kJ· mol-1
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ· mol-1
则含0.5mol NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.7kJ
C.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的
D.己知2C(s)+2O2(g)=2CO2(g));△H= a kJ· mol-1、
2C(s)+O2(g)=2CO(g);△H=b kJ· mol-1,则a>b
-
下列依据热化学方程式得出的结论正确的是( )
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.3 kJ·mol-1
则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
C.已知C(石墨,s)=C(金刚石,s);△H>0,则石墨比金刚石稳定
D.己知2C(s)+2O2(g)=2CO2(g));△H=a、2C(s)+O2(g)=2CO(g);△H=b,则a>b
-
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ· mol—1,则氢气的燃烧热为241.8 kJ· mol—1
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ· mol—1
则含20.0g NaOH的稀溶液与稀醋酸完全中和,放出小于28.7kJ的热量
C.已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定
D.己知2C(s)+2O2(g)=2CO2(g));△H=a、2C(s)+O2(g)=2CO(g);△H=b,则a>b
-
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g) + O2(g) = 2H2O(g)△H =–483.6 kJ·mol–1,则氢气的燃烧热为241.8kJ·mol–1
B.已知C(石墨,s) = C(金刚石,s);△H>0,则金刚石比石墨稳定
C.已知NaOH(aq) + HCl(aq) = NaCl(aq) + H2O(l);△H =–57.4 kJ·mol–1,则含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量
D.已知:2C(s) + 2O2(g) = 2CO2(g);△H1,2C(s) + O2(g) = 2CO(g);△H2则△H1>△H2
CH3OCH3(l)+H2O(l)△H=+71kJ/mol
CH3OH(g)+H2O(g)△H<0 在一定条件下,某反应过程中部分数据如下表:



