-
元素A位于第4周期,其基态原子有6个未成对电子;元素B的原子最外层电子数是其内层电子总数的3倍;元素C基态原子的3p轨道上有4个电子,元素D是有机物必不可少的中心元素,E是周期表中原子半径最小的元素。
(1)元素B与元素C可形成多种化合物。
①元素B与C中电负性较大的是______(填元素符号)。
②离子CB42—的空间构型为______(用文字描述)。
(2)B和E形成简单化合物的沸点大于C和E形成的简单化合物,其原因______。
(3)含A3+的溶液与NaCl、氨水反应可得到化合物Na[A(NH3)2Cl4]。
①基态A原子的电子排布式是______。
②1 mol配合物Na[A(NH3)2Cl4]中含σ键的数目为______mol。
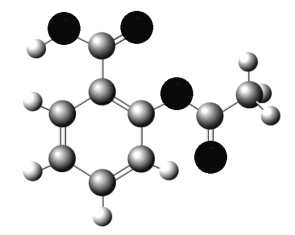
(4)下图为B、D、E三种元素形成的一种化合物的球棍模型,推测该化合物中D原子的杂化方式______。
-
下列四种元素中,其单质氧化性最强的是( )
A.原子含有未成对电子最多的第二周期元素
B.位于周期表中第三周期ⅢA族的元素
C.原子最外层电子排布为2s22p4的元素
D.有9个原子轨道有电子且电子总数最小的元素
-
元素X位于第四周期,其基态原子有4个未成对电子。Y原子最外层电子数是其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子。
(1)Y与Z可形成多种化合物。
① 元素Y与Z中电负性较大的是________(用元素符号描述)。
② 离子ZY32-的空间构型为________(用文字描述)。
③ 写出一种与ZY2互为等电子体的分子的化学式:________。
(2)Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是________。
(3)含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH3)]。1 mol配合物K3[X(CN)5(NH3)]中含σ键的数目为______。
(4)下图为X与Z所形成的一种化合物的基本结构单元,推测该化合物的化学式为______。

-
已知:核电荷数小于18的三种元素X、Y、Z;X原子最外能层的p能级中有一个轨道填充了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的价电子排布式为________,Y的轨道表示式为________。
(2)ZX2的分子构型为________,YX2的电子式为________。
(3)Y与Z形成的化合物中化学键是______键(填“极性”或“非极性”,下同),该分子属于__________分子。
(4)X的最简单氢化物中键角为________,Y的最简单氢化物中中心原子是______杂化。
-
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素原子最外层的p轨道中的电子数等于前一电子层的电子总数,X原子最外层的p轨道中有一个轨道填充了2个电子。
(1)X原子的电子排布式是____________,Y原子的价层电子排布图是: 。
(2)YX2的立体构型是________,YX2的熔、沸点比ZX2________(填“高”或“低”)。
(3)YX2分子中,Y原子的杂化类型是________,一个YX2分子中含________个π键。
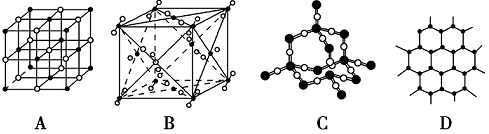
(4)下图表示一些晶体的结构(晶胞),其中代表YX2的是________,代表ZX2的是________(填序号,下同)。
-
已知A、B、C、D、E、W是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E4+与氩原子的核外电子排布相同。W是第四周期d区原子序数最大的元素。请回答下列问题:
(1)填元素名称, C:________写出E的价层电子排布式_________,W在周期表中的位置:___________________
第二周期基态原子未成对电子数与W相同且电负性最小的元素是________(填元素符号).
(2)W(BD)n为无色挥发性剧毒液体,熔点﹣25℃,沸点43℃.不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,W(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________,BD分子的结构式是________
(3)3﹣氯﹣2﹣丁氨酸的结构简式为: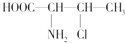 ,一个该有机物分子中含有_____个手性碳原子.
,一个该有机物分子中含有_____个手性碳原子.
-
(12分)化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y为同周期元素,Y与Z为同族元素,Y原子的最外层p能级电子数等于前一电子层电子总数。X原子最外层p能级中只有一个轨道填充了2个电子,则X的电子排布式为________;Y的电子排布式为________;Z的电子排布式为________;YX2的化学式是________,电子式是________ ;ZX2的化学式是________
-
A、B、C、D、E、F、G七种短周期元素,其原子序数依次增大。A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是内层电子数的3倍;D与G处在同一族;F是地壳中含量最高的金属元素。请回答下列问题:
(1)元素F在周期表中的位置 。
(2)B、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(3)配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于 (填晶体类型)。
(4)CA3分子的电子式为 。
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似。ED的熔点比NaCl高,其原因是 。
(6)由A、D、G中任两种元素构成甲、乙两种均含18个电子的分子,所含原子的数目依次为3、4。则甲分子的中心原子采取 杂化;1 mol乙分子含有 molσ键。
-
A、B、C、D、E、F、G七种短周期元素,其原子序数依次增大。A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是内层电子数的3倍;D与G处在同一族;F是
地壳中含量最高的金属元素。请回答下列问题:
(1)元素F在周期表中的位置 。
(2)B、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(3)配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于 (填晶体类型)。
(4)CA3分子的电子式为 。
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似。ED的熔点比NaCl高,其原因是 。
(6)由A、D、G中任两种元素构成甲、乙两种均含18个电子的分子,所含原子的数目依次为3、4。则甲分子的中心原子采取 杂化;1 mol乙分子含有 molσ键。
-
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层p轨道上的电子数等于前一电子层电子总数;X原子最外层的p轨道中有一个轨道填充了2个电子。则
(1)X元素基态原子的电子排布式是________,Y原子的价层电子的电子排布图是_________。
(2)YX2的分子构型是____________。
(3)YX2分子中,Y原子的杂化类型是__________,一个YX2分子中含________个π键。



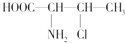 ,一个该有机物分子中含有_____个手性碳原子.
,一个该有机物分子中含有_____个手性碳原子.