-
[2012·江苏卷](10分)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
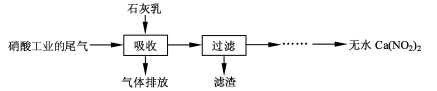
(1)一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)  N2O3(g),其平衡常数表达式为K=________。
N2O3(g),其平衡常数表达式为K=________。
(2)上述工艺中采用气—液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是______________________________;滤渣可循环使用,滤渣的主要成分是__________(填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1∶1。若n(NO)∶n(NO2)>1∶1,则会导致_________________________________;若n(NO)∶n(NO2)<1∶1,则会导致_________________________________。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为______________________________。
-
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO3)2,其部分工艺流程如下:
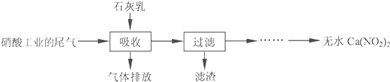
(1)硝酸工业尾气一般用碱液吸收,写出一个吸收尾气离子方程式_____.
(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底部进入,石灰乳从吸收塔顶部喷淋),其目的是___;滤渣可循环利用,滤渣的主要成分是____(填化学式).
(3)该工艺需控制NO和NO2物质的量之比接近1:1.若n(NO):n(NO2)>1:1,则会导致____;若n(NO):n(NO2)<1:1,则会导致_____.
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式___.
-
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
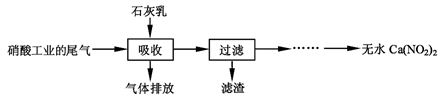
请回答下列问题:
(1)一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)  N2O3(g),其平衡常数表达式为K=________。
N2O3(g),其平衡常数表达式为K=________。
(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底部进入,石灰乳从吸收塔顶部喷淋),其目的是________;滤渣可循环利用,滤渣的主要成分是________(填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1︰1。若n(NO) :n(NO2)>1︰1,则会导致;若n(NO) :n(NO2)<1︰1,则会导致________。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式________。
-
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
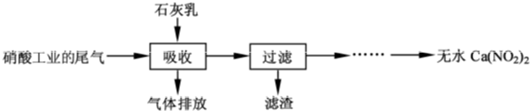
(1)一定条件下,NO 与NO2 存在下列反应:NO(g)+NO2(g)⇌N2O3(g),其平衡常数表达式为K=________.
(2)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是________;滤渣可循环使用,滤渣的主要成分是________(填化学式).
(3)该工艺需控制NO 和NO2 物质的量之比接近1 颐1.若n(NO):n(NO2)>1 颐1,则会导致________;若n(NO):n(NO2)<1 颐1,则会导致________.
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2 会发生分解,产物之一是NO,其反应的离子方程式为________.
-
用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下:
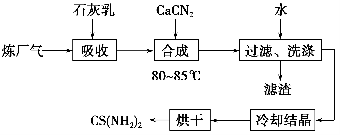
(1)高温下,H2S存在下列反应:2H2S(g)2H2(g)+S2(g),其平衡常数表达式为K=________________。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是_____________________________________________________;
过滤得到的滤渣可再利用,滤渣的主要成分是________(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80~85 ℃)下进行,其目的是_______________________________________。
Ca(HS)2与CaCN2在水溶液中合成硫脲的化学方程式为________________________________。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为________________。
-
用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下:
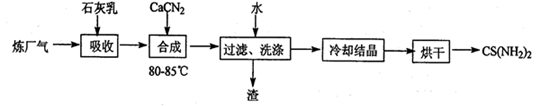
(1)高温下,H2S存在下列反应:2H2S(g)  2H2(g)+S2(g),其平衡常数表达式为K=。
2H2(g)+S2(g),其平衡常数表达式为K=。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是 ________;过滤得到的滤渣可再利用,滤渣的主要成分是 ________(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80℃-85℃)下进行,其目的是 ________。
Ca(HS)2与CaCN2在水溶液中合成硫脉的化学方程式为 。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为 ________。
-
硫及其化合物在化学工业中应用非常广泛.
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中______能导致光化学烟雾的形成;
目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化.
如:CO(g)+NO2(g)⇌NO(g)+CO2(g)△H=-akJ•mol-1(a>0)
2CO(g)+2NO(g)⇌N2(g)+2CO2(g)△H=-bkJ•mol-1(b>0)
则用标准状况下的3.36L CO还原NO2至N2(CO完全反应)的整个过程中放出的热量为______kJ(用含有a和b的代数式表示).
(2)工业上生产硫酸时,将SO2氧化为SO3是关键一步.
①某温度下,已知2SO2(g)+O2(g)⇌2SO3(g),△H=-196kJ•mol-1.开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0mol O2(g),5分钟后反应达到平衡,共放出热量196kJ,该温度下此反应的平衡常数K=______,用O2表示的反应速率为______.
②一定条件下,向一带活塞的密闭容器中充入2mol SO2和1molO2,发生下列反应:2SO2(g)+O2(g)⇌2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是______(填字母).
A.保持温度和容器体积不变,充入2mol SO3
B.保持温度和容器体积不变,充入2mol N2
C.保持温度和容器内压强不变,充入1mol SO3
D.升高温度
E.移动活塞压缩气体
(3)某人设想以右图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式______.

-
硝酸在化学工业中有着极其广泛的应用。
(1)将1.25 mol的NO、NO2、N2O4混合物(其中NO的体积分数为0.60)通入水中,在空气充足的条件下完全反应后可获得硝酸的物质的量范围是_______________。
(2)向稀硝酸中加入18.4 mol/L的浓硫酸(98%)作吸水剂并蒸馏得浓硝酸,当其浓度下降到87%(密度1.8 g/cm3)以下时,则失去吸水能力。50 mL 18.4 mol/L的浓硫酸作为吸水剂时,最多可吸水_________ g。
(3)在65%的HNO3(质量m1)中加入72%的Mg(NO3)2(质量m2)后蒸馏,分别得到97.5%的HNO3和60%的Mg(NO3)2溶液(其中不含硝酸)。若蒸馏过程中,硝酸、硝酸镁均无损耗,H2O的损耗占总质量的5%,则蒸馏前投料比 =______________。
=______________。
(4)硝酸工业中的尾气用烧碱进行吸收产物为NaNO2、NaNO3和H2O。现有含0.50mol氮氧化物的尾气,恰好被一定量的NaOH溶液完全吸收。已知反应后溶液含有0.35molNaNO2。若将尾气NO和NO2的平均组成用NOx表示,则x = 。
-
Ca(NO2)2常用作钢筋混凝土工程中的阻锈剂。硝酸工业尾气中含有大量氮氧化物,含较多NO的尾气可用于制取Ca(NO2)2,工业流程如下:
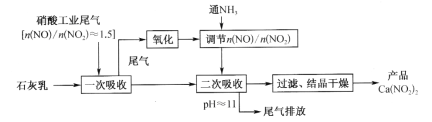
已知:Ca(OH)2 + NO + NO2 Ca(NO2)2 + H2O;
Ca(NO2)2 + H2O;
2Ca(OH)2 + 4NO2 Ca(NO2)2 + Ca(NO3)2 + 2H2O
Ca(NO2)2 + Ca(NO3)2 + 2H2O
回答下列问题:
(1)Ca(NO2)2的名称是____________。
(2)一次吸收后的尾气通过浓硝酸,一部分NO被浓硝酸氧化,反应的化学方程式是____;
在一定条件下,通入NH3将过多的NO2还原为N2以调节n(NO)/n(NO2)的比值,反应中氧化剂与还原剂的物质的量之比为___。
(3)在整个过程中,控制n(NO)/n(NO2)>1的目的是_______________。

(4)用石灰乳两次吸收的目的是_______。
(5)在钢筋混凝土中,Ca(NO2)2可阻止Cl-对钢筋的腐蚀,其原理如下图示,该反应的离子方程式为____________。
(6)产品中主要含有的杂质是Ca(NO3)2。测定Ca(NO3)2含量的实验步骤是:称取0.410g产品溶于水,加入过量Na2SO4溶液,过滤,在滤液中加入足量NH4Cl饱和溶液(发生反应:NH4++NO2- N2 + 2H2O);充分反应后,用稀硫酸酸化,向溶液中加入过量的15.00mL0.1000mol/L (NH4)2Fe(SO4)2溶液至充分反应(假设还原产物为NO);加入N-苯基邻氨基苯甲酸做指示剂,用0.1000mol/LK2Cr2O7标准溶液滴定剩余的Fe2+,消耗标准溶液2.00mL。则:产品中Ca(NO3)2的质量分数为________。
N2 + 2H2O);充分反应后,用稀硫酸酸化,向溶液中加入过量的15.00mL0.1000mol/L (NH4)2Fe(SO4)2溶液至充分反应(假设还原产物为NO);加入N-苯基邻氨基苯甲酸做指示剂,用0.1000mol/LK2Cr2O7标准溶液滴定剩余的Fe2+,消耗标准溶液2.00mL。则:产品中Ca(NO3)2的质量分数为________。
-
I.氯及其化合物在工业生产中有广泛应用。
稀硝酸与活泼金属M反应制备二价金属硝酸盐,当反应物之比m(HNO3):n(M)=5:2时,还原产物为_________(填化学式)。
II.工业废气、汽车尾气中含有的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(一)NOx的消除
汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应2NO(g)+2CO(g) N2(g)+2CO2(g)△H。
N2(g)+2CO2(g)△H。
(1)已知:CO的燃烧热△H1=-283.0kJ·mol-1,N2(g)+O2(g) 2NO(g)△H2=+180.5kJ·mol,则上述反应的△H=_______
2NO(g)△H2=+180.5kJ·mol,则上述反应的△H=_______
(2)某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中的NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示。
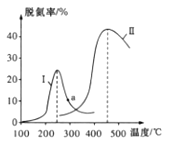
①下列说法正确的是_______(填字、母代号)。
A.两种催化剂均能降低反应的活化能,但反应的△H不变
B.相同条件下,改变压强对脱氮率没有影响
C.曲线Ⅱ中的催化剂适用于450℃左右脱氮
D.曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中催化剂的高
②若温度低于200℃,图中曲线脱氯率随温度升高而变化不大的主要原因是__________;
判断a点对应的脱氮率是否为对应温度下的平衡脱氮率,并说明其理由:____________。
(二)SO2的综合利用
(3)某研究小组对反应NO2(g)+SO2(g) SO3(g)+NO(g)△H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO的平衡转化率[a(NO2)]。部分实验结果如下图所示。
SO3(g)+NO(g)△H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO的平衡转化率[a(NO2)]。部分实验结果如下图所示。
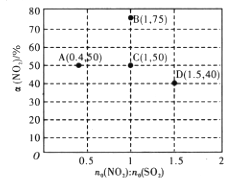
图中C、D两点对应的实验温度分别为TC和TD,通过计算判断:TC______TD(填“>”“=”或“<”)。
(4)已知25℃时,NH3・H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol・L-1,将SO2通入该氨水中,当溶液呈中性时,溶液中的 ______
______

N2O3(g),其平衡常数表达式为K=________。









