-
(1)在2ml 0.1mol/L的NaCl溶液中,加入2ml 0.1mol/L的AgNO3溶液,可观察到的现象是___________,此反应的离子方程式为_______________,将此混合液过滤,滤渣加入2mL 0.1mol/L的KI溶液,搅拌,可观察到的现象是____________________,反应的离子方程式为_________________。
(2)对于Ag2SO4(s)⇌2Ag+(aq)+SO42-(aq),其Ksp的表达式为_______________。
(3)下列说法不正确的是___________
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
B.沉淀反应中常加过量的沉淀剂,其目的是使沉淀尽可能生成
C.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
D.对于Al(OH)3(s)⇌Al(OH)3(aq)⇌Al3++3OH-,前者为溶解平衡,后者为电离平衡
E.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大
高二化学填空题中等难度题查看答案及解析
-
(1)在2mL0.1mol/L的NaCl溶液中,加入2mL0.1mol/L的AgNO3溶液,可观察到______,此反应的离子方程式为________,将此混合液过滤,滤渣加入2mL0.1mol/L的KI溶液,搅拌,可观察到______,反应的离子方程式为______.
(2)对于Ag2S
2Ag++S2-(aq),其Ksp的表达式为=______。
(3)下列说法不正确的是______.
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的;
C.对于Al(OH)3(s)
Al(OH)3(aq)
Al3++3OH-,前者为溶解平衡,后者为电离平衡;
D.除溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大
E.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
高二化学填空题困难题查看答案及解析
-
(1)在2 mL 0.1 mol/L的NaCl溶液中,加入2 mL 0.1 mol/L的AgNO3溶液,可观察到______,此反应的离子方程式为___________________。将此混合液过滤,滤渣加入2 mL 0.1 mol/L的KI溶液,搅拌,可观察到________________,反应的离子方程式为_____。
(2)对于Ag2S(s)
2Ag+(aq)+S2-(aq),其Ksp的表达式为_________。
(3)下列说法正确的是________(填序号)。
A.向Na2SO4溶液中加入过量的BaCl2溶液,则SO42-沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO42-
B.为减少洗涤过程中固体的损耗,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀
C.Ksp小的物质其溶解能力一定比Ksp大的物质的溶解能力小
D.因溶解度小的沉淀易向溶解度更小的沉淀转化,故向ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀
高二化学实验题中等难度题查看答案及解析
-
下列实验“操作和现象”与“结论”都正确的是( )
选项
操作和现象
结 论
A
向盛有2mL 0.1mol/L AgNO3溶液的试管中,先滴几滴0.1mol/L KCl溶液,再滴加0.1mol/L KI溶液。试管中先出现白色沉淀,后出现淡黄色沉淀
Ksp(AgCl)< Ksp(AgI)
B
在分液漏斗中加入碘水后再加入CCl4,充分振荡,静置分层,下层溶液呈紫色
CCl4可作为碘的萃取剂
C
向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变
Fe(NO3)2与H2SO4不反应
D
测定饱和NaClO溶液、CH3COONa溶液的pH, pH(NaClO)> pH(CH3COONa)
弱酸的酸性:
HClO >CH3COOH
高二化学选择题困难题查看答案及解析
-
根据下列实验操作和现象所得到的结论不正确的是
选项
实验操作和现象
结论
A
向2mL浓度均为1.0mol⋅ L−1的NaCl、NaI混合溶液中滴加2~3滴0.0l mol⋅ L−1 AgNO3溶液,振荡,有黄色沉淀产生。
Ksp(AgCl)>Ksp(AgI)
B
向某溶液中加入Ba(NO3)2溶液有白色沉淀产生,再加入足量稀盐酸,白色沉淀不消失。
原溶液中有SO42−
C
向两支分别盛有0.1 mol⋅ L−1醋酸和硼酸溶液的试管中滴加等浓度的Na2CO3溶液,可观察到前者有气泡产生,后者无气泡产生。
电离常数:Ka(CH3COOH)> Ka1(H2CO3)> Ka(H3BO3)
D
在两支试管中各加入4mL0.01 mol⋅ L−1KMnO4酸性溶液和2 mL 0.1 mol⋅ L−1H2C2O4溶液,再向其中一支试管中快速加入少量MnSO4固体,加有MnSO4的试管中溶液褪色较快。
Mn2+对该反应有催化作用
A.A B.B C.C D.D
高二化学单选题中等难度题查看答案及解析
-
已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1.56×10-10。如图是向10 mL AgNO3溶液中逐渐加入0.1 mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图像(实线)。根据图像所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]
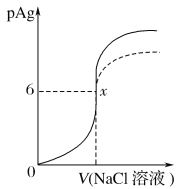
A. 原AgNO3溶液的物质的量浓度为0.1 mol·L-1
B. 图中x点的坐标为(100,6)
C. 图中x点表示溶液中Ag+恰好完全沉淀
D. 把0.1 mol·L-1的NaCl换成0.1 mol·L-1NaI则图像在终点后变为虚线部分
高二化学单选题中等难度题查看答案及解析
-
已知:pAg=-lg c(Ag+),Ksp(AgCl)=1×10-12。如图是向10 mL AgNO3溶液中逐渐加入0.1 mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位:mL)变化的图像(实线)。根据图像所得下列结论正确的是
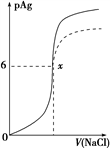
A. 原AgNO3溶液的物质的量浓度为也为0.1 mol·L-1
B. 图中x点的坐标为(10,6)
C. 图中x点可认为溶液中Ag+被沉淀完全
D. 把0.1 mol·L-1的NaCl换成0.1 mol·L-1NaI,则图像在终点后变为虚线部分
高二化学选择题中等难度题查看答案及解析
-
已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1×10-12,如图是向10mL AgNO3溶液中逐渐加入0.1mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象。根据图象所得下列结论不正确的是[提示:Ksp(AgCl)>Ksp(AgI)]
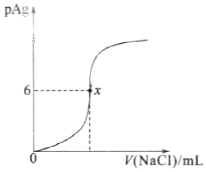
A. 原AgNO3溶液的物质的量浓度为1mol·L-1
B. 图中x点满足c(Ag+)·c(Cl-)= Ks p( AgCl)
C. 相同实验条件下,把0.1mol·L-1的NaCl换成0.1mol·L-1NaI则图象在终点x的纵坐标小于6
D. 相同实验条件下,若改为0.2mol·L-1 NaCl溶液时,x点的横坐标小于100
高二化学单选题中等难度题查看答案及解析
-
下列实验不能成功的是:
①将乙酸和乙醇混合加热制乙酸乙酯
②苯和浓溴水反应制溴苯
③CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型
④用2mL0.1mol/L的CuSO4溶液和2mL0.1mol/L的NaOH溶液混合,然后加入几滴乙醛,加热,根据是否产生红色沉淀来检验醛基。
A.①②③④ B.①③④ C.①②③ D.②③④
高二化学选择题困难题查看答案及解析
-
下列实验不能成功的是:
①将乙酸和乙醇混合加热制乙酸乙酯
②苯和浓溴水反应制溴苯
③CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型
④用2mL0.1mol/L的CuSO4溶液和2mL0.1mol/L的NaOH溶液混合,然后加入几滴乙醛,加热,根据是否产生红色沉淀来检验醛基。
A.①②③④ B.①③④ C.①②③ D.②③④
高二化学单选题困难题查看答案及解析