-
按要求完成下列填空:
(1)常温时,AlCl3的水溶液呈________(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):________________________。AlCl3溶液蒸干并灼烧得到的物质是__________(填化学式)。
(2)泡沫灭火器灭火时发生反应的离子方程是____________;
(3)为了使Na2S溶液中 的比值变小,可加入的物质是_______
的比值变小,可加入的物质是_______
A.适量盐酸 B.适量NaOH溶液
C.适量KOH溶液 D.适量蒸馏水
(4)已知25℃ 时,Ksp[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如要生成Cu(OH)2 沉淀,应调整溶液的pH,使之大于______________。
(5)已知c(Ca2+)≤10-5 mol·L-1时可视为沉淀完全;Ksp(CaCO3)=4.96×10-9。在Ca(NO3)2溶液中加入(NH4)2CO3溶液后过滤,若测得滤液中c(CO )=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
)=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
-
按要求完成下列填空:
(1)将AlCl3溶液加热蒸干并灼烧可得到 (填化学式)。
(2)盛放纯碱溶液的试剂瓶不能用玻璃塞,是因为 。
(3)泡沫灭火器灭火时发生反应的离子方程式是 。
(4)常温下将0.01molCH3COONa和0.02molHCl溶于水,配成0.5L混合溶液。溶液中共有 种粒子,各离子浓度从大到小的顺序为 。
-
请按要求完成下列各项填空:
(1)AlCl3的水溶液呈_______(填“酸”、“中”或“碱”)性,常温时的pH_____7(填“>”、“<”或“=”),原因是(用离子方程式表示):_________________________;实验室在配制 AlCl3溶液时,常将 AlCl3固体先溶于浓盐酸中,然后再用蒸馏水稀释到所需的浓度,以_________(填“促进”或“抑制”)其水解。将AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是________________(填化学式)。
(2)在纯碱溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是___________________________________________,其原因是(以离子方程式和简要的文字说明):_____________________________。
-
请按要求完成下列各项填空:
(1)AlCl3的水溶液呈________(填“酸”、“中”或“碱”)性,常温时的pH________7(填“>”、“<”或“=”),原因是(用离子方程式表示):________;实验室在配制 AlCl3溶液时,常将 AlCl3固体先溶于浓盐酸中,然后再用蒸馏水稀释到所需的浓度,以________(填“促进”或“抑制”)其水解。将AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是________(填化学式)。
(2)在纯碱溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是___________________________________________,其原因是(以离子方程式和简要的文字说明):
__________________________________________________________________________。
-
纯碱工业是基本无机化工之一。完成下列填空:
(1)常温下向纯碱溶液中滴加酚酞试液,溶液变红,原因是___(用离子方程式表示);继续滴加足量氯化钡溶液,可以看到__。
(2)最早的勒布朗法制碱涉及如下反应:Na2SO4+2C+CaCO3 Na2CO3+CaS+2CO2↑。该反应中被还原的元素是___。若转移6.02×1024个电子,生成CO2在标准状况下的体积为__L。
Na2CO3+CaS+2CO2↑。该反应中被还原的元素是___。若转移6.02×1024个电子,生成CO2在标准状况下的体积为__L。
(3)索尔维法(氨碱法)是工业生产纯碱的主要方法,其主要原理可以表示为:NaCl(饱和)+H2O+CO2+NH3=NaHCO3↓+NH4Cl。该反应涉及的各物质中,属于弱电解质的是___。综合平衡理论解释通入CO2和NH3后为何会有NaHCO3析出___。
(4)侯德榜对索尔维法进行了改进,利用平衡移动原理从析出NaHCO3后的母液中提取NH4Cl产品,所需的物质有___(填化学式)。
(5)纯碱厂在生产过程中要时刻关注设备的腐蚀情况。输送饱和食盐水的铸铁管道受到腐蚀时,正极的电极反应方程式为:___。为缓解腐蚀,可在铸铁管道上固定铝-锌-镉三元合金,该方法称为___。
-
(1)在医学上小苏打经常用于治疗胃酸过多,写出其电离方程式__;其水溶液中各离子浓度大小的关系为__。
(2)常温时,AlCl3的水溶液呈酸性的原因是(用离子方程式表示):__。AlCl3溶液蒸干并灼烧得到的物质是__(填化学式)。
(3)泡沫灭火器灭火时发生反应的离子方程是___。
-
按要求回答下列问题:
Ⅰ、稀Na2S溶液有一种臭鸡蛋气味,加入AlCl3溶液后,臭鸡蛋气味加剧,用离子方程式表示气味加剧过程所发生的离子反应方程式_________________________________。
Ⅱ、常温下,向20mL 0.2mol•L﹣1H2A溶液中滴加0.2mol•L﹣1NaOH溶液.有关微粒的物质的量变化如下图(Ⅰ代表H2A,Ⅱ代表HA﹣,Ⅲ代表A2﹣)
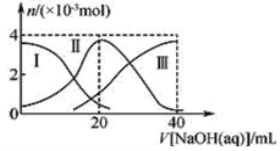
(1)H2A在水中的电离方程式为_________________________。
(2)当V(NaOH)=20 mL时,写出H2A与NaOH反应的离子方程式_________________。此时溶液中所有离子浓度大小关系:__________________。
(3)向NaHA溶液中加水,HA﹣的电离度_________、溶液的pH________。(填增大、减小、不变、无法确定)。
(4)V(NaOH)=30 mL时,溶液中存在如下关系:2c(H+)﹣2c(OH﹣)________2c(A2﹣)﹣3c(H2A)﹣c(HA﹣)(填“<”“>”或“=”)。
(5)某校研究性学习小组开展了题为“H2A是强酸还是弱酸的实验研究”的探究活动。该校研究性学习小组设计了如下方案:你认为下述方案可行的是_______(填编号);
A.测量浓度为0.05 mol/L H2A溶液的pH,若pH大于1,则可证明H2A为弱电解质
B.可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.比较中和等体积、等物质的量浓度的硫酸和H2A溶液所需氢氧化钠的量多少,可证明H2A是强酸还是弱酸。
-
(6分)完成下列离子反应方程式
(1)AlCl3溶液与Na2CO3溶液混合:____________;
(2)向AgCl固体上滴加Na2S溶液,固体变黑色:_________________;
(3)铁在潮湿的空气中发生电化腐蚀时,正极反应式:_________________。
-
(6分)完成下列离子反应方程式
(1)AlCl3溶液与Na2CO3溶液混合:______________;
(2)向AgCl固体上滴加Na2S溶液,固体变黑色:_________________;
(3)铁在潮湿的空气中发生电化腐蚀时,正极反应式:_________________。
-
常温下,下列溶液中由水电离的氢离子浓度为1×10-5的是 ( )
A.pH=5的HClO 溶液 B.pH=9的氨水
C.pH=5的AlCl3溶液 D.pH=5的NaHSO4溶液
的比值变小,可加入的物质是_______
)=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
