-
某配位化合物为深蓝色晶体,由原子序数由小到大的A,B,C,D,E五种元素组成,其原子个数比为14∶4∶5∶1∶1。其中C,D同主族且原子序数D为C的2倍,E元素的外围电子排布式为(n-1)dn+6ns1,试回答下列问题:
(1)元素B,C,D的第一电离能由大到小排列顺序为________(用元素符号表示)。
(2)D元素基态原子的最外层电子排布图为________。
(3)该配位化合物的化学式为________,配体的中心原子的杂化方式为________。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可以任意比互溶,解释其主要原因为_______________。
(5)A元素与B元素可形成分子式为B2A2的某化合物,该化合物的分子具有平面结构,则其结构式为________,分子中含有________个σ键,________个π键。
高二化学综合题中等难度题查看答案及解析
-
某配位化合物为深蓝色晶体,由原子序数由小到大的A,B,C,D,E五种元素组成,其原子个数比为14∶4∶5∶1∶1。其中C,D同主族且原子序数D为C的2倍,E元素的外围电子排布式为(n-1)dn+6ns1,试回答下列问题:
(1)该配位化合物的化学式为________________________,配合物中采取sp3杂化的原子按第一电离能由大到小排列顺序为______________(用元素符号表示),1mol配离子中含有的σ键数目为_________________。
(2)D元素基态原子的最外层电子排布图为_______________________________。
(3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可以任意比互溶,解释其主要原因为_________________________________。
(4)A元素与B元素可形成分子式为B2A2的某化合物,该化合物的分子具有平面结构,则其结构式为________,该分子中B元素的杂化方式为________。
(5)该配合物溶于水得深蓝色溶液,加入乙醇溶剂,将析出深蓝色的晶体,则加入乙醇的作用是____________________________________________________。
高二化学解答题中等难度题查看答案及解析
-
(Ⅰ)由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素原子的电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为____________。
(2)元素B、C、D的第一电离能由小到大排列顺序为____________。(用元素符号表示)
(3)D元素原子的最外层电子轨道表示式为____________。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为____________。
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式____________。
(Ⅱ).卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6____________HIO4(填“>”“<”或“=”)。
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6____________HIO4(填“>”“<”或“=”)。(2)下图为碘晶体晶胞结构。有关说法中正确的是____________。

碘晶体晶胞
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
高二化学填空题简单题查看答案及解析
-
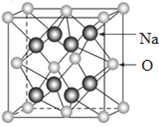
已知元素A为O,元素B为Na(大黑球代表Na),A与B能够形成化合物F,其晶胞结构如图所示,晶胞边长参数acm,F的化学式为___,晶胞中A原子的配位数为___,列式计算晶体F的密度___(g•cm-3)(仅需列出表达式)。
高二化学计算题中等难度题查看答案及解析
-
A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质.B、E均为组成空气的成分.F的焰色反应呈黄色.在G中,非金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图所示(图中部分产物未列出):

请填写下列空白:
(1)A是______,C是______.
(2)H与盐酸反应生成E的化学方程式是:______.
(3)写出E只与F反应的化学方程式是:______.
(4)F与G的水溶液恰好反应只生成I和D的离子方程式是:______.高二化学解答题中等难度题查看答案及解析
-
(10分)A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如右(图中部分产物未列出):

请填写下列空白:
(1)A________,C是________。
(2)H与盐酸反应生成E的化学方程式是________。
(3)E与F反应的化学方程式是________。
(4)F与G的水溶液反应生成I和D的离子方程式是________
高二化学填空题简单题查看答案及解析
-
(15分)A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如下(图中部分产物未列出):

请填写下列空白
(1)A是________,B是________, C是________。
(2)H与盐酸反应生成E的化学方程式是________。
(3)E与F反应的化学方程式是________。
(4)F与G的水溶液反应生成I和D的离子方程式是________。
高二化学填空题简单题查看答案及解析
-
A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如右(图中部分产物未列出):

请填写下列空白:
①.A是________,C是________。
②.H与盐酸反应生成E的化学方程式是________。
③.E与F反应的化学方程式是________。
④.F与G的水溶液反应生成I和D的离子方程式是________。
高二化学填空题简单题查看答案及解析
-
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)X元素是______
(2)X与W组成的化合物中存在______键(填“离子”“共价”).
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为______.
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下A与NaOH溶液反应的离子方程式______.
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式______.高二化学解答题中等难度题查看答案及解析
-
原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式 ;其中含有的化学键是 。
(2)用电子式表示Y2O的形成过程_______________________。
(3)X、Z、W三种元素的最高氧化物对应的水化物只,稀溶液氧化性最强的是____________(填写化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是 (填写化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式__________________。
高二化学填空题困难题查看答案及解析