-
根据元素周期律,下列关系正确的是
A. 原子半径:Cl>P
B. 碱性:NaOH>KOH
C. 热稳定性:SiH4>CH4
D. 还原性:S2->F-
高三化学单选题中等难度题查看答案及解析
-
根据元素周期律可判断( )
A.稳定性:H2S>H2O B.最高化合价:F>N
C.碱性:NaOH>Mg(OH)2 D.原子半径:Cl>Al
高三化学单选题中等难度题查看答案及解析
-
下列说法正确的是( )
A.第二周期元素从C到F,非金属性逐渐减弱
B.第三周期元素从Na到Cl,原子半径逐渐增大
C.HF、HCl、HBr、HI的热稳定性依次逐渐减弱
D.LiOH、NaOH、KOH的碱性依次逐渐减弱高三化学选择题中等难度题查看答案及解析
-
下列关于周期表的说法正确的是( )
A.C和Si属于第ⅣA族元素,SiH4比CH4稳定
B.N和B属于第二周期元素,原子半径:N>B
C.S和Cl属于第三周期元素,其含氧酸的酸性:H2SO4<HClO3
D.某元素氢化物的化学式为RH3,则其最高价氧化物的水化物可能为HRO3
高三化学单选题中等难度题查看答案及解析
-
根据元素周期表和元素周期律,判断下列叙述不正确的是( )

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 已知Ra是第七周期ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强
C. 如上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“
”(ào)命名的第118号元素在周期表中位于第七周期0族
高三化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A. Si、P、S、Cl原子半径依次增大
B. HF、HCl、HBr、HI稳定性依次减弱
C. C、N、O、F 元素的最高正化合价依次升高
D. NaOH、Mg(OH)2、Al(OH)3碱性依次增强
高三化学单选题简单题查看答案及解析
-
已知33As、35Br位于同一周期。下列关系正确的是( )
A. 原子半径:As>Cl>P
B. 热稳定性:HCl>AsH3>HBr
C. 还原性:As3->S2->Cl-
D. 酸性:H3AsO4>H2SO4>H3PO4
高三化学选择题中等难度题查看答案及解析
-
依据元素周期表及元素周期律,下列推断正确的是( )
A.同周期主族元素的原子形成的简单离子电子层结构相同
B.C比Si的原子半径小,CH4的稳定性比SiH4弱
C.Na、Mg、Al失电子能力和其最高价氧化物对应的水化物的碱性均依次减弱
D.在元素周期表金属与非金属的分界处可以寻找催化剂和耐高温、耐腐蚀的合金材料
高三化学选择题中等难度题查看答案及解析
-
下列事实中,不能用元素周期律解释的是
A. 原子半径:K > Ca > Mg
B. 碱性:NaOH > Mg(OH)2 > Al(OH)3
C. 热稳定性:HF > HCl > H2S
D. 酸性:H2SO3 > H2CO3 > H2SiO3
高三化学单选题中等难度题查看答案及解析
-
根据元素周期表和元素周期律,判断下列叙述不正确的是( )
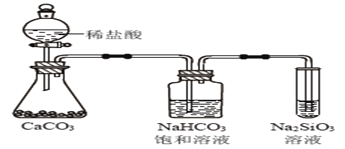
A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 图1所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“
”(ào)命名的第118号元素在周期表中位于第七周期0族
高三化学选择题中等难度题查看答案及解析