-
已知拆开1mol H–H键, 1mol N≡N键分别需要吸收的能量为436kJ 、946kJ;形成1mol N–H键,会放出能量391kJ,在反应N2 + 3H2 2NH3中,每生成2mol NH3,
2NH3中,每生成2mol NH3,
A.放出92 kJ热量 B.吸收92 kJ热量
C.放出209kJ热量 D.吸收209kJ热量
-
已知拆开1mol H-H键、1molN≡N和1mol N—H键分别需要的能量是436kJ、 948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为:________。
-
(1)在一定条件下N2与H2反应生成NH3,已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、945.7 kJ,则N2与H2反应生成NH3的热化学方程式为:_____。
(2)N2H4和H2O2混合可作火箭推进剂,已知:16 g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6 kJ 的热量,反应N2H4(l)+O2(g)=N2(g)+2H2O(l)的△H=_____kJ•mol-1。
已知:2H2O2(l)=O2(g)+2H2O(l) △H=-196.4 kJ•mol-1.N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为_____。
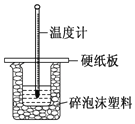
(3)实验室用50 mL 0.50 mol•L-1盐酸与50 mL某浓度的NaOH溶液在如下图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有一处明显的错误,该处错误是缺少一种玻璃仪器,该仪器的名称为_____;实验室提供了0.50 mol•L-1和0.55 mol•L-1两种浓度的NaOH溶液,应选择_____ mol•L-1的溶液进行实验。
-
根据所学知识填写下列空白。
(1)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成1mol NH3的反应热ΔH =__________________。
(2)氢气的燃烧热为286kJ/mol。写出表示氢气燃烧热的热化学方程式____________________________________________。
(3)某温度下纯水中的c(H+) = 1×10-6.5mol/L。若温度不变,滴入稀硫酸使c(H+)= 5×10-5mol/L,则由水电离出的c(H+) =__________mol/L。
(4)已知在第(3)问条件下,盐酸的pH=a,氢氧化钡的pH=b。若酸碱按体积比1:10混合后溶液显中性,则a+b=_________。
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-, HB-  H++B2-。
H++B2-。
已知0.1 mol/L NaHB溶液的pH=2,则0.1 mol/L H2B溶液中c(H+)小于0.11 mol/L的原因是____________________________________。
-
(1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_________________。
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,回答下列问题:
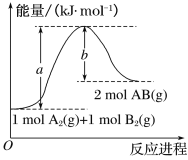
①该反应的ΔH_______0(填 “大于”“小于”或“等于”);
②反应物的总键能为______________;
③写出该反应的热化学方程式________________________________。
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
写出联氨的结构式_______________,上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为_______________________________。
-
(1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_________________。
(2)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,回答下列问题:
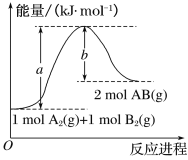
①该反应的ΔH_______0(填 “大于”“小于”或“等于”);
②反应物的总键能为______________;
③写出该反应的热化学方程式________________________________。
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
写出联氨的结构式_______________,上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为_______________________________。
-
(共11分) 拆开1mol H—H键,1mol N—H键,1mol N三N键分别需要吸收的能量为436kJ ,391kJ,946kJ(计算结果保留到整数)
写出此反应的热化学方程式(此空5分)________
则1mol N2 完全生成NH3 ________热量(填:吸收或放出)________ kJ;
1mol H2完全生成NH3 ________ 热量(填:吸收或放出)________ kJ;
理论上,完全分解1mol NH3________热量(填:吸收或放出)________ kJ
-
NH3是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
| 共价键 | H―H | N≡N | N―H |
| 键能/ kJ·mol-1 | 436 | 946 | 391 |
注:拆开气态物质中1 mol某种共价键需要吸收的能量,就是该共价键的键能。
N2 (g)+3 H2 (g) 2 NH3 (g) H =_____kJ·mol-1
2 NH3 (g) H =_____kJ·mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2+3H2 2NH3,测得各组分浓度随时间变化如图8所示。
2NH3,测得各组分浓度随时间变化如图8所示。
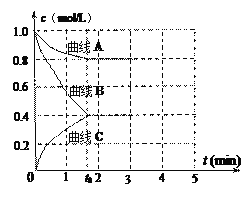
①表示c(N2)的曲线是__________(填“曲线A”、“曲线B”或“曲线C”)。
② 0~t0时用H2表示的反应速率:v(H2)=___________________mol·L-1·min-1。
③ 下列能说明该反应达到平衡的是________。
a.混合气体的压强不再变化
b.2c(H2)= 3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
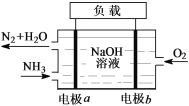
① 电极b名称是__________。
② 电解质溶液中OH-离子向________移动(填“电极a”或“电极b”)。
③电极a的电极反应式为______________________。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是___________________________________________。
-
氮元素可形成多种化合物,在工业生产中具有重要价值。 请回答下列问题:
(1)已知拆开1molH-H 键,1molN-H键, 1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应合成NH3的热化学方程式为 ______________________。
(2)一定温度下,2L密闭容器中充入0.40 mol N2O4,发生反应:N2O4(g) 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| C(NO2)/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
①20 s内,v(NO2)=___________mol·L-1·s-1。
②升高温度时,气体颜色加深,则正反应是_________(填“放热”或“吸热”)反应。
③该温度下反应的化学平衡常数数值为_____________。
④相同温度下,若开始向该容器中充入0.80molNO2,则达到平衡后: c(NO2) ______ 0.30mol·L-1(填“>”、 “=”或“<”)
(3)N2O5是一种新型硝化剂,其性质和制备受人们关注。现以 H2、O2、熔融盐 Z(Na2CO3)组成的燃料电池电解制备N2O5,装置如图所示,其中Y为CO2。
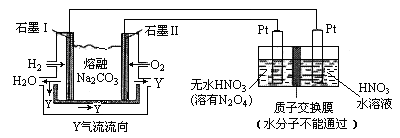
①写出石墨I电极上发生反应的电极反应式 _____________________________;
②在电解池中生成N2O5的电极反应式为 ____________________________
-
依据事实,写出下列反应的热化学方程式。
(1)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式___。





