乳酸薄荷酯有轻微的薄荷香气,尝起来几乎没有味道,但伴有持久的、令人愉快的清凉效果,主要应用于日化产品、药物制备、口腔产品和糖果等产品。其结构如右图,下列说法正确的是
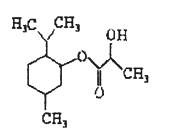
A. 该有机物属于芳香化合物
B. 该有机物可以发生取代、加成和氧化反应
C. 该有机物可溶于水
D. 该有机物能与强碱溶液发生反应
高三化学单选题中等难度题
乳酸薄荷酯有轻微的薄荷香气,尝起来几乎没有味道,但伴有持久的、令人愉快的清凉效果,主要应用于日化产品、药物制备、口腔产品和糖果等产品。其结构如右图,下列说法正确的是

A. 该有机物属于芳香化合物
B. 该有机物可以发生取代、加成和氧化反应
C. 该有机物可溶于水
D. 该有机物能与强碱溶液发生反应
高三化学单选题中等难度题
乳酸薄荷酯有轻微的薄荷香气,尝起来几乎没有味道,但伴有持久的、令人愉快的清凉效果,主要应用于日化产品、药物制备、口腔产品和糖果等产品。其结构如右图,下列说法正确的是

A. 该有机物属于芳香化合物
B. 该有机物可以发生取代、加成和氧化反应
C. 该有机物可溶于水
D. 该有机物能与强碱溶液发生反应
高三化学单选题中等难度题查看答案及解析
乳酸薄荷酯清凉效果持久,可调制出清爽怡人的清凉产品,其结构简式如图所示。下列有关乳酸薄荷酯的说法正确的是

A.乳酸薄荷酯的摩尔质量为214g
B.乳酸薄荷酯能使溴的四氯化碳溶液褪色
C.乳酸薄荷酯能与NaOH溶液反应
D.乳酸薄荷酯属于芳香族化合物
高三化学选择题中等难度题查看答案及解析
乳酸薄荷酯简称ML,可添加到牙膏、口香糖、饮料等中,有长效的清凉效果,其结构简式如下图所示。下列说法正确的是
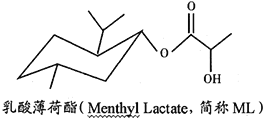
A. ML的分子式为:C13H28O3 B. 1mol ML完全水解能消耗2mol NaOH
C. ML发生消去反应的产物只有一种结构 D. ML分子中的所有碳原子在同一平面上
高三化学单选题中等难度题查看答案及解析
乙酸龙脑酯又名乙酸冰片酯,结构示意图如图。具有清凉的松木香气,是日化香精配制常用的香精。下列关于乙酸龙脑脂的说法正确的是
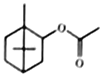
A. 乙酸龙脑酯的分子式为C12H22O2
B. 乙酸龙脑酯的一氯代物有9种
C. 乙酸龙脑酯可以发生加成、消去、氧化等反应
D. 乙酸龙脑酯可由1,7,7-三甲基二环庚烷-2-醇(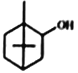 )与乙酸发生取代反应制得
)与乙酸发生取代反应制得
高三化学单选题中等难度题查看答案及解析
环戊酮的各种衍生物具有独特的性能,如α—正己基环戊酮具有清新天然果香气息,并带有较强烈的薄荷凉爽感,香气强度好,留香较持久,可用于牙膏香精、口香糖香精及各种略带凉味、果味的食用香精中。近年来,人们还发现了α—烃基环戊酮具有非常好的抗癌性能,如α—甲基环戊酮 。其可以利用环己醇来合成,合成线路如下:
(1)写出A、B的结构简式。
A______________________________________ B_________________________________
(2)浓硝酸氧化环己醇的反应是一个大量放热的反应,因此在实验中,能够观察到的明显现象是______________________________,为了充分利用原料,液体环己醇的加入方式是_____________________,实验中采用的硝酸浓度是50%,为什么不采用更大尝试的硝酸?_____________________________________________________。
(3)用5.3mL的环己醇和30mL 50%的硝酸制备己二酸(设硝酸的不愿产物为NO),试估算其理论产量。
高三化学填空题困难题查看答案及解析
在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式: 。
(3)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因 。常温下HClO的电离平衡常数为 。洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式 。
(4)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH
K2FeO4在水溶液中易水【解析】
4FeO42-+10H2O4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
高三化学填空题困难题查看答案及解析
在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式: 。
(3)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因 。常温下HClO的电离平衡常数为 。洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式 。
(4)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH;K2FeO4在水溶液中易水【解析】
4FeO42-+10H2O4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
高三化学填空题困难题查看答案及解析
在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式: 。
(3)洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是
A.酸性:HF>HCl>HBr>HI B.键能:H—F>H—Cl>H—Br>H—I
C.熔点:HF<HCl<HBr<HI D.还原性:HF<HCl<HBr<HI
(4)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因 。
常温下HClO的电离平衡常数为 。
洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式 。
(5)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH
K2FeO4在水溶液中易水【解析】
4FeO42-+10H2O4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
A.水 B.NH4Cl、异丙醇 C.Fe(NO3)3、异丙醇 D.CH3COONa、异丙醇
(6)消毒效率是物质单位质量得到的电子数,则Cl2与NaClO两种消毒剂的消毒效率之比为 。
高三化学填空题极难题查看答案及解析
异戊酸薄荷酯(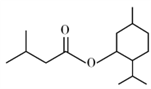 )是一种治疗心脏病的药物,制备异戊酸薄荷酯P的流程如下:
)是一种治疗心脏病的药物,制备异戊酸薄荷酯P的流程如下:

已知: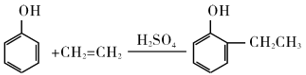 ;
;

完成下列问题:
(1)A的化学名称为____。试剂1的结构简式为____。
(2)由E生成F的化学方程式为____。
(3)试剂2可以是____试剂(填名称或化学式);该反应类型是 ____。
(4)由C和H生成P的化学方程式为____。
(5)M有多种同分异构体,写出所有满足下列条件的同分异构体的结构简式:____。
①属于酚类 ②能发生银镜反应
③核磁共振氢谱有4种峰、且峰值比为1:2:2:1
(6)苯乙烯是一种重要的化工原料。参考制备异戊酸薄荷酯中的方法,设计以苯、乙烯为有机原料(无机试剂自选),制备苯乙烯的合成线路:___。
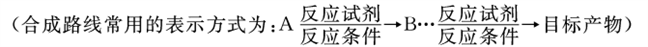
高三化学推断题中等难度题查看答案及解析
某有机物Z具有美白功效,广泛用于日化产品。该物质可用如下反应制备
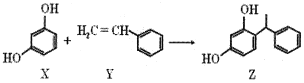
下列叙述错误的是( )
A.X、Y和Z均能和溴水发生反应
B.X和Z均能与Na2CO3溶液反应,但不会放出CO2
C.Y既能发生取代反应,也能发生加聚反应
D.Y分子中所有碳原子一定不共平面
高三化学单选题中等难度题查看答案及解析