-
Ⅰ.纳米级Cu2O既是航母舰艇底部的防腐蚀涂料,也是优良的催化剂。
(1)已知:C(s)+ O2(g)=CO(g)ΔH =–110.4kJ•mol-1,
O2(g)=CO(g)ΔH =–110.4kJ•mol-1,
2Cu2O(s)+O2(g)= 4CuO(s) ΔH =–292kJ•mol-1 ,则工业上用碳粉与CuO粉末混合在一定条件下反应制取Cu2O(s),同时生成CO气体的热化学方程式为________。
(2)用纳米级Cu2O作催化剂可实现甲醇脱氢制取甲醛:
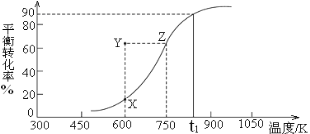
CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如右图所示。
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如右图所示。
①该反应的ΔH___0 (填“>”或“<”);600K时,Y点甲醇的v(正) ____v(逆)(填“>”或“<”)。
②从Y点到X点可采取的措施是___________________________________。
③在t1K时,向固定体积为2L的密闭容器中充入1molCH3OH(g),温度保持不变,9分钟时达到平衡,则0~9min内用CH3OH(g)表示的反应速率v(CH3OH)=_____________, 温度为t1时,该反应的平衡常数K=____________。
Ⅱ.金属铜因导电性强而应用广泛。
由黄铜矿冶炼得到的粗铜经过电解精炼才能得到纯铜。电解时,粗铜作______极,阴极的电极反应式为_______________。
Ⅲ.含铜离子的的废水会造成污染,通常将其转化为硫化铜沉淀而除去。
已知:Ksp[CuS]=1×10-36,要使铜离子的浓度符合排放标准(不超过0.5mg/L),溶液中的硫离子的物质的量浓度至少为__________mol/L(保留至小数点后一位)。
-
纳米级Cu2O既是航母舰艇底部的防腐蚀涂料,也是优良的催化剂。
(1)已知:1克碳粉燃烧全部生成CO气体时放出9.2kJ热量,2Cu2O(s)+O2(g)= 4CuO(s) ΔH =–292kJ•mol-1 ,则工业上用碳粉与CuO粉末混合在一定条件下反应制取Cu2O(s),同时生成CO气体的热化学方程式为________________________________________。
(2)用纳米级Cu2O作催化剂可实现甲醇脱氢可制取甲醛:
CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。
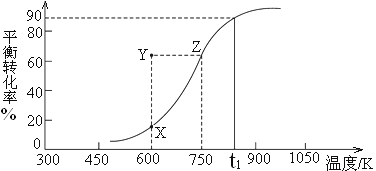
①该反应的ΔH___0 (填“>”或“<”);600K时,Y点甲醇的υ(正) ____υ(逆)(填“>”或“<”)。
②从Y点到X点可采取的措施是___________________________________。
③在t1K时,向固定体积为2L的密闭容器中充入1molCH3OH(g),温度保持不变,9分钟时达到平衡,则0~9min内用CH3OH(g)表示的反应速率v(CH3OH)=_____________, t1K时,该反应的平衡常数K=____________。
(3)研究表明,纳米级的Cu2O也可作为太阳光分解水的催化剂。
① 其他条件不变时,若水的分解反应使用Cu2O催化剂与不使用催化剂相比,使用催化剂会使该反应的活化能___________ (填“增大”、“减小”或“不变”),反应热(ΔH)______(填“增大”、“减小”或“不变”)。
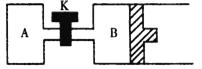
② 如图所示,当关闭K时,向容器A、B中分别充入0.04molH2O(g),起始时V(A) = V(B) = 2L。在一定条件下使水分解(反应过程中温度保持不变,B中活塞可以自由滑动),达到平衡时,V(B) = 2.4L。平衡时,两容器中H2O(g)的分解率A_____________B (填“<”、“=”或“>”)。打开K,过一段时间重新达平衡时,B的体积为____________L。(连通管中气体体积不计)。
-
Cu及化合物在生产、国防中有重要的应用。
I.纳米级Cu2O既是航母舰艇底部的防腐蚀涂料,也是优良的催化剂。
(1)已知:Cu2O(s)+ O2(g)=2CuO(s) ΔH=-196kJ/mol
O2(g)=2CuO(s) ΔH=-196kJ/mol
2C(s)+O2(g)=2CO(g) ΔH=-220.8kJ/mol
则工业上用碳粉与CuO粉末混合在一定条件下反应制取Cu2O(s),同时生成CO气体的热化学方程式为___。
(2)用纳米级Cu2O作催化剂可实现甲醇脱氢制取甲醛:CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。
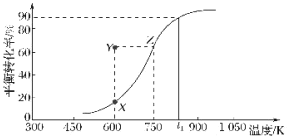
①该反应的ΔH___0(填“>”或“<”);600K时,Y点甲醇的v(正)___v(逆)(填“>”或“<”)。
②在t1K时,向固定体积为1L的密闭容器中充入2molCH3OH(g),温度保持不变,9分钟时达到平衡,则0~9min内用CH3OH(g)表示的反应速率v(CH3OH)___,温度为t1时,该反应的平衡常数K的值为___。
II.Cu既是常见的催化剂,又是常见的电极材料。
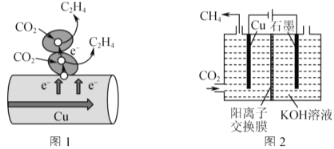
(3)图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当直接传递的电子物质的量为2mol时,则参加反应的CO2的物质的量为___。
(4)图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为___。
III.含铜离子的废水会造成污染,通常将其转化为硫化铜沉淀而除去。
(5)已知:Ksp(CuS)=1×10-36,要使铜离子的浓度符合排放标准(不超过0.4mg/L),溶液中的硫离子的物质的量浓度至少为___mol/L(保留至小数点后一位)。
-
纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
①2Cu(s)+ O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
②C(s)+ O2===CO(g) ΔH=-110.5 kJ·mol-1,
O2===CO(g) ΔH=-110.5 kJ·mol-1,
③2Cu(s)+ O2(g)===2CuO(s) ΔH=-314 kJ·mol-1
(1)则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为______________________。
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
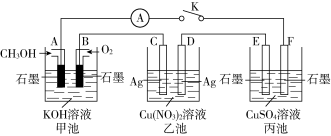
请回答下列问题:
①甲池为__________(填“原电池”“电解池”或 “电镀池”),A电极的电极反应式为______________
②丙池中电池总反应的离子方程式:_______________________
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为______mL(标准状况)。
④一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是________(填选项字母)。
A.CuO B. Cu C.Cu(OH)2 D.Cu2(OH)2CO3
-
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:

(1)已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H=akJ·mol-1
C(s)+1/2O2(g)=CO(g);△H=bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s);△H=ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=_________kJ·mol-1
(2)工业上极少用方法I制取Cu2O是由于方法I反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因:________________。
(3)方法II为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为_________________________。
(4)方法III采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如下图所示:写出电极反应式并说明该装置制备Cu2O的原理___________________。
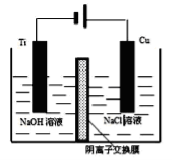
(5)在相同的密闭容器中.用以上两种方法制得的Cu2O分别进行催化分解水的实验:
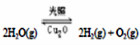 △H>0,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示:
△H>0,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示:
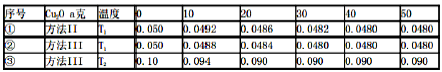
下列叙述正确的是_________(填字母)。
A.实验的温度:T2<T1
B.实验①前20min的平均反应速率v(O2)=7×10-5mol·L-1·min-1
C.实验②比实验①所用的Cu2O催化效率高
D.实脸①、②、③的化学平衡常数的关系:K1=K2<K3
-
纳米级Cu2O由于具有优良的催化性能而受到关注。
(1)已知:①2Cu(s)+1/2O2(g)=Cu2O(s) △H=-169kJ/mol
②C+1/2O2(g)=CO(g) △H=-110.5kJ/mol
③Cu(s)+1/2O2(g)=CuO(s) △H=-157kJ/mol
用炭粉在高温条件下还原CuO的方法制得纳米级Cu2O的热化学方程式为_______________。
(2)采用离子交换膜控制电解液中OH-的浓度也可以制备纳米级Cu2O,装置如右图所示:
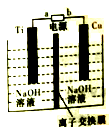
为保证电解能持续稳定进行,若电解槽中的离子交换膜只允许一种离子通过,则该交换膜应为_____ (填“Na+”或“H+”或“OH-”)离子交换膜,该电池的阳极反应式为_______。
(3)用Cu2O做催化剂,工业上在一定条件一下,可以用一氧化碳与氢气反应合成甲醇:
CO(g)+2H2(g)  CH3OH(g)
CH3OH(g)
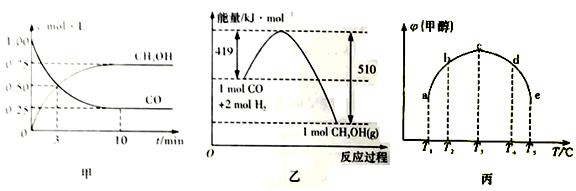
①甲图是反反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=_________。
②乙图表示该反应进行过程中能量的变化。请在乙图中画出用Cu2O作催化剂时“反应过程——能量”示意图_________。
③温度升高,该反应的平衡常数K_____(填“增大”、“不变”或“减小”)。
④ 某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则该反应在该温度下的平衡常数为_____(保留一位有效数字)。相同温度下,若向上述2L密闭容器中加入4molCO、3molH2、1molCH3OH,反应开始时,v(正)____v(逆)(填“大于”、“小于”或“等于”)。
⑤ 在容积均为1L的a、b、c、d、e,5个密闭容器中都分别充入1molCO和2molH2的混合气体,控温。图丙表示5个密闭容器温度分别为T1~T5、反应均进行到5min时甲醇的体积分数,要使容器c中的甲醇体积分数减少,可采取的措施有___________。
⑥ 据研究,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是_______(用化学方程式表示)。
-
请根据化学学科中的基本理论,回答下列问题
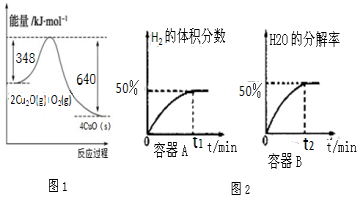
(1)纳米级的Cu2O可作为太阳光分解水的催化剂。火法还原CuO可制得Cu2O.已知:1克C(s)燃烧全部生成CO时放出热量9.2kJ;Cu2O(s)与O2(g)反应的能量变化如图1所示;请写出用足量炭粉还原CuO(s)制备Cu2O(s)的热化学方程式
(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O.该反应的化学方程式为______
(3)某兴趣小组同学以纳米级Cu2O催化光解水蒸气并探究外界条件对化学平衡的影响.
①在体积均为1L,温度分别为T1、T2的A、B两密闭容器中都加入纳米级Cu2O并通人0.1mol水蒸气,反应:2H2O(g)⇌2H2(g)+O2(g)△H=+484kJ•mol-1经测定A、B两容器在反应过程中发生如图2所示变化,则A、B两容器反应的温度T1________T2(填“<”、“=”或“>”),该过程中A容器至少需要吸收能量________kJ
②当该反应处于平衡状态时,下列既能增大反应速率,又能增大H2O(g)分解率的措施是(填序号)_________.
A.向平衡混合物中充入Ar B.升高反应的温度
C.增大反应体系的压强 D.向平衡混合物中充人O2
(4)25℃时,H2SO3═HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=_________mol/L.
-
纳米级Cu2O由于具有优良的催化性能而受到关注,下述为制取Cu2O的两种方法:
方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O  Cu2O+H2↑
Cu2O+H2↑
(1)已知:①2Cu(s) + O2 (g)=Cu2O(s) △H1= akJ/mol
②C(s)+ 
 O2 (g)=CO(g) △H2= bkJ/mol
O2 (g)=CO(g) △H2= bkJ/mol
③Cu(s)+ 
 O2 (g)= CuO(s) △H3= ckJ/mol
O2 (g)= CuO(s) △H3= ckJ/mol
则方法a中反应的热化学方程式是:_________________。
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O装置如图所示:
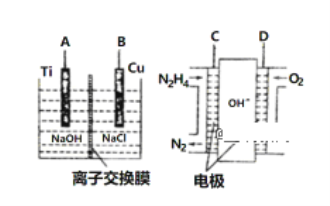
①如图装置中D电极应连______电极。(填“A”或“B”)
②该离子交换膜为______离子交换膜(填“阴”或“阳”),该电解池的B极反应式为: ____________________________________________。
③C极反应式为:____________________________。
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:2H2O 2H2(g)+O2(g) △H>0 ,水蒸气的浓度随时间t变化如表所示:
2H2(g)+O2(g) △H>0 ,水蒸气的浓度随时间t变化如表所示:
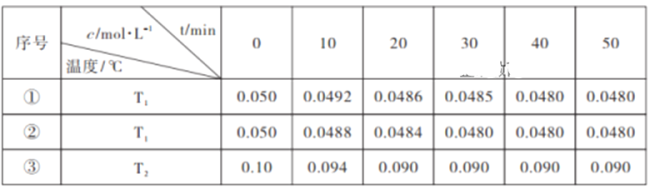
根据上述数据分析:
①催化剂的效率:实验①_______实验②(填“>”或“<”);
②通过实验①、③分析, T1______T2(填“>”或“<”);
③实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:_________。
-
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 电解法,反应为2Cu + H2O  Cu2O + H2↑。 Cu2O + H2↑。 |
| 方法c | 用肼(N2H4)还原新制Cu(OH)2 |
(1)已知:2Cu(s)+ O2(g)=Cu2O(s) △H =-169kJ·mol-1
O2(g)=Cu2O(s) △H =-169kJ·mol-1
C(s)+ O2(g)=CO(g) △H =-110.5kJ·mol-1
O2(g)=CO(g) △H =-110.5kJ·mol-1
Cu(s)+ O2(g)=CuO(s) △H =-157kJ·mol-1
O2(g)=CuO(s) △H =-157kJ·mol-1
则方法a发生反应的热化学方程式是_____________________________________。
(2)方法b采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该离子交换膜为______离子交换膜(填“阴”或“阳”),该电池的阳极反应式为______________________________________。
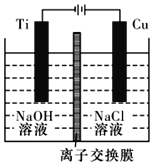
(3)方法c为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为________________________________________。
(4)在容积为1L的恒容密闭容器中,用以上方法制得的三种纳米级Cu2O分别进行催化分解水的实验:2H2O(g)  2H2(g)+O2(g),ΔH>0。水蒸气的浓度c随时间t 的变化如下表所示。
2H2(g)+O2(g),ΔH>0。水蒸气的浓度c随时间t 的变化如下表所示。
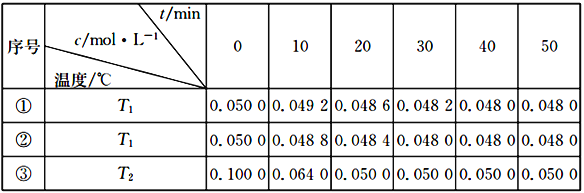
①对比实验的温度:T2_________T1(填“>”、“<”或“=”)
②催化剂催化效率:实验①________ 实验②(填“>”或“<”)
③在实验③达到平衡状态后,向该容器中通入水蒸气与氢气各0.1mol,则反应再次达到平衡时,容器中氧气的浓度为 ____________________。
-
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O Cu2O+H2↑
Cu2O+H2↑
(1)已知:①2Cu(s)+1/2O2(g)=Cu2O(s) △H=-169kJ/mol
②C(s)+1/2O2(g)=CO(g) △H=-110.5kJ/mol
③Cu(s)+1/2O2(g)=CuO(s) △H=-157kJ/mol
则方法a中反应的热化学方程式是:_________________。
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
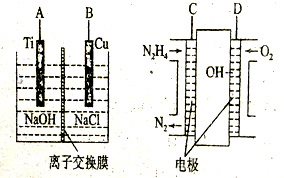
① 上述装置中B电极应连______电极(填“℃”或“D”)
② 该离子交换膜为_______离子交换膜(填“阴”或“阳”),该电解池的阳极反应式为:______。
③ 原电池中负极反应式为:_______________。
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:
2H2O 2H2(g)+O2(g) △H>0
2H2(g)+O2(g) △H>0
水蒸气的浓度随时间t变化如下表所示:
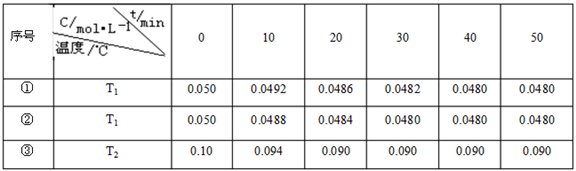
①催化剂的效率:实验①_______实验②(填“>”或“<”);
② 实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:_______。
O2(g)=CO(g)ΔH =–110.4kJ•mol-1,

HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如右图所示。







 △H>0,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示:
△H>0,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示:








 2H2(g)+O2(g) △H>0
2H2(g)+O2(g) △H>0