中国短道速滑队在索契冬奥会取得了骄人的成绩。速滑冰刀可用不锈钢制成,不锈钢含有的主要元素是

A. 铁 B. 碳 C. 铜 D. 铝
高二化学单选题简单题
中国短道速滑队在索契冬奥会取得了骄人的成绩。速滑冰刀可用不锈钢制成,不锈钢含有的主要元素是

A. 铁 B. 碳 C. 铜 D. 铝
高二化学单选题简单题
中国短道速滑队在索契冬奥会取得了骄人的成绩。速滑冰刀可用不锈钢制成,不锈钢含有的主要元素是

A. 铁 B. 碳 C. 铜 D. 铝
高二化学单选题简单题查看答案及解析
中国短道速滑队在索契冬奥会取得了骄人的成绩。速滑冰刀可用不锈钢制成,不锈钢含有的主要元素是

A.铁 B.碳 C.铜 D.铝
高二化学选择题简单题查看答案及解析
下列材料主要成分不属于有机高分子的是
A.断电保护器外壳工程塑料(PBT)
B.2022年冬奥会聚氨酯速滑服
C.滑雪板底座聚乙烯
D.“玉兔二号”钛合金筛网轮
高二化学单选题中等难度题查看答案及解析
I、钢铁中加入少量镍铬等元素可制成不锈钢,东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是______________________。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_________,提供孤电子对的成键原子是________。
(2)铁元素有变价,试根据原子核外电子排布所遵循的原理解释Fe2+具有较强的还原性,易被氧化为Fe3+的原因______________________________。
(3)普鲁士蓝(Prussian Blue),即亚铁氰化铁,化学式Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有____________________;
a.共价键 b.离子键 c.配位键 d.金属键 e.氢键
II、钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为2Mn2++5S2O82−+8H2O=2MnO4−+10SO42−+16H+
(4)写出基态锰原子的价电子排布的轨道表示式:________________。
(5)已知H2S2O8的结构如图:
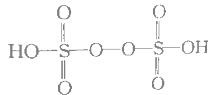
①H2S2O8硫原子的轨道杂化方式为________________。
②上述反应每生成2 mol MnO4−,S2O82−断裂的共价键数目为_________。
③上述反应中被还原的元素为________________。
高二化学综合题中等难度题查看答案及解析
下列说法错误的是 ( )
A.高纯度石英可用来制造光导纤维
B.棉花的主要成分是纤维素
C.原电池将电能转化为化学能
D.不锈钢是一种铁合金
高二化学单选题简单题查看答案及解析
2010年11月12日至27日,中国广州成功举办了第16届亚运会,中国代表团共获得了199枚金牌。为保证比赛成绩的公正、公平,反兴奋剂是一项重要而艰巨的工作。某种兴奋剂的结构简式如图所示。有关该物质的说法错误的是

A.该有机物能与FeCl3溶液发生显色反应
B.一定条件下1mol该物质能与7mol H2发生加成反应
C.该有机物分子中所有的原子不可能在同一平面
D.该有机物是苯酚的同系物
高二化学选择题中等难度题查看答案及解析
2010年11月12日至27日,中国广州成功举办了第16届亚运会,中国代表团共获得了199枚金牌.为保证比赛成绩的公正、公平,反兴奋剂是一项重要而艰巨的工作.某种兴奋剂的结构简式如图所示.有关该物质的说法错误的是( )
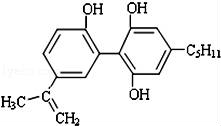
A.该有机物能与FeCl3溶液发生显色反应
B.一定条件下1mol该物质能与7molH2发生加成反应
C.该有机物分子中所有的原子不可能在同一平面
D.该有机物是苯酚的同系物
高二化学选择题简单题查看答案及解析
不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3以防止腐蚀。
(1)基态碳原子的电子排布图为___。
(2)铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为___。
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是___,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为____。
③氨是___分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___,氨的沸点高于PH3,原因是___。
(3)镍元素基态原子的价电子排布式为___,3d能级上的未成对电子数为___。
(4)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是___。
(5)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3,晶胞参数a=___nm。
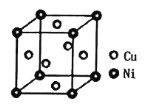
高二化学综合题简单题查看答案及解析

高二化学解答题中等难度题查看答案及解析
X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素。
(1)N元素在周期表中的位置是______,M的基态原子的价层电子排布图为_____。
(2)Y、D、E三种元素的电负性从大到小的排列顺序为________,第一电离能从大到小的排列顺序为_______。(均用元素符号表示)。
(3)由X、D两种元素按原子个数比为2:1组成的化合物,其中心原子的杂化方式为__________,该化合物属于___________分子(填“极性”或“非极性”)。
(4)金属镍粉在化合物YE气流中轻微加热,生成无色挥发性液态Ni(YE)4,呈四面体构型。423K时,Ni(YE)4分解为Ni和YE,从而制得高纯度的Ni粉。试推测:该液态物质易溶于下列______中(填字母)。
A.水 B.硫酸镍溶液 C.苯 D.四氯化碳
(5)某盐中含NE42-离子,是一种水处理剂,加入稀硫酸后快速生成黄色溶液并释放出一种无色无味的气体,请写出该反应的离子方程式___________________。
高二化学推断题困难题查看答案及解析