-
已知反应:H2(g)+ 1/2O2(g)=H2O(g)△H1
1/2N2(g)+O2(g)=NO2(g)△H2 1/2 N2(g)+ 3/2H2(g)=NH3(g)△H3
则反应2NH3(g)+ 7/2O2(g)=2NO2(g)+3H2O(g)的△H为
A. 2△H1+2△H2﹣2△H3 B. △H1+△H2﹣△H3
C. 3△H1+2△H2+2△H3 D. 3△H1+2△H2﹣2△H3
高三化学单选题中等难度题查看答案及解析
-
已知反应:H2(g) +
O2(g) = H2O(g) △H1
N2(g) + O2(g) = NO2 (g) △H2
N2(g) +
H2(g) = NH3 (g) △H3
则反应2NH3 (g) +
O2(g) =2NO2 (g) +3H2O(g) 的△H=
A.2△H1+2△H2—2△H3 B.△H1+△H2—△H3
C.3△H1+2△H2+2△H3 D.3△H1+2△H2—2△H3
高三化学选择题中等难度题查看答案及解析
-
已知反应:H2(g)+
O2(g)=H2O(g) ΔH1
N2(g)+O2(g)=NO2(g) ΔH2
N2(g)+3/2H2(g)=NH3(g) ΔH3
则反应2NH3(g)+
O2(g)=2NO2(g)+3H2O(g)的ΔH为( )
A. 2ΔH1+2ΔH2-2ΔH3 B. ΔH1+ΔH2-ΔH3
C. 3ΔH1+2ΔH2+2ΔH3 D. 3ΔH1+2ΔH2-2ΔH3
高三化学单选题中等难度题查看答案及解析
-
已知反应:H2(g)+
O2(g)=H2O(g) ΔH1
N2(g)+O2(g)=NO2(g) ΔH2
N2(g)+3/2H2(g)=NH3(g) ΔH3
则反应2NH3(g)+
O2(g)=2NO2(g)+3H2O(g)的ΔH为( )
A. 2ΔH1+2ΔH2-2ΔH3 B. ΔH1+ΔH2-ΔH3
C. 3ΔH1+2ΔH2+2ΔH3 D. 3ΔH1+2ΔH2-2ΔH3
高三化学单选题中等难度题查看答案及解析
-
(1)一定温度下,在恒容密闭容器中NO2与O2反应如下:4NO2(g)+O2(g)⇌2N2O5(g);若已知K350℃<K300℃,则该反应是______反应(填“吸热”或“放热”).反应达平衡后,若再通入一定量NO2,则平衡常数K将______,NO2的转化率______(填“增大”、“减小”或“不变”)
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据:
①写出该反应的平衡常数表达式:K=______.t/s 500 1000 c(N2O5)/mol•L-1 5.00 3.52 2.48
②1000s内N2O5的分解速率为______.
③若每有1molN2O5分解,放出或吸收QkJ的热量,写出该分解反应的热化学方程式______.高三化学解答题中等难度题查看答案及解析
-
(1)一定温度下,在恒容密闭容器中NO2与O2反应如下:4NO2(g)+O2(g)⇌2N2O5(g);若已知K350℃<K300℃,则该反应是______反应(填“吸热”或“放热”).反应达平衡后,若再通入一定量NO2,则平衡常数K将______,NO2的转化率______(填“增大”、“减小”或“不变”)
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据:
①写出该反应的平衡常数表达式:K=______.t/s 500 1000 c(N2O5)/mol•L-1 5.00 3.52 2.48
②1000s内N2O5的分解速率为______.
③若每有1molN2O5分解,放出或吸收QkJ的热量,写出该分解反应的热化学方程式______.高三化学解答题中等难度题查看答案及解析
-
下列说法正确的是
A.①2NO2
N2O4 ②N2O4
2NO2,反应①的化学平衡常数是反应②的化学平衡常数的倒数
B.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol,将0.05mol/LBa(OH)2溶液100.0mL与0.05mol/LH2SO4溶液100.0mL混合,在298K、101kPa条件下放热量为0.573kJ
C.已知298K 时,0.10mol/L HAc的电离度为1.32%。在0.10mol/L HAc和0.10mol/LNaAc的混合溶液20.00mL中,有如下变化:①HAc
H++Ac-,②NaAc=Na++Ac-,③Ac-+H2O
HAc+OH-,向该溶液中滴入几滴稀盐酸,溶液的pH保持相对稳定
D.将明矾与纯碱溶液混合,有沉淀产生,该沉淀的成分为碳酸铝
高三化学单选题中等难度题查看答案及解析
-
(10分)(1)一定温度下,在恒容密闭容器中NO2与O2反应如下:4NO2(g)+O2(g)
2N2O5(g);
若已知K350℃< K300℃,则该反应是_______反应(填“吸热”或“放热”)。
反应达平衡后,若再通入一定量NO2,则平衡常数K将______,NO2的转化率________(填“增大”、“减小”或“不变”)
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据:
t/s
0
500
1000
c(N2O5)/mol·L-1
5.00
3.52
2.48
① 写出该反应的平衡常数表达式:K=________。
②1000 s内N2O5的分解速率为________。
③若每有1molN2O5分解,放出或吸收QkJ的热量,写出该分解反应的热化学方程式________。
高三化学填空题中等难度题查看答案及解析
-
(10分)(1)一定温度下,在恒容密闭容器中NO2与O2反应如下:4NO2(g)+O2(g)
2N2O5(g);
若已知K350℃< K300℃,则该反应是_______反应(填“吸热”或“放热”)。
反应达平衡后,若再通入一定量NO2,则平衡常数K将______,NO2的转化率________(填“增大”、“减小”或“不变”)
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据:
t/s
0
500
1000
c(N2O5)/mol·L-1
5.00
3.52
2.48
① 写出该反应的平衡常数表达式:K=。
② 1000 s内N2O5的分解速率为。
③若每有1molN2O5分解,吸收QkJ的热量,写出该分解反应的热化学方程式________。
高三化学填空题中等难度题查看答案及解析
-
一定温度下,在2L密闭容器中NO2和O2可发生下列反应: 4NO2(g)+O2(g)
2N2O5(g)+5286 kJ已知体系中n(NO2)随时间变化如下表:
t(s)
0
500
1000
1500
n(NO2)(mol)
20
13.96
10.08
10.08
(1)能说明该反应已达到平衡状态的是________。
A.v(NO2)=4v(O2) B.容器内压强保持不变
C.v逆(N2O5)=2v正(O2) D.容器内密度保持不变
(2)反应达到平衡后,NO2的转化率为________,此 时若再通入一定量氮气,则NO2的转化率将________(填“增大”、“减小”、“不变”)。
(3)图中能表示N2O5的浓度变化的曲线是________,用O2表示从0~500s内该反应的平均速率v=________。
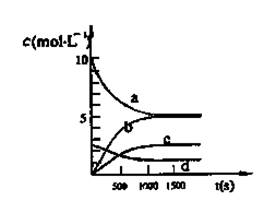
(4)能使该反应的反应速率增大,且平衡向正应方向移动的是________。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效催化剂
高三化学填空题困难题查看答案及解析