-
卤素原子之间可以形成类似卤素单质的分子,如溴化碘(IBr)能跟大多数金属反应生成金属卤化物,能跟水反应,其化学方程式为IBr+H2O=HBr+HIO。下面有关IBr的叙述中不正确的是( )
A. 在很多反应中IBr是强氧化剂
B. IBr与H2O反应时,其氧化产物是HBr,还原产物是HIO
C. IBr跟NaOH溶液反应生成NaBr、NaIO和H2O
D. IBr跟金属锌反应生成ZnBr2和ZnI2
高三化学单选题中等难度题查看答案及解析
-
卤素原子之间可以形成类似卤素单质的分子,如溴化碘(IBr)能跟大多数金属反应生成金属卤代物,能跟水反应其化学方程式为:IBr+H2O═HBr+HIO.下面有关IBr的叙述中不正确的是( )
A.在很多反应中IBr是强氧化剂
B.IBr与H2O反应时,其氧化产物是HBr,还原产物是HIO
C.IBr跟NaOH溶液反应生成NaBr、NaIO和H2O
D.IBr跟金属锌反应生成ZnBr2和ZnI2高三化学选择题中等难度题查看答案及解析
-
溴化碘(IBr)的化学性质与卤素单质相似,能跟大多数金属反应生成金属卤化物,能跟水反应IBr+H2O==HBr+HIO.下列有关叙述中不正确的是 ( )
A.IBr是双原子分子
B.IBr与水反应时,它既是氧化剂,又是还原剂
C.在很多化学反应中IBr作氧化剂
D.跟NaOH溶液反应可生成NaBr和NaIO
高三化学选择题简单题查看答案及解析
-
溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式为IBr+H2O==HBr+HIO。下列有关IBr的叙述中,不正确的是
A. IBr的电子式:
B. IBr和Zn的反应化学方程式2IBr+2Zn==ZnI2 +ZnBr2
C. IBr和NaOH溶液反应生成NaBr 和NaIO
D. IBr和水反应时,既是氧化剂又是还原剂
高三化学单选题中等难度题查看答案及解析
-
溴化碘
的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式为IBr+H2O=HBr+HIO。下列有关IBr的叙述中,不正确的是( )
A.IBr是双原子分子
B.在很多反应中,IBr是强氧化剂
C.IBr和NaOH溶液反应生成NaBr和NaIO
D.IBr和水反应时,既是氧化剂又是还原剂
高三化学单选题中等难度题查看答案及解析
-
阅读下列短文:不同的卤素之间可以相互结合形成一系列的化合物。这类化合物称为卤素互化物。卤素互化物具有很高的化学活性,它们有许多化学性质跟卤素单质相似,例如:能跟大多数金属起反应生成相应的卤化物,也能跟某些非金属单质起反应生成相应的卤化物。溴化碘(IBr)是卤素互化物的一种。这种化合物在常温下是深红色的固体,熔点为41℃,沸点为116℃。下列对IBr的各种描述中,不正确的是
A.在很多化学反应中,溴化碘是一种氧化剂
B.固体溴化碘是一种原子晶体
C.与水能反应:IBr + H2O=HBr+ HIO
D.在Fe3+的催化下可与苯反应生成
和HBr
高三化学选择题中等难度题查看答案及解析
-
溴化碘(IBr)的化学性质类似于卤素单质,试回答下列问题:
(1)溴化碘的电子式是________,它是由________键形成的________分子。
(2)溴化碘和水反应生成了一种三原子分子,该分子的电子式为________。
高三化学填空题中等难度题查看答案及解析
-
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为__。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为__。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于__。
(4)互为等电子体的微粒相互之间结构相似。I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为___,中心原子杂化类型为__。
(5)铁在元素周期表中的位置___(用“周期”和“族”来描述)。
(6)简述三价铁比二价铁稳定的原因___。
(7)如图所示为卤化物冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子__、__;大立方体的体心处▽所代表的是__。
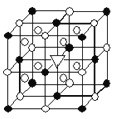
高三化学综合题中等难度题查看答案及解析
-
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为________。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为________。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于________。
(4)互为等电子体的微粒相互之间结构相似。I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为________,中心原子杂化类型为________。
(5)①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]的酸性由强到弱的顺序为________(填序号)。
(6)卤化物RbICl2在加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式________。
(7)如图所示为卤化物冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子________、________;大立方体的体心处▽所代表的是________。
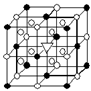
高三化学填空题困难题查看答案及解析
-
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为_______________。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为_____________。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于___________________________。
(4)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为_____________________,中心原子杂化类型为________________。
(5)①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]的酸性由强到弱的顺序为____________(填序号)。
(6)卤化物RbICl2在加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为______________________。
高三化学填空题简单题查看答案及解析