已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )

A. 反应I2(aq)+I-(aq)I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
高一化学单选题中等难度题
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )

A. 反应I2(aq)+I-(aq)I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
高一化学单选题中等难度题
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )

A. 反应I2(aq)+I-(aq)I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
高一化学单选题中等难度题查看答案及解析
在碘水中加入KI发生如下反应:I2(aq)+I−(aq)I3-(aq)(aq表示水溶液)。某I2、KI混合溶液中,c(I3-)在不同温度下的平衡平衡浓度与温度T的关系如图曲线所示。下列说法不正确的是
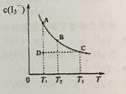
A.反应I2(aq)+I−(aq) I3-(aq) 是放热反应
B.压强变化对该平衡影响不大
C.状态D时,v正<v逆
D.状态A与状态B相比,状态A的c(I2) 小
高一化学单选题简单题查看答案及解析
I2在KI溶液中存在平衡:I2(aq)+I-(aq)I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的平衡曲线图如图。下列说法不正确的是
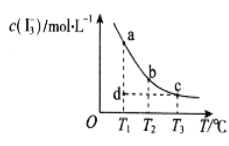
A.反应I2(aq)+I-(aq)I3-(aq)的△H>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
C.若反应进行到状态d时,一定有正>
逆
D.状态a与状态b相比,状态a的c(I2)小
高一化学单选题简单题查看答案及解析
在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3- (aq)。某I2、KI混合溶液中I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是

A. 反应I2(aq)+I-(aq) I3- (aq)的ΔH>0
B. 若温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2
C. 若反应进行到状态D时,一定有v(正) > v(逆)
D. 状态A与状态B相比,状态A的c(I2)大
高一化学单选题中等难度题查看答案及解析
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq) I3- (aq)。上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。下列说法不正确的是
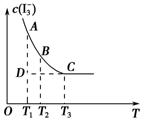
A.该反应的正反应是吸热反应
B.A点与C点的化学反应速率vA<vC
C.反应进行到D点时,v(正)>v(逆)
D.A点与B点相比,B点的c(I-)大
高一化学选择题简单题查看答案及解析
对平衡CO2(g)CO2(aq) △H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
A. 升温增压 B. 降温减压
C. 升温减压 D. 降温增压
高一化学单选题简单题查看答案及解析
碘化钠在光学器件石油探测、安检、环境监测等领域有重要应用。某研究小组开发设计的制备高纯NaI的简化流程如图:
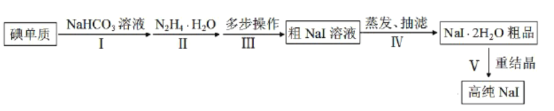
已知:
①I2(s)+I-(aq)I3-(aq)。
②水合肼(N2H4•H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO3-离子。
①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为___。
②实验过程中,加少量NaI固体能使反应速率加快,其原因是___。
(2)步骤Ⅱ,水合肼与IO‾反应的离子方程式为___。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。上述①②③操作中,调整pH值时依次加入的试剂为___。
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有___。
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为___。
(5)将制备的NaI•2H2O粗品以无水乙醇为溶剂进行重结晶。请给出合理的操作排序___。
加热乙醇→ → → → →纯品(选填序号)。
①高纯水洗涤 ②减压蒸发结晶 ③NaI•2H2O粗品溶解 ④趁热过滤 ⑤真空干燥 ⑥抽滤
高一化学实验题困难题查看答案及解析
将FeCl3溶液和KI溶液混合,发生反应:2Fe3+(aq)+2I-(aq)2Fe2+(aq)+I2(aq)。下列各项能判断上述可逆反应达到平衡状态的是
A. 溶液颜色不再变化
B. c(K+)不再变化
C. c(Fe3+)与c(Fe2+)之和不再变化
D. v正(I-)=2v正(I2)
高一化学单选题中等难度题查看答案及解析
下列关于电解质的叙述中,正确的是
①硫酸银在水中的溶解度很小,其溶液的导电能力很弱,所以硫酸银是弱电解质
②碳酸钙在水中的溶解度虽小,但溶解的部分全部电离,所以碳酸钙是强电解质
③氨气的水溶液导电性很好,所以它是强电解质
④水难电离,纯水几乎不导电,所以水是弱电解质
A.② B.① C.①③ D.②④
高一化学选择题简单题查看答案及解析
一定温度下,在氢氧化钙的悬浊液中,存在如下的溶解平衡关系:Ca(OH)2 (s) Ca2+(aq)+2OH-(aq)。向此悬浊液中加入少量的氧化钙粉末,下列叙述正确的是
A.溶液中Ca2+数减小 B.溶液中c(Ca2+)减小
C.溶液中c(OH-)增大 D.pH减小
高一化学选择题中等难度题查看答案及解析