在碘水中加入KI发生如下反应:I2(aq)+I−(aq)I3-(aq)(aq表示水溶液)。某I2、KI混合溶液中,c(I3-)在不同温度下的平衡平衡浓度与温度T的关系如图曲线所示。下列说法不正确的是
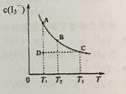
A.反应I2(aq)+I−(aq) I3-(aq) 是放热反应
B.压强变化对该平衡影响不大
C.状态D时,v正<v逆
D.状态A与状态B相比,状态A的c(I2) 小
高一化学单选题简单题
在碘水中加入KI发生如下反应:I2(aq)+I−(aq)I3-(aq)(aq表示水溶液)。某I2、KI混合溶液中,c(I3-)在不同温度下的平衡平衡浓度与温度T的关系如图曲线所示。下列说法不正确的是

A.反应I2(aq)+I−(aq) I3-(aq) 是放热反应
B.压强变化对该平衡影响不大
C.状态D时,v正<v逆
D.状态A与状态B相比,状态A的c(I2) 小
高一化学单选题简单题
在碘水中加入KI发生如下反应:I2(aq)+I−(aq)I3-(aq)(aq表示水溶液)。某I2、KI混合溶液中,c(I3-)在不同温度下的平衡平衡浓度与温度T的关系如图曲线所示。下列说法不正确的是

A.反应I2(aq)+I−(aq) I3-(aq) 是放热反应
B.压强变化对该平衡影响不大
C.状态D时,v正<v逆
D.状态A与状态B相比,状态A的c(I2) 小
高一化学单选题简单题查看答案及解析
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )

A. 反应I2(aq)+I-(aq)I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
高一化学单选题中等难度题查看答案及解析
I2在KI溶液中存在平衡:I2(aq)+I-(aq)I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的平衡曲线图如图。下列说法不正确的是
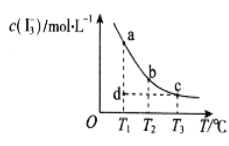
A.反应I2(aq)+I-(aq)I3-(aq)的△H>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
C.若反应进行到状态d时,一定有正>
逆
D.状态a与状态b相比,状态a的c(I2)小
高一化学单选题简单题查看答案及解析
在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3- (aq)。某I2、KI混合溶液中I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是

A. 反应I2(aq)+I-(aq) I3- (aq)的ΔH>0
B. 若温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2
C. 若反应进行到状态D时,一定有v(正) > v(逆)
D. 状态A与状态B相比,状态A的c(I2)大
高一化学单选题中等难度题查看答案及解析
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq) I3- (aq)。上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。下列说法不正确的是
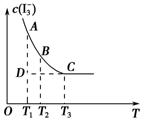
A.该反应的正反应是吸热反应
B.A点与C点的化学反应速率vA<vC
C.反应进行到D点时,v(正)>v(逆)
D.A点与B点相比,B点的c(I-)大
高一化学选择题简单题查看答案及解析
将FeCl3溶液和KI溶液混合,发生反应:2Fe3+(aq)+2I-(aq)2Fe2+(aq)+I2(aq)。下列各项能判断上述可逆反应达到平衡状态的是
A. 溶液颜色不再变化
B. c(K+)不再变化
C. c(Fe3+)与c(Fe2+)之和不再变化
D. v正(I-)=2v正(I2)
高一化学单选题中等难度题查看答案及解析
已知:将KI.盐酸.试剂X和淀粉四种溶液混合,无反应发生。若再加入双氧水,将发生反应:H2O2+2H++2I—→2H2O+I2,且生成的I2立即与试剂X反应而被消耗。一段时间后,试剂X将被反应生成的I2完全消耗。由于溶液中的I—继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝。因此,根据试剂X的量.滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I—→2H2O+I2的反应速率。
下表为某同学依据上述原理设计的实验及实验记录(各实验均在室温条件下进行):
| 编 号 | 往烧杯中加入的试剂及其用量(mL) | 催化剂 | 溶液开始变蓝时间(min) | ||||
|
| H2O | X 溶液 |
|
| |||
| 1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 无 | 1.4 |
| 2 | 20.0 | m | 10.0 | 10.0 | n | 无 | 2.8 |
| 3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 无 | 2.8 |
| 4 | 20.0 | 0 | 10.0 | 10.0 | 40.0 | 无 | t |
| 5 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
回答下列问题:
(1)已知:实验1、2的目的是探究H2O2浓度对H2O2+2H++2I—→2H2O+I2反应速率的影响。实验2中m= ,n=
(2)一定温度下,H2O2+2H++2I—→2H2O+I2反应速率可以表示为v=k·c a(H2O2)·c b (I—)·c(H+)(k为常数),则:
①实验4时,烧杯中溶液开始变蓝的时间t=___________。
②根据上表数据可知,a、b的值依次为 和 。
(3)实验5表明:硫酸铁能提高反应速率。
①催化剂能加快反应速率是因为催化剂 (填“提高”或“降低”)了反应活化能。
②试用离子方程式表示Fe2(SO4)3对H2O2+2H++2I—→2H2O+I2催化的过程。
. (不必配平)
高一化学填空题简单题查看答案及解析
水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:O2MnO(OH)2
I2
S4O62-
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:_______________________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水样的溶解氧,消耗0.010 00 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L-1表示),写出计算过程_____。
高一化学计算题中等难度题查看答案及解析
下列表示对应化学反应的离子方程式正确的是
A. 碘水中通入适量的 SO2:I2+SO2+H2O=2I-+SO42-+4H+
B. 0.5mol/LNaHSO4 与 0.5mol/LBa(OH)2 混合溶液呈中性: Ba2++OH-+SO42-+H+=BaSO4 ↓+H2O
C. NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++2OH-+2HCO3=CaCO3↓+CO32-+2H2O
D. 向NaAlO2溶液中通入过量CO2: AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
高一化学单选题困难题查看答案及解析
某固体混合物可能含有、
、
、
和
中的一种或几种,将该混合物进行如下实验:
①将少许混合物放入水中得到无色溶液和白色沉淀,过滤;
②取溶液进行焰色反应,火焰呈黄色;
③取白色沉淀加入稀盐酸,沉淀完全溶解并放出气体
由上述现象推断:
(1)该混合物中一定含有________,一定不含有________,可能含有________。
(2)若要检验可能含有的物质是否存在,可以采用的实验操作为_____(填写字母)。
A.取步骤①中滤液,加入溶液
B.取步骤①中滤液,加入NaOH溶液
C.取步骤①中滤液,加入足量溶液,静置后在上层清液中加入硝酸酸化
溶液
D.取步骤①中滤液,加入足量溶液,静置后上层清液中加入硝酸酸化
溶液
高一化学推断题中等难度题查看答案及解析