氢化铝钠(NaAlH4)是最冇研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4Na3AlH6+2Al+3H2↑。下列说法正确的是
A. NaAlH4中氢元素为+1价
B. 每生成11. 2 L(标准状况下)H2,转移2NA个电子
C. 在反应中有50%的氢被氧化
D. 反应中氧化产物与还原产物的物质的量之比为1: 1
高三化学单选题中等难度题
氢化铝钠(NaAlH4)是最冇研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4Na3AlH6+2Al+3H2↑。下列说法正确的是
A. NaAlH4中氢元素为+1价
B. 每生成11. 2 L(标准状况下)H2,转移2NA个电子
C. 在反应中有50%的氢被氧化
D. 反应中氧化产物与还原产物的物质的量之比为1: 1
高三化学单选题中等难度题
氢化铝钠(NaAlH4)是最冇研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4Na3AlH6+2Al+3H2↑。下列说法正确的是
A. NaAlH4中氢元素为+1价
B. 每生成11. 2 L(标准状况下)H2,转移2NA个电子
C. 在反应中有50%的氢被氧化
D. 反应中氧化产物与还原产物的物质的量之比为1: 1
高三化学单选题中等难度题查看答案及解析
氢化铝钠(NaAlH4)是最冇研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4Na3AlH6+2Al+3H2↑。下列说法正确的是
A. NaAlH4中氢元素为+1价
B.每生成11. 2 L(标准状况下)H2,转移2NA个电子
C. 在反应中有50%的氢被氧化
D.反应中氧化产物与还原产物的物质的量之比为1: 1
高三化学选择题中等难度题查看答案及解析
氢化铝钠(NaAlH4)是最有研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4Na3AlH6+2Al+3H2↑。下列说法正确的是
A.NaAlH4中含有离子键和非极性共价键
B.每生成11. 2 L(标准状况下)H2,转移NA个电子
C.NaAlH4中氢元素为+1价,在反应中有50%的氢被还原
D.反应中氧化产物与还原产物的物质的量之比为1:1
高三化学选择题中等难度题查看答案及解析
复合氢化物可作为储氢和固体电解质材料,在能源与材料领域得到了深入的研究。
如:①Mg(NH2)2 ②NaNH2 ③ H3N-BH3 ④NaAlH4 ⑤Li3AlH6
(1)复合氢化物升温加热可逐步分解放出氢气,理论上单位质量的上述复合氢化物其储氢能力最低的是__________(填标号)。
(2)在Mg(NH2)2和NaNH2中均存在NH2-,NH2-的空间构型为_________,中心原子的杂化方式为____________。
(3)H3N-BH3与水反应生成一种盐和H2的化学方程式:_____________________。写出基态B原子的价电子轨道表达式:__________________________。
(4)Li3AlH6晶体的晶胞参数为a=b=801.7 pm,c=945.5 pm,α=β=90°、γ=120°,结构如图所示:
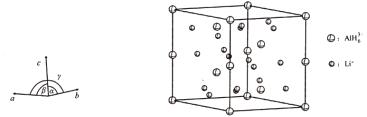
①已知AlH63-的分数坐标为(0,0,0)、(0,0,),(
,
,
),(
,
,
),(
,
,
)和(
,
,
),晶胞中Li+的个数为____________。
②如图是上述Li3AlH6晶胞的某个截面,共含有10个AlH63-,其中6个已经画出(图中的○),请在图中用○将剩余的AlH63-画出____________。

③此晶体的密度为____g·cm-3(列出计算式,已知阿伏加德罗常数约为6.02×1023mol-1)。
高三化学综合题中等难度题查看答案及解析
铝氢化钠(NaAlH4)是有机合成的重要还原剂。某课题组经查阅资料后设计合成铝氢化钠的简易流程如图所示。

已知:①AlCl3、NaH、NaAlH4遇水都能迅速发生反应。
②常温下,可用高锰酸钾、氯酸钾、重铬酸钾、次氯酸钙等与浓盐酸反应制取氯气。
(1)铝氢化钠遇水发生剧烈反应,甚至可能发生爆炸,其原因是_______________。写出铝氢化钠与水反应的化学方程式_____________________。
(2)甲同学设计实验制备无水氯化铝的装置如图所示。
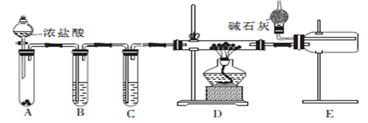
①装置E中干燥管的作用是_______________________。
②点燃装置D处酒精灯之前 需先排尽装置内的空气,其操作方法是________________。
(3)乙同学分析甲同学设计的装置后,认为只改变A、B、D中的试剂就可以用甲同学设计的装置制备NaH。
①试管B中的试剂改为____________________。
②若操作不当,则制得的NaH产品中可能含有的杂质有_________________。
(4)丙同学设计以下4种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。
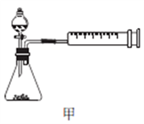
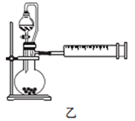
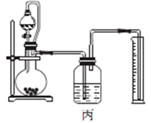
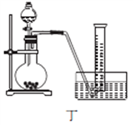
从易操作性、准确性角度考虑,宜选装置________。铝氢化钠与水完全反应,冷却至室温的标志是______。
高三化学实验题困难题查看答案及解析
铝氢化钠(NaAlH4)是有机合成的重要还原剂。某课题组经查阅资料后设计合成铝氢化钠的流程如图所示。

已知:①AlCl3、NaH、NaAlH4遇水都能迅速发生反应。
②常温下,可用高锰酸钾、氯酸钾、重铬酸钾、次氯酸钙等与浓盐酸反应制取氯气。
(1)铝氢化钠遇水发生剧烈反应,甚至可能发生爆炸,其原因是_______
写出铝氢化钠与水反应的化学方程式 _________
(2)甲同学设计实验制备无水氯化铝的装置如图所示。
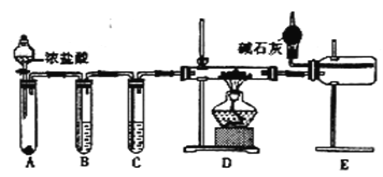
①装置E中干燥管的作用是_______________________。
②点燃装置D处酒精灯之前 需先排尽装置内的空气,其操作方法是 ______。
(3)乙同学分析甲同学设计的装置后,认为只改变A、B、D中的试剂就可以用甲同学设计的装置制备NaH。
①试管B中的试剂改为____________________。
②若操作不当,则制得的NaH产品中可能含有的杂质有_______。
(4)丙同学设计以下3种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。
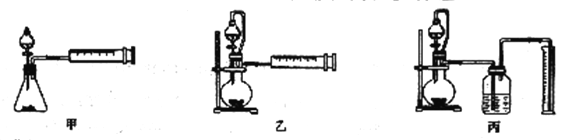
从易操作性、准确性角度考虑宜选装置___。如何判断铝氢化钠与水完全反应:___
高三化学简答题中等难度题查看答案及解析
铝氢化钠(NaAlH4)是有机合成的重要还原剂。某课题组经查阅资料后设计合成铝氢化钠的简易流程如图所示。

已知:①AlCl3、NaH、NaAlH4遇水都能迅速发生反应。
②常温下,可用高锰酸钾、氯酸钾、重铬酸钾、次氯酸钙等与浓盐酸反应制取氯气。
(1)铝氢化钠遇水发生剧烈反应,甚至可能发生爆炸,其原因是_______________。写出铝氢化钠与水反应的化学方程式_____________________。
(2)甲同学设计实验制备无水氯化铝的装置如图所示。
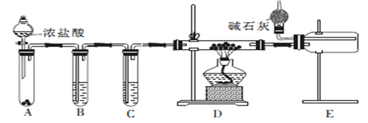
①装置E中干燥管的作用是_______________________。
②点燃装置D处酒精灯之前 需先排尽装置内的空气,其操作方法是________________。
(3)乙同学分析甲同学设计的装置后,认为只改变A、B、D中的试剂就可以用甲同学设计的装置制备NaH。
①试管B中的试剂改为____________________。
②若操作不当,则制得的NaH产品中可能含有的杂质有_________________。
(4)丙同学设计以下4种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。
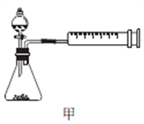
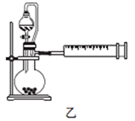
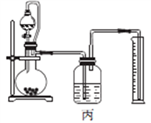
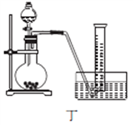
从易操作性、准确性角度考虑,宜选装置________。铝氢化钠与水完全反应,冷却至室温的标志是______。
高三化学实验题困难题查看答案及解析
铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成线路如下图所示。

(1)铝氢化钠遇水发生剧烈反应,其反应的化学方程式为_____________________。
(2)AlCl3与NaH反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因是__________________。
(3)实验室利用下图装置制取无水AlCl3。
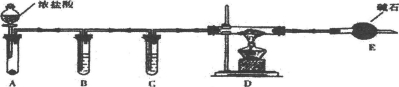
①A中所盛装的试剂是_______________。
②点燃D处酒精灯之前需排除装置中的空气,其操作是______________________。
(4)改变A和D中的试剂就可以用该装置制取NaH,若装置中残留有氧气,制得的NaH中可能含有的杂质为____________
(5)现设计如下四种装置,测定铝氢化钠粗产品(只含有NaH杂质)的纯度。
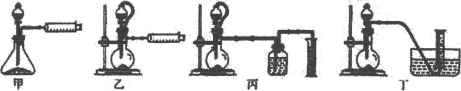
从简约性、准确性考虑,最适宜的装置是_________(填编号)。称取15.6g样品与水完全反应后,测得气体在标准状况下的体积为22.4L,样品中铝氢化钠的质量分数为___________。(结果保留两位有效数字)
高三化学实验题困难题查看答案及解析
铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成线路如下图所示。
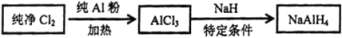
(1)铝氢化钠遇水发生剧烈反应,其反应的化学方程式为__________________________。
(2)AlCl3与NaH反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因是__________________________________________。
(3)实验室利用下图装置制取无水AlCl3。
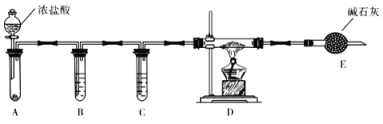
①A中所盛装的试剂是_______________。
②点燃D处酒精灯之前需排除装置中的空气,其操作是____________________________
(4)改变A和D中的试剂就可以用该装置制取NaH,若装置中残留有氧气,制得的NaH中可能含有的杂质为____________ 。
(5)现设计如下四种装置,测定铝氢化钠粗产品(只含有NaH杂质)的纯度。
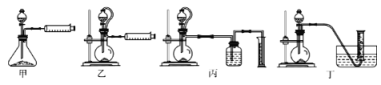
从简约性、准确性考虑,最适宜的装置是_________(填编号)。称取15.6g样品与水完全反应后,测得气体在标准状况下的体积为22.4L,样品中铝氢化钠的质量为___________。
高三化学实验题困难题查看答案及解析
H、N、Na、Al、Ti等元素在能源、材料等领域应用广泛。回答下列问题:
(一)氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢。NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如图所示,为长方体。
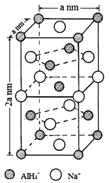
(1)基态Ti原子的价电子排布图为_________, L能层中电子云的形状有_______种。
(2)AlCl3在178℃时升华,属于__________晶体,其蒸气的相对分子质量约为267,蒸气分子的结构式为___________(标明配位键),其中 Al的轨道杂化方式为____________。
(3)写出与AlH4-空间构型相同的一种分子和一种离子_________(填化学式)。
(4)NaAlH4晶体中,与AlH4-紧邻且等距的Na+有__________个;NaAlH4晶体的密度为_____________g·cm-3(用含a的代数式表示)。
(二)叠氮化钠和氢叠氮酸(HN3)已一步步进入我们的生活,如汽车安全气囊等。
(1)写出与N3-属于等电子体的一种分子__________(填分子式)。
(2)氢叠氮酸(HN3)可由肼(N2H4)被HNO2氧化制得,同时生成水。下列叙述错误的是___(填标号)
A.上述生成HN3的化学方程式为:N2H4+HNO2= HN3+2 H2O
B.NaN3的晶格能大于KN3的晶格能
C.氢叠氮酸(HN3)和水能形成分子间氢键
D.HN3和N2H4都是由极性键和非极性键构成的非极性分子。
E.HN3分子中四个原子可能在一条直线上
高三化学综合题困难题查看答案及解析