-
下列各项叙述正确的是
①水玻璃、碱石灰、漂白粉、福尔马林、淀粉均为混合物
②进行中和热的测定实验时,必须用到两个量筒和两个温度计
③已知酸性强弱:HCl>H2S,由此可以推断出非金属性相对强弱:Cl>S
④有单质参加的反应或有单质生成的反应一定是氧化还原反应
⑤ 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
⑥工业上制漂白粉,所得的氯化物都具有漂白性
⑦Ca(HCO3)2、Fe(OH)3 可由化合反应制得,Fe3O4 可由置换反应制得
A. ①⑤⑦ B. ①③⑤ C. ②③⑤⑦ D. ①②④⑥
高三化学单选题中等难度题查看答案及解析
-
下列各项叙述正确的是
①水玻璃、碱石灰、漂白粉、福尔马林、淀粉均为混合物
②进行中和热的测定实验时,必须用到两个量筒和两个温度计
③由不同种原子间形成的共价键一定是极性共价键
④有单质参加的反应或有单质产生的反应一定是氧化还原反应
⑤碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
⑥蒸馏在天然香料,药物提取及核燃料处理等技术中得到了广泛的应用
⑦Ca(HCO3)2、Fe(OH)3可由化合反应制得,Fe3O4可以由置换反应制得
A. ①③⑤ B. ①⑤⑦ C. ②③⑤⑦ D. ①②④⑥
高三化学单选题中等难度题查看答案及解析
-
下列有关说法正确的是
A. 陶瓷、水晶、水泥、玻璃都属于硅酸盐产品
B. 糖类、油脂、蛋白质都能发生水解反应
C. 进行中和热的测定实验时,必须用到两个量筒和两个温度计
D. “血液透析”利用了胶体的渗析原理
高三化学单选题简单题查看答案及解析
-
下列关于实验仪器和用品的选择,不正确的是
A.实验室制备乙烯时加入碎瓷片,可以防止暴沸
B.用KMnO4滴定H2C2O4时需要用到两支酸式滴定管
C.进行中和热的测定实验时,必须用到两个量筒和两个温度计
D.实验室测定化学反应速率时,需要用到仪器秒表
高三化学选择题简单题查看答案及解析
-
在实验室进行下列实验,括号内的实验仪器或试剂都能用到的是
A.中和热的测定(量筒、温度计、酒精灯)
B.从溴水中提取溴单质(分液漏斗、无水乙醇、玻璃棒)
C.探究浓硫酸与铜反应的产物(蘸有碳酸钠溶液的棉花团、蒸馏水、烧杯)
D.制氢氧化铁胶体(饱和FeCl3溶液、NaOH溶液、胶头滴管)
高三化学选择题中等难度题查看答案及解析
-
(14分)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
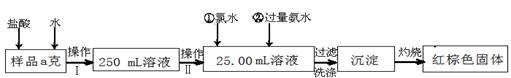
请根据上面流程,回答以下问题:
(1)操作 I 所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有________(填自选仪器名称),操作 II 必须用到的仪器是________ (从以下选项中选择,填编号)。
A.50mL烧杯 B.50mL量筒 C.25mL碱式滴定管 D.25mL酸式滴定管
(2)加入试剂①和②后发生反应的离子反应方程式为:________
(3) 将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3 g,则接下来还应进行的操作是____________。
(4) 若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:________。
(5) 有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是:
________ (用化学方程式表示)
高三化学实验题中等难度题查看答案及解析
-
某氯化铁样品含有少量FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
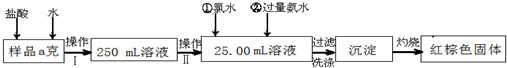
请根据上面流程,回答以下问题:
(1)操作 I 所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有______(填自选仪器名称),操作 II 必须用到的仪器是______ (从以下选项中选择,填编号).
A.50mL烧杯 B.50mL量筒 C.25mL碱式滴定管 D.25mL酸式滴定管
(2)加入试剂①和②后发生反应的离子反应方程式为:______
(3)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是______.
(4)若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:______.
(5)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的.他的理由是:
______ (用化学方程式表示)高三化学解答题中等难度题查看答案及解析
-
(15分)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
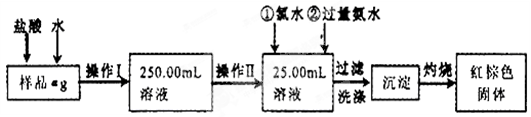
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯.玻璃棒.量筒外,还必须有____________ (填仪器名称),操作II必须用到的仪器是____________(填编号)。
A.50mL烧杯 B.50mL量筒
C.25mL碱式滴定管 D.25mL酸式滴定管
(2)洗涤是洗去附着在沉淀上的____________。(写离子符号)
(3)检验沉淀是否已经洗涤干净的操作是________________________。
(4)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是_________。
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是__________。
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是____________。(用化学方程式表示)
高三化学实验题中等难度题查看答案及解析
-
(15分)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
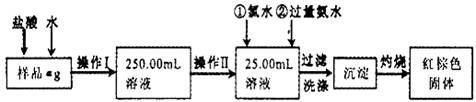
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯.玻璃棒.量筒外,还必须有____________ (填仪器名称),操作II必须用到的仪器是____________(填编号)。
A.50mL烧杯 B.50mL量筒
C.25mL碱式滴定管 D.25mL酸式滴定管
(2)洗涤是洗去附着在沉淀上的____________。(写离子符号)
(3)检验沉淀是否已经洗涤干净的操作是________________________。
(4)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是_________。
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是____________。
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是________________________。(用化学方程式表示)
高三化学填空题中等难度题查看答案及解析
-
在测定中和热的实验中,下列说法中正确的是 ( )
A.该实验需要用的主要玻璃仪器有:两个大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒
B.不能用保温杯代替烧杯做有关测定中和热的实验
C.该实验至少需要测定并记录温度的次数是6次
D.若NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高
高三化学选择题简单题查看答案及解析