-
KIO3是一种无色易溶于水的晶体,医药上可作防治地方甲状腺肿的药剂,目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:
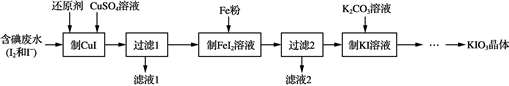
(1) 检验“含碘废水”中含有的单质I2,常用的试剂是________。
(2) 进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加________盐溶液来检验其是否已洗涤干净。
(3) “滤渣2”的成分为____________(填化学式)。
(4) “制KI”时,发生反应的化学方程式为____________。
(5) 江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33 mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000 g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00 mL 6.000×10-4 mol·L-1 Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O; I2+2S2O ===2I-+S4O
===2I-+S4O 。
。
①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)。
_______
②该食盐试样是否符合江苏食用加碘盐新标准并说明判断依据。
_______
-
KIO3是一种无色易溶于水的晶体,医药上可作防治地方甲状腺肿的药剂,目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:

(1)检验“含碘废水”中含有的单质I2,常用的试剂是______。
(2)进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤过滤滤液中可通过滴加______盐溶液来检验其是否已洗涤干净。
(3)“滤渣2”的成分为______(填化学式)。
(4)“制KI”时,发生反应的化学方程式为______。
(5)江苏食用加碘盐新标准是每千克食盐中碘元素含量为25毫克(波动范围为18~33mg/kg)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL6.000×10-4mol·L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O32—=2I- +S4O62—。
①计算该食盐试样中碘元素的含量(单位mg/kg,写出计算过程)_____。
②该食盐试样是否符合江苏食用加碘盐新标准,并说明判断依据______。
-
α-呋喃基丙烯酸广泛应用于医药、化妆品及香料,某兴趣小组尝试试用α-呋喃甲醛和醋酸酐合成α-呋喃基丙烯酸。反应原理如下:
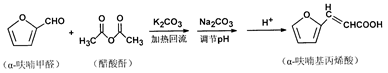
反应流程为:

已知:α-呋喃基丙烯酸为针状晶体,易溶于乙醇、乙醚,微溶于水。
请回答下列问题:
(1)醋酸酐过量的目的是_________________;
(2)加热回流在图1装置中进行(加热装置和夹持仪器均略去),仪器B的名称是__________;该过程中不同温度对产率的影响如图2所示,据此分析产率随温度变化的原因是__________;
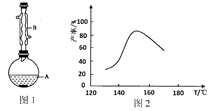
(3)活性炭脱色后,需趁热过滤的原因是__________;
(4)在冰水浴中边搅拌边滴加浓盐酸,判断浓盐酸已过量的方法是__________;
(5)提纯该粗产品的实验操作名称为__________。
-
为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:KIO3+5KI+3H2SO4 = 3I2+3K2SO4+3H2O
①该反应中,还原剂是___________,还原产物是___________。
②当有6molI2生成时,有_________mol还原剂被氧化。
③用单线桥表示电子的转移KIO3+5KI+3H2SO4 ═3K2SO4+3I2+3H2O
-
【加试题】常温下碘酸钙[Ca(IO3)2]是一种白色晶体,微溶于水,不溶于乙醇,能溶于盐酸,是目前广泛使用的既能补碘又能补钙的新型食品和词料添加剂。其制备原理如下:
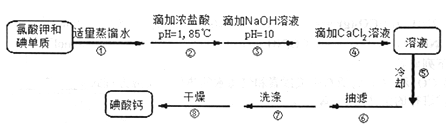
Ⅰ.碘酸钙的制备
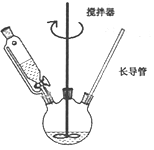
(1)某同学设计的实验装置如下图所示(夹持装置已省略),步骤②的加热方式为_________。
(2)步骤⑤冷却热的饱和溶液没有析出晶体,为了得到晶体可以采取的一种措施是________。
(3)步骤⑦洗涤的具体操作是____________。
Ⅱ.产品纯度测定
准确称取0.5000 g样品,酸化溶解,定容至250 mL,从中取出25.00 mL试样于锥形瓶中,加入足量的KI充分反应,用0.04000 mol·L-1硫代硫酸钠溶液滴定至终点,重复以上步骤,所测得实验数据如下:
| 1 | 2 | 3 |
| 滴定起始读数/mL | 1.52 | 1.16 | 0.84 |
| 滴定终止读数/mL | 31.50 | 31.18 | 30.84 |
己知:2Na2S2O3 + I2= Na2S4O6 + 2NaI
(4)加入KI时发生反应的离子方程式是_____________。
(5)滴定时所用的指示剂是_________________.
(6)经计算产品的纯度为________________。
-
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH===5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法中正确的是( )
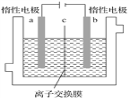
A. 电解过程中OH-从a极区通过离子交换膜c进入b极区
B. 随着电解进行,KOH溶液浓度会逐渐减小
C. a电极反应式:I--6e-+6OH-=== IO3-+3H2O,a极区的KI最终转变为KIO3
D. 当阳极有0.1 mol I-放电时,阴极生成6.72 L H2
-
我国从1994年起在食盐中添加碘酸钾(KIO3)作为营养强化剂。请回答:
(1)成人如果长期缺碘,会引起的病症是 (填字母)。
A.佝偻病 B.甲状腺肿大 C.夜盲症
(2)在瘦肉、胡萝卜、海带中,富含碘元素的是 。
(3)依据化学方程式为:5KI+KIO3+6HCl = 6KCl+3I2 +3H2O可检验加碘盐中是否含有碘。此反应中的还原剂是 (填化学式),生成的含I2的溶液遇淀粉可变为 色。
-
我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3),据此回答下列问题:
(1)碘是合成下列哪种激素的主要原料之一( )
A、胰岛素
B、甲状腺素
C、生长激素
D、雄性激素
(2)长期生活在缺碘山区,又得不到食盐供应,易患( )
A、甲状腺亢进
B、贫血症
C、地方性甲状腺肿
D、糖尿病
(3)可用盐酸酸化的碘化钾淀粉溶液,检查食盐中含碘酸钾。反应的化学方程式为 。可观察到的明显现象为 。
-
(8分)我国从1994年起在食盐中添加碘酸钾(KIO3)作为营养强化剂。请回答:
(1)成人如果长期缺碘,会引起的病症是________(填字母)。
A.佝偻病 B.甲状腺肿大 C.夜盲症
(2)在瘦肉、胡萝卜、海带中,富含碘元素的是________ 。
(3)依据化学方程式为:5KI+KIO3+6HCl = 6KCl+3I2 +3H2O可检验加碘盐中是否含有碘。此反应中的还原剂是________(填化学式),生成的含I2的溶液遇淀粉可变为________色。
-
(8分)我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3),据此回答下列问题:
(1)碘是合成下列哪种激素的主要原料之一 ________
A、胰岛素 B、甲状腺素 C、生长激素 D、雄性激素
(2)长期生活在缺碘地区,又得不到食盐供应,易患________
A、甲状腺亢进 B、贫血症 C、地方性甲状腺肿 D、糖尿病
(3)可用盐酸酸化的碘化钾淀粉溶液,检查食盐中含碘酸钾。反应的化学方程式为
5KI + KIO3 + 6HCl === 6KCl + 3I2 +3H2O。
此反应的氧化剂是________(填化学式),可观察到的现象是________。







