-
已知下列数据:
2Fe(s)+O2(g)===2FeO(s) ΔH=-544 kJ·mol-1
4Al(s)+3O2(g)===2Al2O3(s) ΔH=-3 350 kJ·mol-1
则2Al(s)+3FeO(s)===Al2O3(s)+3Fe(s)的ΔH是
A.-859 kJ·mol-1 B.+859 kJ·mol-1
C.-1 403 kJ·mol-1 D.-2 491 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
已知:
2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s) △H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
A.- 859 kJ·mol-1 B.+859 kJ·mol-1
C.-1403 kJ·mol-1 D.-2491 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
已知下列数据:
2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s) △H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
A.- 859 kJ·mol-1 B.+859 kJ·mol-1
C.-1403 kJ·mol-1 D.-2491 kJ·mol-1
高二化学选择题简单题查看答案及解析
-
已知下列数据:4Al(s)+3O2(g)=2Al2O3(s) △H=-3350kJ·mol-1
2Fe(s)+O2(g)=2FeO(s) △H=-544kJ·mol-1
则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是( )
A. +1403 kJ·mol-1 B. -859 kJ·mol-1
C. -1718 kJ·mol-1 D. -2806kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
已知下列数据:
4Al(s)+3O2(g)=2Al2O3(s) △H=-3350kJ·mol-1
2Fe(s)+O2(g)=2FeO(s) △H=-544kJ·mol-1
则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是( )
A.-859 kJ·mol-1 B.+1403 kJ·mol-1 C.-1718 kJ·mol-1 D.-2806kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
(1)已知热化学方程式:
4Al (s) + 3O2(g) = 2Al2O3 (s) ΔH1=-3288.6 kJ·mol-1,
4Fe (s) + 3O2 (g) =2Fe2O3 (s) ΔH2=-1631.8 kJ·mol-1,
则铝粉与氧化铁发生铝热反应的热化学方程式为________ 。
(2)已知标准状况下44.8L氢气燃烧生成液态水时放出571.6KJ的热量,氢气的燃烧热为 ________;又已知1mol液态水变成气态时需要吸收44KJ的热量,则标准状况下22.4L氢气燃烧生成气态水的热化学方程式为 ________ 。
高二化学填空题中等难度题查看答案及解析
-
(1)已知:①2Fe(s)+O2(g)=2 FeO(s)△H1=﹣544.0kJ•mol﹣1;
②4Al(s)+3O2(g)═2Al2O3(s)△H2=﹣3351.4kJ•mol﹣1。
Al和FeO发生铝热反应的热化学方程式是
(2)反应物与生成物均为气态的
某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
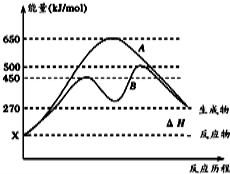
①据图判断该反应是 (填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,逆反应速率将 (填“增大”、“减小”或“不变”)。
②其中B历程表明此反应采用的条件为 (填字母)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
(3)已知热化学方程式:2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ•mol﹣1,该反应的活化能为334.4kJ•mol﹣1,则其逆反应的活化能为
。
高二化学填空题困难题查看答案及解析
-
已知25℃、101kPa条件下:4Al (s) + 3O2 (g) == 2Al2O3 (s) △H = -2834.9 kJ·mol-1
4Al (s) +2O3 (g) == 2Al2O3 (s) △H = -3119.91 kJ·mol-1,由此得出的结论正确的是
A.等质量的O2比O3能量低,由O2变O3 为吸热反应
B.等质量的O2比O3能量低,由O2变O3 为放热反应
C.O3比O2稳定,由O2变O3 为吸热反应
D.O2比O3稳定,由O2变O3 为放热反应
高二化学选择题简单题查看答案及解析
-
已知25℃、10lkPa条件下:
4Al(s) + 3O2(g) = 2Al2O3(s) ΔH=-2834.9 kJ·mol-1
4Al(s) + 2O3(g) = 2Al2O3(s) ΔH=-3119.1 kJ·mol-1
由此得出的正确结论是:( )
A、等质量的O2比O3能量低,由O2变O3为吸热反应
B、等质量的O2比O3能量低,由O2变O3为放热反应
C、O3比O2稳定,由O2变O3为吸热反应
D、O2比O3稳定,由O2变O3为放热反应
高二化学选择题中等难度题查看答案及解析
-
在常温常压下,已知:
4Fe(s) + 3O2(g) = 2Fe2O3(s) ΔH1
4Al(s) + 3O2(g) = 2Al2O3(s) ΔH2
2Al(s) + Fe2O3(s) = Al2O3(s) + 2Fe(s) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是
A.ΔH3=
(ΔH1+ΔH2) B.ΔH3=ΔH2-ΔH1
C.ΔH3=2(ΔH2+ΔH1) D.ΔH3=
(ΔH2-ΔH1)
高二化学选择题中等难度题查看答案及解析