-
已知X、Y、Z、W、Q都是周期表中短周期的元素,它们的核电荷数依次增大.其中X、Y、Z是同周期的非金属元素.W的三价阳离子与Z的阴离子具有相同的电子层结构,它们相互形成的化合物中存在离子键;XZ2为非极性分子;Y、Z 氢化物的沸点比它们同族其他元素氢化物的沸点高;Q在同周期元素中原子半径最小.
回答下列问题:
(1)写出化合物XZ2的电子式______,其晶体类型为______.
(2)Y、Z 氢化物的沸点比它们同族元素氢化物的沸点高的原因是______.
(3)将少量YZ2通入过量小苏打溶液中,再使逸出的气体通过装有足量过氧化钠颗粒的干燥管,最后收集到的气体是______.
(4)某温度下,在2L密闭容器中投入0.2mol H2和0.2mol XZ2,发生如下反应:H2+XZ2⇌H2Z+XZ 测得平衡时,XZ2的转化率为60%,则该温度下的平衡常数为______.
(5)高铁酸钾(K2FeO4)是一种新型的高效氧化剂和消毒剂,常用于饮用水处理.工业生产高铁酸钾的方法为:①常温下先将Q的单质通入氢氧化钠溶液中制得含Q元素的一种含氧酸盐;②再将其与氢氧化钠溶液混合氧化硝酸铁,得到高铁酸钠粗产品;③过滤后用氢氧化钾溶液溶解,重结晶,再经过脱碱、洗涤、干燥处理,得到高铁酸钾.写出②中发生反应的离子方程式______,第③步中高铁酸钠能够转化为高铁酸钾的原因是______.高三化学解答题中等难度题查看答案及解析
-
X、Y、Z、W、Q、R 是周期表中前 36 号元素,核电荷数依次增大,其中 X、Y、Z、 W 都是元素周期表中短周期元素。X 为非金属元素,且 X 原子的核外成对电子数是未成对电子数的 2 倍,Z 的次外层电子数是最外层电子数的
,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。 回答下列问题:
(1)X的最高价氧化物对应的水化物分子中,中心原子采取______________杂化。
(2)化合物 XZ 与 Y 的单质分子互为______________,1mol XZ 中含有π键的数目为______________。
(3)W 的稳定离子核外有______________种运动状态的电子。W元素的第一电离能比其同周期 相邻元素的第一电离能高,其原因是:_____。
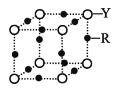
(4)Q 的晶体结构如图所示,则在单位晶胞中 Q 原子的个数为______________,晶体的配位数是______________。
(5)R元素的基态原子的核外电子排布式为________;Y 与 R 形成某 种化合物的晶胞结构如图所示,已知该晶体的密度为ρg·cm-3,阿伏加德罗常数的数值为 NA,则该晶体中 R 原子和 Y 原子之间的最短距离为______________cm。(只写计算式)
高三化学综合题中等难度题查看答案及解析
-
X、Y、Z、W、Q、R 是周期表中前 36 号元素,核电荷数依次增大,其中 X、Y、Z、 W 都是元素周期表中短周期元素。X 为非金属元素,且 X 原子的核外成对电子数是未成对电子数的 2 倍,Z 的次外层电子数是最外层电子数的
,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。 回答下列问题:
(1)X的最高价氧化物对应的水化物分子中,中心原子采取______________杂化。
(2)化合物 XZ 与 Y 的单质分子互为______________,1mol XZ 中含有π键的数目为______________。
(3)W 的稳定离子核外有______________种运动状态的电子。W元素的第一电离能比其同周期 相邻元素的第一电离能高,其原因是:_____。
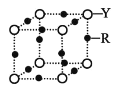
(4)Q 的晶体结构如图所示,则在单位晶胞中 Q 原子的个数为______________,晶体的配位数是______________。
(5)R元素的基态原子的核外电子排布式为________;Y 与 R 形成某 种化合物的晶胞结构如图所示,已知该晶体的密度为ρg·cm-3,阿伏加德罗常数的数值为 NA,则该晶体中 R 原子和 Y 原子之间的最短距离为______________cm。(只写计算式)
高三化学综合题中等难度题查看答案及解析
-
(16分)A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5。请回答下列问题(用相应的元素符号、化学式和化学术语填空)
(1)G在周期表中的位置是____,F元素的原子基态价层电子排布式__ 。
(2)BD2分子的电子式为__________,CA3分子的空间立体构型为__________。
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:__________、I:__________。
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有__________。
(5)0.3g H在足量氧气中燃烧,生成气态CO2和液态H2O,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为____________________。
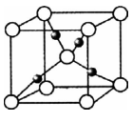
高三化学填空题极难题查看答案及解析
-
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素, F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个成单电子,G是ⅠB族的元素。回答下列问题:
(1)写出E、F、G的元素符号,B、C、D元素的第一电离能由大到小的顺序是________(用元素符号表示),A元素分别与B、D元素形成的二种微粒都具有NH3相似的结构,属于等电子体,它们的化学式是________。
(2)F元素的原子基态价层电子排布图是________。
(3)向G的硫酸盐溶液中滴加氨水会生成蓝色沉淀,继续滴加氨水至沉淀刚好全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[G(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过________键与中心离子G2+结合;NH3分子中N原子的杂化方式是________;
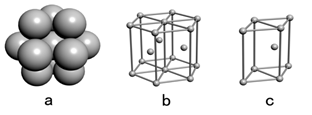
(4)E单质晶体中原子的堆积模型如右图,晶胞是图中的________(填a、b或c);配位数是________;若紧邻的四个E原子的中心连线构成的几何体的体积是a cm3,E单质的密度为ρg/ cm3;则E的相对原子质量的计算式是________ 。
高三化学填空题极难题查看答案及解析
-
A、B、C、D、E代表原子序数依次增大的前四周期元素,其中A和C为同一主族,C常用于制作半导体器件和集成电路,B的简单氢化物的水溶液呈碱性,E元素的正三价离子的3d亚层为半充满,D被称为“未来金属”,其重量轻、强度高、耐腐蚀,其在周期表中位于第4周期、第ⅣB族。
(1)A、B、C三种元素的第一电离能由小到大的顺序为______________________,电负性由小到大的顺序为____________________。
(2)B的简单氢化物易液化的原因是_______________;BH4+中B原子的杂化方式为___________,空间构型为__________________。
(3)E元素基态原子的电子排布式为____________________________________。
(4)B和C形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于__________________晶体。
(5)D有多种氧化物,其中一种氧化物的晶胞结构如图1所示,则该晶体中D的配位数为__________________;图2为E的一种面心立方晶胞结构,若晶胞的边长为acm,NA表示阿伏加德罗常数的值,则E的密度为__________________g·cm-3(用含a和NA的代数式表示)。

高三化学综合题中等难度题查看答案及解析
-
[选修物质结构与性质]已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素,其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的+3价离子的3d能级为半充满状态.(答题时用ABCDE对应的元素符号表示)
(1)A的氢化物A2H2分子的空间构型为______,其中心原子采取的杂化形式为______,分子中含有______个σ键,______π键.
(2)写出化合物DC的电子式______,E原子的核外电子排布式______.
(3)由E元素形成的金属的晶胞结构如图,则该晶胞中含有金属原子的数目为______.
(4)化合物E(CO)5常温下为液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于______(填晶体类型).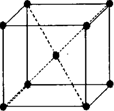
高三化学解答题中等难度题查看答案及解析
-
已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素,其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的+3价离子的3d能级为半充满状态。(答题时用ABCDE对应的元素符号表示)
(1)A的氢化物A2H2分子的空间构型为__________,其中心原子采取的杂化形式为___________,分子中含有___________个
键,__________π键。
(2)写出化合物DC的电子式_______,E原子的核外电子排布式________。
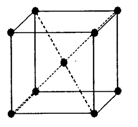
(3)由E元素形成的金属的晶胞结构如右图,则该晶胞中含有金属原子的数目为_______________。
(4)化合物E(CO)5常温下为液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于__________(填晶体类型)。
高三化学填空题简单题查看答案及解析
-
(15分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;元素B的氢化物能用于刻蚀玻璃; C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是___________,A、B、C、D的第一电离能由小到大的顺序为__________。
(2)化合物CA的熔点远高于C的氯化物的熔点,理由是______________;
(3)A的最高价含氧酸根离子中,其中心原子采取_____杂化,D的低价氧化物分子的空间构型是_______。
(4)B2与NaOH溶液反应的产物之一是OB2,该反应的离子方程式为__________。
高三化学填空题困难题查看答案及解析
-
【化学—选修3:物质结构】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子; B元素是地壳中含量最多的金属元素;C原子核外的M层中有两对成对电子;D是使用最广泛的合金的主要成分。E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E+离子的最外层电子排布式_____________ ,A、B、C的第一电离能最小的是____________ 。
(2)A的最高价含氧酸分子中心原子是____________________杂化。
(3)A、B形成某种化合物的晶胞结构如下图一所示(“O”表示B原子),则其化学式为________ ,一个A原子周围距离最近且等距的A原子有_____________个。B原子的堆积方式与下图中的_______相同。(填“图二”或“图三”)

(4)1183 K 以下D 晶体的晶胞为钾型,而1183 K 以上则转变为铜型,在两种晶胞中最邻近的D 原子间距离相同,则两种晶体中原子的空间利用率之比为____(可用根号表示)。
(5)开发新型储氢材料是氢能利用的重要研究方向。分子X 可以通过氢键形成“笼状结构”而成为潜在的储氢材料。X 一定不是______(填标号)。
A. H2O B. CH4 C. HF D. CO(NH2)2
高三化学推断题困难题查看答案及解析