-
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
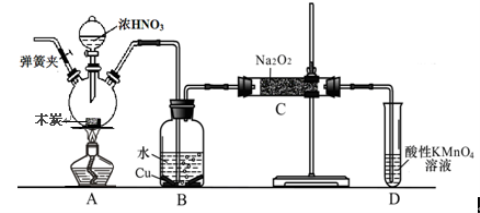
已知:室温下,①2NO+Na2O2 = 2NaNO2
②3NaNO2+3HCl == 3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO或NO2– 都能与MnO4–反应生成NO3– 和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2) B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 。
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
-
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛.现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示(部分夹持装置略).
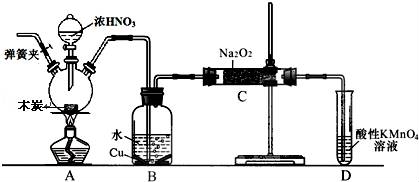
已知:室温下,①2NO+Na2O2=2NaNO2②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;③酸性条件下,NO或NO2﹣ 都能与MnO4﹣反应生成NO3﹣ 和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 .
(2)B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 .
(3)检验C中产物有亚硝酸钠的方法是 .
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 .
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g.
-
(12分)重铬酸钠Na2Cr2O7·2H2O俗称红矾钠,是一种重要的无机盐产品,可作氧化剂,在印染、颜料、电镀、医药等工业方面有广泛的用途。某化学兴趣小组设计实验测定市场上的红矾钠中Na2Cr2O7的质量分数,其步骤如下:
I.称取Wg红矾钠,溶于酸配成l00mL溶液;
Ⅱ.用cmol·L-1的标准KMnO4酸性溶液滴定20.00mL一定浓度的FeSO4溶液,消耗KMnO4溶液20.00rnL;
Ⅲ.取20.00mL Na2Cr2O7溶液,用上述FeSO4溶液滴定,达到滴定终点时,消耗24.00mLFeSO4溶液;
查阅资料知:Cr相对原子质量为52
Cr2O2-7具有强氧化性,在酸性条件下易被还原为Cr3+
回答下列问题:
(1)Na2Cr2O7与FeSO4的反应离子方程式为.
(2)步骤Ⅱ中的滴定过程选用________(填“酸式”或“碱式”)滴定管。
(3)已知:MnO-4+5Fe2++8H+==Mn2++5Fe3++4H2O,此红矾钠中Na2Cr2O7的质量分数的表达式为________。
(4)判断下列操作对Na2Cr2O7的质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”):
①步骤Ⅲ中的滴定过程,滴定终点读数时俯视读数________;
②配制c mol·L-1的KMnO4标准溶液时,转移时有少量溶液洒出________。
(5)有同学提出FeSO4有很强的还原性,在空气中易被氧化而变质,因此对测定结果会造成影响,请你分析后指出,如果FeSO4变质,对测定结果的影响是________(填“偏高”、“偏低”或“无影响”)。
-
下列有关化学反应的叙述正确的是( )
A.过氧化钠在空气中变色,发生了氧化还原反应
B.工业上可用氯气和澄清石灰水反应制漂白粉
C.硫在过量氧气中燃烧生成三氧化硫
D.过量的铜和浓硝酸反应时只生成一种气体
-
甘油是一种在医药、化妆品等方面应用广泛的保湿、保润剂,也是一种重要的工业原料,可用于合成环氧树脂、油脂、硝化甘油(三硝酸甘泊酯)等。由烷烃A合成甘油及其衍生物的一种路线如下图所示,请回答下列问题。
己如:①烷烃A的相对分子质量为44;B的核磁共振氢谱有两个峰。
②
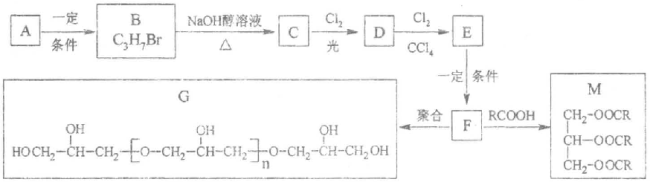
(1)A 的分子式(或化学式)为__________,F的官能团是____________。
(2)B→C的反应类型属于___________反应;F→G的反应类型属于_______(填“加聚”或“缩聚”)反应。
(3)B 的同分异构体的结构简式为_________,C与Cl2反应除生成D 外,另一无机产物为_______(写化学)。
(4)由D→E的化学方程式为:__________________。
(5)硝化甘油既是一种炸药,也是一种心绞痛急救药,它可由F 与硝酸制得。硝化甘油的结构简式为____________。
(6)1 mol M与足量的NaOH 洛液完全反应,至少消耗NaOH_______mol。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
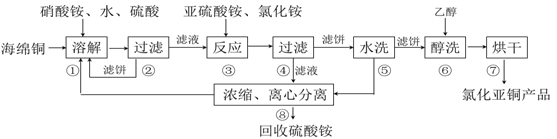
回答下列问题:
(1)步骤①溶解温度应控制在60~70度,原因是_____________,加入硝酸铵的作用是_____________。
(2)写出步骤③中主要反应的离子方程式_______________。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_____________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是 。
(5)准确称取所制备的氯化亚铜样品m g,将其置于若两的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。
-
碳及其化合物在有机合成、能源开发等方面具有十分广泛的应用。
Ⅰ.工业生产精细化工产品乙二醛(OHC—CHO)
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,此反应的化学方程式为_____________,该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点: ___________________。
(2)乙二醇(HOCH2CH2OH)气相氧化法
①已知:2H2(g)+O2(g) ⇌2H2O(g) ΔH=-484 kJ/mol,化学平衡常数为K1。
OHC—CHO(g)+2H2(g) ⇌HOCH2CH2OH(g) ΔH=-78 kJ/mol,化学平衡常数为K2。
则乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) ⇌OHC—CHO(g)+2H2O(g)的ΔH=______。相同温度下,该反应的化学平衡常数K=_______(用含K1、K2的代数式表示)。
②当原料气中氧醇比为4∶3时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495 ℃之间和超过495℃时,乙二醛产率降低的主要原因分别是____________、___________。
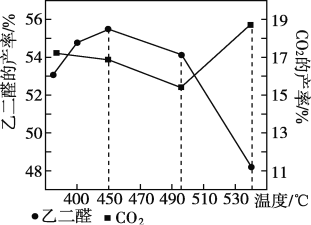
Ⅱ.副产物CO2的再利用
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生反应C(s)+CO2(g) ⇌2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是______(填字母)。
A.550℃时,若充入氢气,则v正、v逆均减小,平衡不移动
B.650℃时,反应达平衡后CO2的转化率为25%
C.T℃时,若再充入等物质的量的CO2和CO,平衡向逆反应方向移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0p总
已知:计算用平衡分压代替平衡浓度,气体分压(p分)=气体总压(p总)×体积分数。

-
请阅读下列材料,回答下列小题
将一定比例的三氧化硫和水混合可制得硫酸。硫酸是一种重要的化工原料,用途十分广泛,除用于化学工业外,还非常广泛应用于肥料、非碱性清洁剂、护肤品、油漆添加剂与炸药的制造等方面。
1.关于浓硫酸的说法正确的是
A.易挥发
B.见光分解
C.密度比水的小
D.常温下能使铝片钝化,浓硫酸作氧化剂
2.稀硫酸可以用于实验室制氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑,该反应的反应类型说法正确的是
A.化合反应 B.复分解反应 C.置换反应 D.分解反应
3.在其他条件不变的情况下,欲提高硫酸与锌反应产生氢气的速率,可以采用的措施有
A.选用颗粒更大的锌粒
B.升高反应温度
C.用98%浓硫酸来代替稀硫酸反应
D.加入硫酸钾溶液
4.下列反应中,生成物总能量高于反应物总能量的是
A.S+O2 SO2
SO2
B.CaO+H2O=Ca(OH)2
C.C+CO2 2CO
2CO
D.Zn+H2SO4=ZnSO4+H2↑
-
(16分)甲醇是重要的化工原料,在工业生产上的应用十分广泛,二氧化碳被认为是加剧温室效应的主要来源,如何有效地开发利用CO2引起了全世界的普遍重视。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)将CO2转化成甲醇燃料是减排、环保的一种科学方法。
已知:2H2(g)+O2(g) =2H2O(g);△H=-483. 6kJ·mol-1 ①
2CO2(g)+4H2O(g)  2CH3OH(g)+3O2(g);ΔH=+1352.8kJ·mol-1②
2CH3OH(g)+3O2(g);ΔH=+1352.8kJ·mol-1②
则反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)的ΔH= 。
CH3OH(g)+H2O(g)的ΔH= 。
(2)500 ℃时,在体积为1 L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,回答下列问题:

①计算从反应开始到10min时,H2的反应速率及该温度下反应的平衡常数。
(写出具体的计算过程)
②下列措施不能使CO2的转化率增大的是______(双选)。
A.在原容器中再充入lmol CO2
B.在原容器中再充入1mol H2
C.将反应体系温度降低
D.使用更有效的催化剂
③升高温度,800℃时,在体积为1 L 的固定容积的密闭容器中充入1mol CO2、3mol H2,在上图中画出CH3OH 浓度随时间变化的曲线(不需要定量计算)。
-
过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
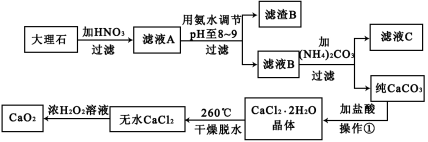
请回答下列问题:
(1)用氨水调节pH至8——9的目的是 。
(2)若测得滤液C中c(CO32-)=10-3mol/L,则Ca2+ (填“是”或“否”)沉淀完全。(已知c(Ca2+)≤10-5mol/L可视为沉淀完全;Ksp(CaCO3)=4.96×10-9)
(3)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中,c(NH4+) c(NO3-)(填“≥”、“≤”、“<”、“>”或“=”)。
(4)在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,写出该反应的化学方程式: ,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9——11,才出现大量沉淀。用化学方程式和简要的文字解释需用氢氧化钠调节pH至9——11的原因 。








