直接电解吸收是烟气脱硝的一种有效方法。用6%的稀硝酸吸收NOx会生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸。电解装置如下(阴、阳离子可通过隔膜,但分子不能通过):
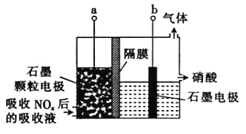
下列说法不正确的是
A. 吸收NOx的过程涉及氧化还原反应
B. 石墨电极为颗粒状,可增大接触面积,提高电解效率
C. 当b极上产生2.8 L(标准状况)H2时,转移的电子数为0.5NA(设NA为阿伏加德罗常数的数值)
D. 极的电极反应式为HNO2-2e-+H2O=3H++N03-
高三化学单选题中等难度题
直接电解吸收是烟气脱硝的一种有效方法。用6%的稀硝酸吸收NOx会生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸。电解装置如下(阴、阳离子可通过隔膜,但分子不能通过):

下列说法不正确的是
A. 吸收NOx的过程涉及氧化还原反应
B. 石墨电极为颗粒状,可增大接触面积,提高电解效率
C. 当b极上产生2.8 L(标准状况)H2时,转移的电子数为0.5NA(设NA为阿伏加德罗常数的数值)
D. 极的电极反应式为HNO2-2e-+H2O=3H++N03-
高三化学单选题中等难度题
直接电解吸收是烟气脱硝的一种有效方法。用6%的稀硝酸吸收NOx会生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸。电解装置如下(阴、阳离子可通过隔膜,但分子不能通过):

下列说法不正确的是
A. 吸收NOx的过程涉及氧化还原反应
B. 石墨电极为颗粒状,可增大接触面积,提高电解效率
C. 当b极上产生2.8 L(标准状况)H2时,转移的电子数为0.5NA(设NA为阿伏加德罗常数的数值)
D. 极的电极反应式为HNO2-2e-+H2O=3H++N03-
高三化学单选题中等难度题查看答案及解析
直接电解吸收是烟气脱硝的一种有效方法。用6%的稀硝酸吸收NOx会生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸。电解装置如下所示(阴、阳离子可通过隔膜,但分子不能通过)下列说法不正确的是( )

A.吸收NOx的过程涉及氧化还原反应
B.石墨电极为颗粒状,可增大接触面积提高电解效率
C.当a极转移电子数为0.5NA时,b极放出11.2L气体(标准状况)
D.a极的电极反应式为HNO2-2e-+H2O=3H++NO3-
高三化学单选题中等难度题查看答案及解析
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如右图所示(图中电极均为石墨电极)。
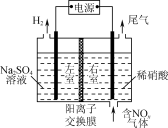
(1)若用NO2气体进行模拟电解法吸收实验。
① 写出电解时NO2发生反应的电极反应式:________。
② 若有标准状况下2.24 L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为________mol。
(2)某小组在右室装有10 L 0.2 mol·L-1硝酸,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。
①实验前,配制10 L 0.2 mol·L-1硝酸溶液需量取________mL密度为1.4 g·mL-1、质量分数为63%的浓硝酸。
②电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中含3 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28 LH2。计算原气体中NO和NO2的体积比(假设尾气不含氮氧化物,写出计算过程)。
高三化学简答题困难题查看答案及解析
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如右图所示(图中电极均为石墨电极)。
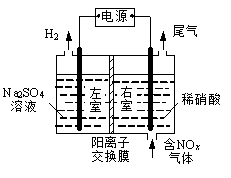
(1)若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式: 。
②若有标准状况下2.24 LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为 mol。
(2)某小组在右室装有10 L 0.2 mol·L-1硝酸,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。
①实验前,配制10 L 0.2 mol·L-1硝酸溶液,需量取 mL的密度为1.4 g·mL-1、质量分数为63%的浓硝酸。
②电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中含3 molHNO3、0.1 molHNO2,同时左室收集到标准状况下28 L H2。计算原气体中NO和NO2的体积比(假设尾气中不含氮氧化物,写出计算过程)。
高三化学计算题中等难度题查看答案及解析
合成氨厂和硝酸厂的烟气中含有大量的氮氧化物(NOx),通常使用以下两种方法将烟气中的氮氧化物转化为无害物质。
(1)还原法。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其转化过程如下图所示。
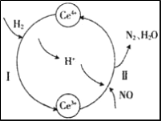
①过程混合溶液中Ce3+和Ce4+离子的总数________(填“增大”、“减小”或“不变”)。
②反应II中氧化剂与还原剂的物质的量之比为________________。
(2)电解法。先用6%稀硝酸吸收NOx,会生成HNO2(一元弱酸),再将吸收液导入电解槽中进行电解,使之转化为硝酸,其电解装置如图所示:
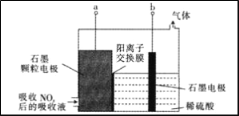
①中a应连接电源的____________(填“正极”或“负极”)。
②石墨电极做成颗粒状的目的是________________。
③阳极的电极反应式为____________________________________。
④电解一段时间后,当电路中有5mol电子转移时,阳离子交换膜两侧溶液相差____g。
高三化学综合题中等难度题查看答案及解析
烟气(主要成分CO2、CO、SO2、NOX) 的排放对环境有很大的影响。
I.利用氨水作吸收液是当前有效捕捉CO2的方法,经过可逆反应生成NH4HCO3。生成的NH4HCO3分解可得到CO2,从而实现吸收液的再生。
(1)写出氨水捕捉 CO2 的化学方程式 。
(2)已知:NH4HCO3 溶液显碱性,下列说法不正确的是 。
a .c (NH3·H2O) > c (H2CO3)
b.c (NH4+) > c (HCO3-) > c (OH-) > c (H+)
c.c (NH3·H2O) + c (NH4+) = c (H2CO3) + c (HCO3-)
d .c (HCO3-) + 2c (CO32-) + c (OH-) = c (H+)+c (NH4+)
(3)右图是氨水吸收 CO2 的脱除率随温度变化的关系图。应用平衡移动原理分析 CO2 在 40℃-45℃ 脱除率降低可能的原因 。

(4)捕捉的 CO2 和 H2O 的混合气体在固态金属氧化物电解池中电解可制备 H2 和 CO,是一种新的能源利用方式,基本原理如图所示。
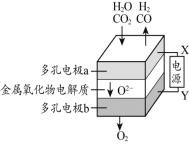
①X 是电源的 (填“正极”或“负极”),a电极上发生的电极反应式为:H2O + 2eˉ = H2+ O2ˉ和 。
②a 和 b 两电极产生的气体的物质的量之比为 。
II.SO2、NOX 可以经 O3 预处理后用 CaSO3 水悬浮液吸收,可减少烟气中SO2、NOX 的含量。O3 氧化烟气中 NOX 的主要反应的热化学方程式为:
NO (g) +O3 (g) = NO2 (g) +O2 (g) ∆ H = -200.9 kJ · mol-1
NO (g) +1/2O2 (g) = NO2 (g) ∆ H = -58.2 kJ · mol-1
(5)依据以上反应,可知:3 NO (g)+O3 (g) = 3 NO2 (g) ∆ H = kJ · mol-1。
(6)用CaSO3水悬浮液吸收烟气中NO2时,清液 ( pH约为8) 中SO32-将NO2转化为NO2-,其离子方程式为 。
(7)CaSO3水悬浮液中加入Na2SO4溶液能提高NO2 的吸收速率,用平衡移动原理解释其主要原因是 。
高三化学填空题困难题查看答案及解析
烟气(主要成分CO2、CO、SO2、NOX) 的排放对环境有很大的影响。
I.利用氨水作吸收液是当前有效捕捉CO2的方法,经过可逆反应生成NH4HCO3。生成的NH4HCO3分解可得到CO2,从而实现吸收液的再生。
(1)写出氨水捕捉CO2 的化学方程式 。
(2)已知:NH4HCO3 溶液显碱性,下列说法不正确的是 。
a.c(NH3·H2O)>c(H2CO3)
b.c(NH4+)>c(HCO3—)>c(OH—)>c(H+)
c.c(NH3·H2O)+c(NH4+)=c(H2CO3)+c(HCO3—)
d.c(HCO3—)+2c(CO32—)+c(OH—)=c(H+)+c(NH4+)
(3)如图是氨水吸收CO2 的脱除率随温度变化的关系图。
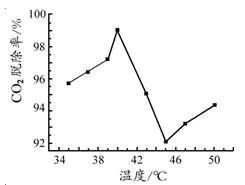
应用平衡移动原理分析 CO2 在 40℃-45℃ 脱除率降低可能的原因 。
II.SO2、NOX 可以经 O3 预处理后用 CaSO3 水悬浮液吸收,可减少烟气中SO2、NOX 的含量。O3 氧化烟气中 NOX 的主要反应的热化学方程式为:
(4)用CaSO3水悬浮液吸收烟气中NO2时,清液 ( pH约为8) 中SO32-将NO2转化为NO2-,其离子方程式为 。
(5)CaSO3水悬浮液中加入Na2SO4溶液能提高NO2 的吸收速率,用平衡移动原理解释其主要原因是 。
高三化学简答题困难题查看答案及解析
(主要指NO和
)是大气主要污染物之一。有效去除大气中的
,是环境保护的重要课题。
(1)用稀硝酸吸收,得到
和
的混合溶液,惰性电极电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:______________________________________。
(2)在有氧条件下,新型催化剂M能催化与
反应生成
。
①写出与
反应方程式__________________________________________。
②将一定比例的、
和
的混合气体,匀速通入装有催化剂M的反应器中反应(如图-1所示)
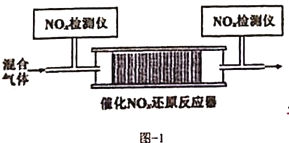
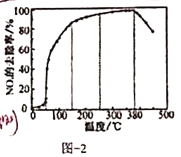
反应相同时间的去除率随反应温度的变化曲线如图-2所示,在50~150℃范围内随着温度的升高,
的去除率迅速上升的主要原因是_____________________________,150~380℃范围
的去除率上升缓慢的主要原因是_____________________________。当反应温度高于380℃时,
的去除率迅速下降的原因可能是:_____________________________;_____________________________。
高三化学综合题困难题查看答案及解析
硝酸厂的烟气中含有大量的氮氧化物(NOx),将烟气与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3[Ce中文名“铈”]的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
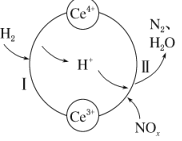
A.该转化过程的实质为NOx被H2还原
B.x=l时,过程II中氧化剂与还原剂的物质的量之比为2:1
C.处理过程中,混合溶液中Ce3+和Ce4+总数减少
D.过程I发生反应的离子方程式:H2+Ce4+=2H++Ce3+
高三化学单选题中等难度题查看答案及解析
燃煤烟气脱硫有很多方法
方法I:先用氨水将SO2转化为NH4HSO3,再通入空气氧化成(NH4)2SO4。
方法II:用Na2SO3溶液吸收S02,再经电解转化为H2SO4。
据此回答以下问题:
(1)方法I中发生氧化还原反应的离子方程式__________。能提高方法I燃煤烟气SO2中去除率的措施有__________(填字母)。
A.增大氨水浓度 B.增大燃煤烟气的流速
C.事先去除燃煤烟气中的二氧化碳 D.增大压强
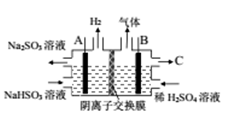
(2)采用方法II脱硫,燃煤烟气中的二氧化碳能否与生成的NaHSO3溶液反应_______(说明理由)。已知H2SO3为的电离平衡常数为K1=1.54×10-2,K2=1.02×10-7。则NaHSO3溶液中含S元素粒子浓度由大到小的顺序为_______。通过右图所示电解装置可将生成的NaHSO3转化为硫酸,电极材料皆为石墨。则A为电解池的______(填“阴极”或“阳极”)。C为______(填物质名称)。若将阴离子交换膜换成阳子交换膜,写出阳极区域发生的电极反应______。
高三化学填空题困难题查看答案及解析