-
氯碱工业是最基本的化学工业之一,它的产品应用广泛。请回答下列问题:
(1)氯碱工业是利用电解食盐水生产 为基础的工业体系。
(2)电解前,为除去食盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入下列试剂的顺序合理的是 (填下列各项中序号)。
a、碳酸钠、氢氧化钠、氯化钡 b、碳酸钠、氯化钡、氢氧化钠
c、氢氧化钠、碳酸钠、氯化钡 d、氯化钡、氢氧化钠、碳酸钠
(3)“盐泥”是电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
利用盐泥生产MgSO4·7H2O晶体的工艺流程如下图所示。

回答下列问题:
①酸洗过程中加入的酸为 ,加入的酸应适当过量,控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,在此过程中同时生成CaSO4。其中碳酸钙可以转化为硫酸钙的原因是 。
②过滤所得滤渣的主要成分为 。
③根据图分析,蒸发结晶过滤所得晶体A主要成分为 。

④真空干燥MgSO4·7H2O晶体的原因是 。
-
(共13分)氯碱工业是最基本的化学工业之一,其主要原理基于电解饱和食盐水:2NaCl+2H2O 2NaOH+H2↑+Cl2↑,它的产品烧碱和氯气以及氢气应用广泛。请回答下列问题:
2NaOH+H2↑+Cl2↑,它的产品烧碱和氯气以及氢气应用广泛。请回答下列问题:
(1)电解前,如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42- ,该钡试剂可以是______________(填字母代号)。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)“盐泥”是电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
利用盐泥生产MgSO4·7H2O晶体的工艺流程如下图所示。

回答下列问题:
①酸洗过程中加入适量硫酸控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,CaCO3在此过程中转化为CaSO4,请解释此转化得以发生的原因_________。
②过滤所得滤渣的主要成分为____________________________。
③根据下图分析,蒸发结晶过滤所得晶体A主要成分为____________________。

④真空干燥MgSO4·7H2O晶体的原因是______________________。
(3)已知NaCl在60 ℃的溶解度为37.1 g,现电解60 ℃精制饱和食盐水1371 g,经分析,电解后溶液密度为1.37 g·cm-3,其中含有20 g NaCl,则电解后NaOH的物质的量浓度为________________mol/L。
-
化学与生产、生活密切相关。下列说法错误的是( )
A.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2
B.电渗析法淡化海水利用了离子交换膜技术
C.硅橡胶既能耐高温又能耐低温,广泛应用于航天航空工业
D.木材和织物用水玻璃浸泡后,不易着火
-
化学与生产、生活密切相关。下列说法错误的是
A.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2
B.电渗析法淡化海水利用了离子交换膜技术
C.硅橡胶既能耐高温又能耐低温,广泛应用于航天航空工业
D.煤经过气化和液化等化学变化可转化为清洁能源
-
利用下图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是( )
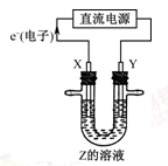
A.氯碱工业中,若X、Y均为石墨,Y附近能得到氯气
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.外加电流的阴极保护法中,Y是待保护金属
D.电镀工业中,X是待镀金属,Y是镀层金属
-
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
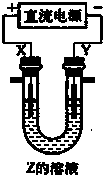
A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠
B.铜的精炼中,X是粗铜,Y是纯铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,Y是待保护金属
-
利用如下图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是

A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,Y是待保护金属
-
利用右图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。

下列说法中正确的是
A.氯碱工业中,X、Y均为石墨,Y附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,X是待保护金属
-
氯碱工业是最基本的化学工业之一,其产品用途广泛。
(1)写出氯碱工业电解食盐水的离子方程式____________。
(2)①图1是氯碱工业中阳离子交换膜电解槽示意图(“阳离子交换膜”特性是只允许阳离子通过而阻止阴离子和气体通过)。
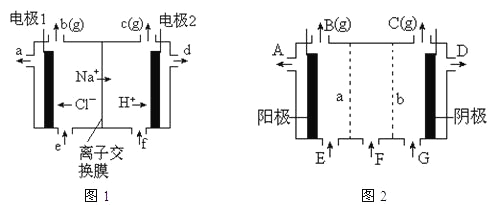
图1中电极1应连接电源的__极(填“正”或“负”极);理论上讲,从f口加入纯水即可,但实际生产中,纯水中要加入一定量的NaOH溶液,其原因是_____。
②图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。其中a、b处均设有离子交换膜,则a处为__(填“阳”、“阴”)离子交换膜。阳极的电极反应式是___。从D口流出的物质为____。
(3)某同学采用如下装置对氯碱工业中电解食盐水的条件进行探究,记录如下:
| 装置 | 编号 | 条件控制 | 测定结果 |
| 电极材料 | 溶液浓度 | 温度/℃ | *电解电压/V | 气体V阴:V阳 |
| 阴极 | 阳极 |
| 
| I | C | C | 1 mol/L | 25 | 8 | >1:1 |
| II | 饱和 | 25 | 5 | ≈1:1 |
| III | 饱和 | 50 | 4 | ≈1:1 |
| IV | Fe | C | 饱和 | 50 | 3.5 | ≈1:1 |
电解电压:开始发生电解反应时的电压
①对比实验I和Ⅱ阴、阳极气体体积比,推测实验I阳极可能有其它气体生成,其它气体的化学式为_____。
②资料显示:“较低的电解电压有利于节能降耗……”。结合上表中Ⅲ和Ⅳ的数据,解释Ⅳ更有利于节能降耗的原因_______________。
(4)资料显示“氯碱工业中采用金属阳极材料,可以降低电解电压,实现节能降耗”,该同学用50℃的饱和NaCl溶液进行实验验证,结果如下:
| 装置 | 编号 | 电极材料 | 电解 电压/V | 现象 |
| 阴极 | 阳极 |
| 
| V | Fe | Fe | 1.5 | 阴极:产生无色气体 U形管底部:有白色沉淀生成 |
| VI | Fe | Cu | 2 | 阴极:产生无色气体 阳极:有白色胶状沉淀生成且逐渐增多 U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色,最后变成砖红色 |
实验V中,通过检验阴、阳极附近溶液所含离子,推断产生白色沉淀为Fe(OH)2 。该同学经查阅资料分析认为:“实验VI中白色沉淀是CuCl,淡黄色沉淀是CuOH。
i.阳极生成CuCl的电极反应式为_________。
ii.用化学用语和必要文字解释阴极区白色胶状沉淀转化为淡黄色的原因___________。
该同学通过以上探究认为,氯碱工业中不能采用Fe、Cu作阳极材料。
(5)综合以上探究,你对氯碱工业中电解食盐水条件控制的建议有 _____(至少写出两条)。
-
(10)(1)氯碱工业是利用电解食盐水生产① 为基础的工业体系。
(2)电解前,为除去食盐水中的Mg2+、Ca2+、 等杂质离子,下列加入顺序合理的是________② 。
等杂质离子,下列加入顺序合理的是________② 。
A.碳酸钠、氢氧化钠、氯化钡 B.碳酸钠、氯化钡、氢氧化钠
C.氢氧化钠、碳酸钠、氯化钡 D.氯化钡、氢氧化钠、碳酸钠
(3)“盐泥”是粗盐提纯及电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶于酸的物质 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
为生产七水硫酸镁,设计了以下工艺流程:

生产七水硫酸镁工艺流程图
1-反应器 2-过滤器 3-蒸发浓缩器 4-结晶槽 5-洗涤槽 6-真空干燥器
装置1中加入的酸应选用________③ ,加入的酸应适当过量,控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,在此过程中同时生成CaSO4。其中碳酸钙可以转化为硫酸钙的原因是________④ 。
装置2中滤渣的主要成分为________⑤。
装置3中通入高温水蒸汽并控制温度在100~110℃,蒸发结晶,此时析出的晶体主要是__⑥__。
用装置6(真空干燥器)干燥七水硫酸镁晶体的理由是________⑦ 。









