-
19-I(6分)下列描述中正确的是
A.CS2为V形的极性分子
B.Cl0— 3 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO2— 3 的中心原子均为sp3杂化
19-Ⅱ(14分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为______________________________;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO ________ FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为_______________._______________;
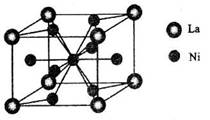
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_______________;
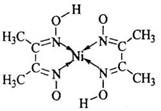
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是 键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;
键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;
②该结构中,氧氢之间除共价键外还可存在_______________;
③该结构中,碳原子的杂化轨道类型有_______________。
-
19-I(6分)下列描述中正确的是
A、CS2为V形的极性分子
B、Cl0— 3 的空间构型为平面三角形
C、SF6中有6对完全相同的成键电子对
D、SiF4和SO2— 3 的中心原子均为sp3杂化
19-Ⅱ(14分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为______________________________;
(2)Ni0、Fe0的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO ________ FeO(填“<”或“>”);
(3)Ni0晶胞中Ni和O的配位数分别为_______________、_______________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_______________;
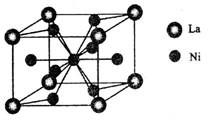

(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是 键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;
键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;
②该结构中,氧氢之间除共价键外还可存在_______________;
③该结构中,碳原子的杂化轨道类型有_______________。
-
(20分)
19-I(6分)下列描述中正确的是
A、CS2为V形的极性分子
B、Cl0— 3 的空间构型为平面三角形
C、SF6中有6对完全相同的成键电子对
D、SiF4和SO2— 3 的中心原子均为sp3杂化
19-Ⅱ(14分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为______________________________;
(2)Ni0、Fe0的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO ________ FeO(填“<”或“>”);
(3)Ni0晶胞中Ni和O的配位数分别为_______________、_______________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_______________;
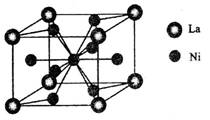
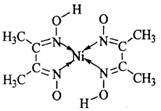
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是 键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;
键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;
②该结构中,氧氢之间除共价键外还可存在_______________;
③该结构中,碳原子的杂化轨道类型有_______________。
-
下列描述中正确的是 ( )
A.CS2为V形的极性分子
B.ClO3—的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4的中心原子为sp3杂化,SO32—的中心原子为sp2杂化
-
I下列描述中正确的是______
A、CS2为V形的极性分子
B、Cl03- 的空间构型为平面三角形
C、SF6中有6对完全相同的成键电子对
D、SiF4和SO32- 的中心原子均为sp3杂化
Ⅱ金属镍及其化合物在合金材料以及催化剂等方面应用广泛.请回答下列问题:
(1)Ni原子的核外电子排布式为______;
(2)Ni0、Fe0的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO______ FeO(填“<”或“>”);
(3)Ni0晶胞中Ni和O的配位数分别为______、______;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示.该合金的化学式为______;
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示.
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是______,氮镍之间形成的化学键是______;
②该结构中,氧氢之间除共价键外还可存在______;
③该结构中,碳原子的杂化轨道类型有______.
-
下列描述中正确的是( )
A.σ键一定比π键强度大
B.AB3型的分子空间构型一定为平面三角形
C.不同元素组成的多原子分子内的化学键一定是极性键
D.利用手性催化剂合成可得到一种或主要得到一种手性分子
-
下列描述中正确的是
A.ClO3-的空间构型为平面三角形
B.SiF4 和 SO32-的中心原子均为 sp3 杂化
C.在所有的元素中,氟的第一电离能最大
D.C2H5OH 分子中共含有 8 个极性键,1 个 π 键
-
下列说法正确的是 ( )
A.某微粒空间构型为平面三角形,则中心原子一定是sp2杂化
B.某微粒空间构型为V形,则中心原子一定有孤电子对
C.某微粒空间构型为三角锥形,则该微粒一定是极性分子
D.某微粒空间构型为正四面体,则键角一定是109°28’
-
下列有关说法不正确的是
A.SO42-的空间构型是正四面体形
B.CS2分子中各原子均达8电子稳定结构
C.CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
D.H2O2分子是既含极性键又含非极性键的非极性分子
-
三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型的叙述,不正确的是( )
A.PCl3分子中的三个共价键的键长、键角都相等
B.PCl3分子中的P—Cl键属于极性共价键
C.PCl3分子中三个共价键的键能均相等
D.PCl3是非极性分子

键,碳氮之间的共价键类型是______________,氮镍之间形成的化学键是_______________;




