-
铜是生命必要的元素,也是人类最早使用的金属之一,西汉时期《淮南万毕术》里就有“曾青得铁,则化为铜”的记载,曾青可能是碳酸铜一类物质,把其溶于酸中得溶液,当把铁粉投入此溶液即可得铜。
(1)根据学过的化学知识,写出该过程的离子方程式:________。
(2)在化学反应中,铜元素可表现为0、+1、+2。Cu2+ 的未成对电子数有______个,向硫酸铜溶液中加入过量的氨水可以得到 [Cu(NH3)4]SO4 溶液,[Cu(NH3)4]2+的结构简式为___。
(3)向[Cu(NH3)4]SO4 水溶液中通入SO2 气体至溶液呈微酸性,析出白色沉淀CuNH4SO3。反应化学方程式为 _____________。
(4)CuNH4SO3 与足量的硫酸混合并微热,得到金属Cu等物质,本法制得的Cu呈超细粉末状,有重要用途,写出该反应的离子方程式________,若该反应在密闭容器中进行,且酸量充足,计算反应物中Cu元素变成超细粉末Cu的转化率_______,理由是__________。
高二化学综合题中等难度题查看答案及解析
-
铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。请完成(1)~(3)题:
(1)在西汉古籍中曾有记载:曾青得铁则化为铜[即曾青(CuSO4)与铁反应生成铜]。试写出该反应的化学方程式: _____________________________。
(2)铜器表面有时会生成铜绿,请写出生成铜绿的化学方程式:____________________________。
这层铜绿可以用化学方法除去,试写出除去铜绿而不损伤器物的化学方程式: _________________________。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币。(铜的熔点是1 183.4 ℃,铁的熔点是1 534.8 ℃)_________________ ___________。
高二化学填空题中等难度题查看答案及解析
-
早在西汉时期就有记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱,要加快该化学反应的速率,所采取的下列措施无效的是( )
A.增大硫酸铜的浓度 B.提高反应的温度
C.增大压强 D.用铁粉代替铁片
高二化学单选题简单题查看答案及解析
-
有A、B、C、D四种元素,A元素的原子的所有能级具有相同的电子数,由B元素形成的单质在常温常压为易挥发的液体,可从海水是提取,C及其合金是人类最早使用的金属材料。D与A位于同一主族,是构成地球上矿物质的主要元素。请回答下列问题:
(1)元素A能形成多种单质,其中的一种单质能用作电极、润滑剂与制造铅笔等。A与D所形成的化合物属于 晶体,其中心原子是以 杂化成键;
(2)B的核外电子排布式为 ,
(3)向含有C的硫酸盐中逐滴滴加氨水,所观察到的现象是 ;再向上述溶液中加入乙醇,有 ;原因是 ;
(4)A的氢化物比D的氢化物相比,熔点高是的 (填化学式),理由是
(5)下列说法正确的是( )
a.晶体析出规则是晶格能高的晶体最后析出
b.铜型和钾型都是密置层堆积方式
c.在干冰晶体中,每一个CO2周围有12个紧邻的CO2分子
d.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
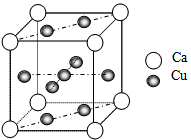
(6)下图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为_____________,已知两个最近的Ca原子之间的距离为apm,则该合金的密度为_____________g/cm3,(用含NA和a的代数式表示)。
高二化学推断题困难题查看答案及解析
-
铜是生物体必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)写出铜与稀硝酸反应的化学方程式:
。
(2)为了保护环境和节约资源,通常先用H2O2和稀硫酸的混合溶液溶出废旧印刷电路板中的铜,最终实现铜的回收利用。写出溶出铜的离子方程式: 。
(3)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S
6Cu+SO2,该反应的还原剂是 ;当生成19.2 g Cu时,反应中转移的电子为 mol。
(4)铜在潮湿的空气中能发生吸氧腐蚀而生锈,铜锈的主要成分为Cu2(OH)2CO3(碱式碳酸铜)。试写出上述过程中负极的电极反应式: 。
(5)研究性学习小组用“间接碘量法”测定某试样中CuSO4·5H2O(不含能与I-反应的氧化性杂质)的含量。取a g试样配成100 mL溶液,每次取25.00 mL,滴加KI溶液后有白色碘化物沉淀生成。写出该反应的离子方程式: 。继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫代硫酸钠标准溶液滴定,发生反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6,平均消耗c mol/L的Na2S2O3溶液V mL。则试样中CuSO4·5H2O的质量分数为 。
高二化学填空题困难题查看答案及解析
-
下列有关说法不正确的( )
A.无单质参加的化合反应有可能是氧化还原反应
B. Al既能溶于强酸,又能溶于强碱,所以说明“Al既有金属性,又有非金属性”
C.青铜是人类在生产生活中使用最早的合金
D.硅在自然界中只以化合态形式存在
高二化学选择题中等难度题查看答案及解析
-
铜合金以纯铜为基体加入一种或几种其他元素所构成的合金,是人类使用最早的金属材料。
(1)电解精炼铜的实验中使用的粗铜含有Cu和少量的Zn、Ag、Au、Cu2Te及其他化合物,请写出电解精炼铜时,阳极发生的电极反应式__________、______________。
(2)从粗铜精炼的阳极泥(主要含有Cu2Te)中提取粗碲的一种工艺流程如图:(已知TeO2是两性氧化物,微溶于水,易溶于强酸和强碱)
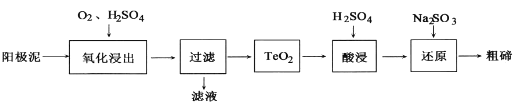
①“氧化浸出”时为使碲元素沉淀充分应控制溶液的pH为4.5~5.0,生成TeO2沉淀。如果H2SO4过量,溶液酸度过大,将导致碲沉淀不完全,原因是_____.
②“过滤”用到的玻璃仪器有____。
③“还原”时发生的离子方程式是________。
④判断粗碲洗净的方法是_________。
⑤在滤液中逐滴加入氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色的透明溶液。写出此蓝色沉淀溶解的离子方程式_______。根据以上实验判断NH3和H2O与Cu2+的配位能力:NH3_____H2O(填“>”或“=”或“<”)。
高二化学工业流程困难题查看答案及解析
-
[化学-选修3:物质结构与性质]
铁铜是人类最早大规模使用的金属,它们的化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)铁元素在周期表中的位置是________,铜的基态原子核外电子排布式为__________,元素铁与铜的第二电离能分别为:ICu="1958" kJ·mol-1、IFe="1561" kJ·mol-1,ICu比IFe大得多的原因是_______。
(2)二茂铁[Fe(C5H5)2],橙色晶型固体,有类似樟脑的气味,抗磁性。熔点172.5~173℃,100℃以上升华,沸点249℃。据此判断二茂铁晶体类型为______________。
(3)蓝矾(CuSO4·5H2O)的结构如下图所示:
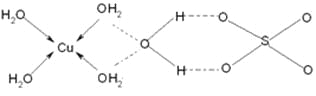
图中虚线表示_____________,SO42-的立体构型是__________,其中S原子的杂化轨道类型是___________;O原子的价电子排布图为__________________。
(4)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为___________。
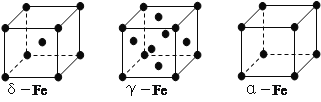
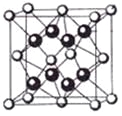
(5)某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,该晶体中原子之间的作用力是_______________。氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构(晶胞结构如右图)相似,该晶体储氢后的化学式为______________。
高二化学综合题中等难度题查看答案及解析
-
铜是人类最早发现并广泛使用的一种金属。回答下列问题:
(1)CuFeS2是其中铜的主要存在形式。CuFeS2中存在的化学键类型是_______。其组成的三种元素中电负性较强的是 _______。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是____,中心原子杂化类型为____。
②X的沸点比水低的主要原因是___________。
(3)[Cu(NH3)4]2+中,提供孤对电子的是________。Cu(NH3)2Cl2有两种同分异构体,其中一种可溶于水,则此种化合物是________(填“极性”或“非极性”)分子,由此推知 [Cu(NH3)4]2+的空间构型是________。
(4)某镍白铜合金的立方晶胞结构如图所示。
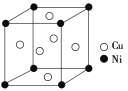
①晶胞中铜原子与镍原子的数量比为________。
②若合金的密度为d g·cm-3,晶胞参数a=________nm。(设NA代表阿伏加德罗常数)
高二化学综合题中等难度题查看答案及解析
-
我国早在西汉成书的《淮南万毕术》里就有“曾青得铁则化为铜”的记载.曾青又有空青、白青、石胆、胆矾等名称,其实都是天然的硫酸铜.
(1)写出“曾青得铁则化为铜”的离子方程式________.
(2)理论上讲,任何自发的氧化还原反应都可以设计成原电池.若根据上述反应设计成原电池,则该电池的负极材料是________,发生________反应(选填“氧化”或“还原”),电解质溶液是________,正极上发生的电极反应为:________.
(3)若导线上转移电子1mol,则生成铜________克.
高二化学填空题中等难度题查看答案及解析