-
某元素基态原子失去3个电子后,3d轨道半充满,其原子序数为( )
A. 24 B. 25 C. 26 D. 27
高二化学选择题中等难度题查看答案及解析
-
某元素基态原子失去3个电子后,3d轨道半充满,其原子序数为( )
A. 24 B. 25 C. 26 D. 27
高二化学单选题中等难度题查看答案及解析
-
4p轨道电子排布达到半充满的元素,其原子序数是
A. 15 B. 33 C. 35 D. 51
高二化学选择题中等难度题查看答案及解析
-
某主族元素的原子,M 层上有一个半充满的亚层(即该亚层的每个轨道只有1个电子),这种原子的质子数
A. 只能是7 B. 只能是15 C. 是11或15 D. 是11或13
高二化学单选题简单题查看答案及解析
-
下列元素的最高价氧化物对应的水化物酸性最强的是
A.原子的L电子层p轨道只填了两个电子的元素
B.外围电子排布式为3s23p2的元素
C.第三周期有7个价电子的元素
D.3p轨道电子半充满的元素
高二化学单选题中等难度题查看答案及解析
-
(17分)(1)第四周期元素的基态原子中,4p轨道半充满的是________,3d轨道半充满的是________,4s轨道半充满的是。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是轨道上的电子,其电子云在空间有伸展方向;元素X的氢化物的电子式是________。元素Y的原子最外层电子排布式为nsn—1npn+1,元素Y的氢化物的结构式________,Y的电负性比X________(填大、小)。在X的单质分子中,X的原子之间存在着______个σ键和______个π键。X分子中X与X形成键的键长比白磷(P4)分子中磷磷键的键长________(填长或短);X分子中的键能比白磷(P4)分子中的键能________(填大或小)
(3)氯化溴(BrCl)的化学性质类似于卤素单质,氯化溴的电子式是________,它是由________键(填σ键或π键)形成的。氯化溴和水反应生成了一种三原子分子,该分
子的电子式为________。氯化溴中溴显________价,原因是________
高二化学填空题简单题查看答案及解析
-
X、Y、Z、W、Q、M六种元素均为前四周期元素,X的原子半径是所有元素中最小的;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;Z基态原子的2p原子轨道为半充满状态;W的原子最外层电子数是内层的3倍;Q基态原子的3p原子轨道上有4个电子;M元素的原子序数为24。
(1)写出M基态原子的核外电子排布式_________。
(2)Y、Z元素的某些氢化物的分子中均含有18个电子,其中沸点较高的是_____(填分子式);Y、Z 的这些氢化物的沸点相差较大的主要原因是_______。
(3)木精(分子组成为YX4W)是一种有毒化合物,极易溶于水。木精极易溶于水的主要原因是木精分子与水分子间可形成分子间氢键,请画出在木精水溶液中氢键的图示:_____(以“A-H…B”的形式表示)。
(4)比较W、Q的简单气态氢化物的热稳定性并从键能的角度加以解释:_______。
(5)ZX3中Z原子的杂化方式为_______,空间构型为________。
高二化学综合题中等难度题查看答案及解析
-
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。
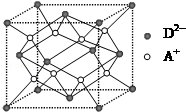
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
高二化学填空题简单题查看答案及解析
-
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B﹣少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+与D2﹣离子数之比为2:1.请回答下列问题:
(1)A元素形成的晶体属于A2密堆积型式,则其晶体内晶胞类型应属于 (填写“六方”、“面心立方”或“体心立方”).
(2)B﹣的价电子排布图为 ,在CB3分子中C元素原子的原子轨道发生的是 杂化.
(3)C的氢化物的空间构型为
(4)B元素的电负性 D元素的电负性(填“>”、“<”或“=”);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱: .
(5)如图所示是R形成的晶体的晶胞,设晶胞的棱长为 a cm.试计算R晶体的密度为
g/cm3 .(阿伏加德罗常数用 NA表示)
高二化学填空题简单题查看答案及解析
-
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数。化合物R是由A、D两元素形成的离子化合物,其中A+阳离子与Dn-阴离子数之比为2∶1。请回答下列问题:
(1)B-的电子排布式为______________,在CB3分子中C元素原子的原子轨道发生的是______杂化。
(2)C的氢化物的空间构型为________________,其氢化物在同族元素所形成的氢化物中沸点最高的原因是__________________________________________________________。
(3)B元素的电负性____D元素的电负性(填“>”、“<”或“=”),用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:________________________________。
(4)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm。 试计算R晶体的密度为_________________。(阿伏加德罗常数用NA表示)

高二化学综合题中等难度题查看答案及解析