-
X、Y、Z、W、Q、M六种元素均为前四周期元素,X的原子半径是所有元素中最小的;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;Z基态原子的2p原子轨道为半充满状态;W的原子最外层电子数是内层的3倍;Q基态原子的3p原子轨道上有4个电子;M元素的原子序数为24。
(1)写出M基态原子的核外电子排布式_________。
(2)Y、Z元素的某些氢化物的分子中均含有18个电子,其中沸点较高的是_____(填分子式);Y、Z 的这些氢化物的沸点相差较大的主要原因是_______。
(3)木精(分子组成为YX4W)是一种有毒化合物,极易溶于水。木精极易溶于水的主要原因是木精分子与水分子间可形成分子间氢键,请画出在木精水溶液中氢键的图示:_____(以“A-H…B”的形式表示)。
(4)比较W、Q的简单气态氢化物的热稳定性并从键能的角度加以解释:_______。
(5)ZX3中Z原子的杂化方式为_______,空间构型为________。
高二化学综合题中等难度题查看答案及解析
-
(15分)
Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增。已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,Q、R两种元素组成的原子个数比为1:1的化合物N是中学化学中常见的有机溶剂;
⑤Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同。
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)化合物M的空间构型为________ ,其中心原子采取________杂化;化合物N在固态时的晶体类型为________。
(2)R、X、Y三种元素的第一电离能由小到大的顺序为________;
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为________(写分子式)
(4)由R、X、Y三种元素组成的RXY-离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物质。该反应的离子方程式为________。
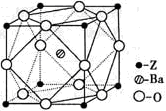
(5)Z原子基态时的外围电子排布式为________;Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个Z原子等距离且最近的氧原子数为________
高二化学填空题简单题查看答案及解析
-
已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大。元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同。
请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
(1)Y、Z、W元素的第一电离能由大到小的顺序是 。
(2)K的电子排布式是 。
(3)Y、Z元素的某些氢化物的分子中均含有18个电子,则Y的这种氢化物的化学式是 ;Y、Z的这些氢化物的沸点相差较大的主要原因是 。
(4)若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合物分子中Y原子轨道的杂化类型是 ;1 mol该分子中含有σ键的数目是 。
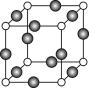
(5)Z、K两元素形成的某化合物的晶胞结构如右图所示,则该化合物的化学式是 ,Z原子的配位数是 。
高二化学填空题中等难度题查看答案及解析
-
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。
已知:①Q为元素周期表中原子半径最小的元素;②R的基态原子中电子占据三种能量不同的能级,且每种能级中的电子总数相同;③Y的基态原子的核外成对的电子数是未成对的电子数的3倍;④Z基态原子有六个未成对电子。用对应的元素符号或化学式回答下列问题:
(1)R、X、Y的第一电离能由大到小的顺序为____________________。
(2)Q元素在元素周期表中属于____区,与Y元素同族的第四周期元素的价电子排布式为______。
(3)RY2的电子式为________________,Z3+的离子结构示意图为____________。
(4) 由Y、Z两种元素组成的Z2Y72-离子在酸性条件下可与乙醇反应,生成乙酸、Z3+等物质。该反应的离子方程式为______。
高二化学推断题困难题查看答案及解析
-
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。
已知:①Q为元素周期表中原子半径最小的元素;②R的基态原子中电子占据三种能量不同的能级,且每种能级中的电子总数相同;③Y的基态原子的核外成对的电子数是未成对的电子数的3倍;④Z基态原子有六个未成对电子。用对应的元素符号或化学式回答下列问题:
(1)R、X、Y的第一电离能由大到小的顺序为____________________。
(2)Q元素在元素周期表中属于____区,与Y元素同族的第四周期元素的价电子排布式为______。
(3)RY2的电子式为________________,Z3+的离子结构示意图为____________。
(4) 由Y、Z两种元素组成的Z2Y72-离子在酸性条件下可与乙醇反应,生成乙酸、Z3+等物质。该反应的离子方程式为______。
高二化学推断题困难题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1 : 1的化合物N是常见的有机溶剂。
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为____________,属于___________分子(填“极性”或“非极性”),E的基态原子的外围电子排布式为____________。
(2)B、C、D三种元素
的第一电离能由小到大的顺序为____________。
(3)C元素形成含氧酸酸性强弱:HNO3____________H
NO2(填“>”或“<”)NO3—的空间构型是___________,NO2—中心原子的杂化方式为___________
(4)下列叙述正确的是____________(填序号)。
A. M是极性分子,N是非极性分子
B. M和BD2分子中的中心原子均采用sp2杂化
C. N分子中含有6个σ键和1个大π键
D. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5)已知:①E的一种氧化物Q,其晶胞结构如图所示:
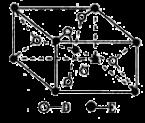
①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECl4和BD气体的热化学方程式:____________________
高二化学填空题极难题查看答案及解析
-
已知A、B、C、D、E、F、G七种元素的原子序数依次递增,前四种元素为短周期元素
位于元素周期表s区,电子层数与未成对电子数相等;B基态原子中电子占据三种能量不同的原子轨道,且每轨道中的电子总数相同;D原子核外成对电子数为未成对电子数的3倍;F位于第四周期d区,最高能级的原子轨道内只有2个未成对电子;E的一种氧化物具有磁性;C与G同主族。
(1)
基态原子的价电子轨道排图为______,B2A2的电子式为_______,CD3-的空间构型为______ .
(2)F(BD)n的中心原子价电子数与配体提供电子总数之和为18(1个BD分子可提供的电子数为2),则
______
根据等电子原理,B、D 分子内
键与
键的个数之比为______ .
(3)FXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为
,若晶体中的F分别为F2+、F3+,此晶体中F2+与F3+的最简整数比为______ .
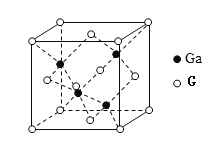
(4)G元素与Ga可形成原子晶体GaG,其晶胞结构如图所示,密度为
,Ga和G的摩尔质量分别为M1g·mol-1和M2g·mol-1原子半径分别为r1pm和r2pm,阿伏伽德罗常数值为
,则该晶胞中原子的体积占晶胞体积的百分率为______.(写出用M1、和M2、r1、r2、ρ表示的计算式)
高二化学综合题困难题查看答案及解析
-
已知X、Y、Z、W、R五种元素均位于周期表的前四周期,且原子序数依次增大。元素X的基态原子中电子占据了三种能量不同的原子轨道,且成对电子数是未成对电子数的2倍;元素Y与W同主族,且Y是地壳中含量最多的元素;Z基态原子有12种不同运动状态的电子;元素R基态原子最外层只有1个电子且内层电子全充满。
请回答下列问题:(答题时,X、Y、Z、W、R用所对应的元素符号表示)
(1)基态Y原子的轨道式表示式为
___。
(2)元素Y、W均可形成含18个电子的氢化物,其中Y的氢化物沸点较高,原因是___;
(3)元素Z与同周期相邻两元素第一电离能由高到低的顺序为___。
(4)元素R在周期表中位于___区,R分别与Y、W形成离子化合物R2Y和R2W,其中熔点较高的为___。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)4]2+,在配离子中与R2+形成配位键的原子是___。
(6)X的一种单质(相邻原子间通过共价键形成空间网状结构)、XY2、WY2、ZW对应的晶体熔沸点由高到低的顺序为___。
高二化学推断题中等难度题查看答案及解析
-
【化学——选修3物质结构与性质】已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E是第四周期d区原子序数最大的元素,F+的最外层电子排布全充满。请回答下列问题:
(1)写出E的价层电子排布式 。
(2)A、B、C、D电负性由小到大的顺序为________(填元素符号)。
(3)E(BD)4为无色或黄色挥发性剧毒液体,熔点-19.3℃,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,该晶体的类型为 ,E与BD之间的作用力为 。
(4)①写出一种与BD32-互为等电子体的分子的化学式 。
②含F2+的溶液与K2SO4、氨水反应可得到化合物 [F(NH3)4]SO4。1 mol配合物离子[F(NH3)4]2+中含σ键的数目为 。
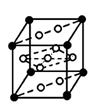
③ E元素与镧(La)元素的合金可做储氢材料,该晶体的晶胞如图所示,晶胞中心有一个E原子,其他E原子都在晶胞面上,则该晶体的化学式为 ;已知该合金的摩尔质量为M g•mol-1,晶胞参数为a pm,用NA表示阿伏伽德罗常数,则该晶胞的密度为 g.cm-3。
高二化学推断题简单题查看答案及解析
-
T、X、Y、Z、Q、R、P、W为周期表前四周期元素,原子序数依次递增,其相关信息如表:
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是______(用元素符号表示,下同).元素 相 关 信 息 T T原子所处的周期数、族序数分别与其原子序数相等 X X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 Z Z可形成Z2、Z3两种气态单质 Q 在该元素所在周期中,Q的基态原子的第一电离能最小 R R的离子为单核离子,且离子半径是与其具有相同电子层结构离子中半径最小的 P Z是P不同周期的邻族元素;R和P的原子序数之和为30 W W的一种核素的质量数为56,中子数为30
(2)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中σ键和π键的个数比为______.
(3)将amolQ单质与bmolR单质组成的固体混合物投入到足量的水中,若固体完全溶解最终得到澄清溶液,则同时产生的气体的物质的量为______mol(用a、b表示);当a=b时,写出反应的离子方程式______.
(4)Y2T4分子中Y原子轨道的杂化类型为______.Y2T4用亚硝酸氧化可生成另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977.写出Y2T4与亚硝酸反应的化学方程式______;
(5)YT3的沸点比化合物XT4的高,其主要原因是:______;
(6)P的单质与T、Z形成的既有极性化学键又有非极性化学键共价化合物反应的离子方程式为______.
(7)上述八种元素形成的微粒中的两种可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入0.1mol/L氢氧化钠溶液,随着氢氧化钠溶液的加入,产生沉淀的关系如图,则该复盐的化学式为______.
高二化学解答题中等难度题查看答案及解析