-
某研究性学习小组设想将少量Cl2通入Fe2+和I-的混合溶液,来探究Fe2+和I-的还原性强弱。
【提出假设】
假设1:; 假设2:;
假设3:Fe2+和I-的还原性一样强。
【验证假设】
(1) 利用以下装置进行试验,
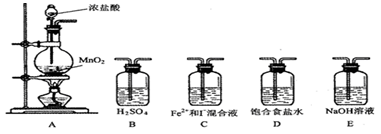
实验必需的装置是:A ________ ________(按氯气流向的顺序用序号书写)
________(按氯气流向的顺序用序号书写)
(2)实验开始后,控制通入少量氯气,通过观察溶液颜色的变化,________(能或不能)判断反应的先后顺序。
(3)请在下表中填写实验步骤及预期现象与结论。
| 实验步骤 | 预期现象与结论 |
| 取少量反应的溶液置于A、B两支试管中; 向A试管中滴加________; 向B试管中滴加________: | ① 若________ ________则假设1成立 ② 若 ________则假设2成立 ③ 若________ ________则假设3成立 |
(4)该实验成功的关键是控制各反应物的用量。该小组称量1.52gFeSO4(M=152g/mol)和1.66gKI(M=166g/mol)固体溶于水中,为了验证上述假设,通入的氯气的体积最多不能超过。(标准状况)
(5)有同学质疑,上述实验只能验证氯气分别与Fe2+和I-反应的速率的大小。并不能证明Fe2+和I-的还原性强弱。于是提出另一验证方案:往KI溶液中滴加________溶液,如果能发生反应,就可证明二者的还原性强弱,该反应的离子方程式是。
-
某研究性学习小组设想将少量Cl2通入Fe2+和I-的混合溶液中,探究Fe2+和I-的还原性强弱。
[提出假设] 假设1:Fe2+还原性比I-强。
假设2:I-还原性比Fe2+强。
[验证假设] 选择几种装置进行实验:
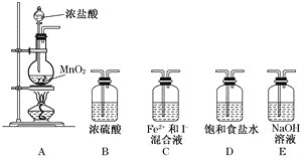
(1)实验必需的装置是A→____________(按Cl2气流方向的顺序填写)。
(2)实验开始后,控制通入氯气的量,当通入少量氯气时,通过观察混合溶液颜色的变化________(填“能”或“不能”)判断反应的先后顺序。
(3)请在下表中写出实验步骤及预期现象和结论________、________、________、________、_______、________。

(4)为了实验成功,必须控制各物质的量。该小组称取1.52g FeSO4固体,同时称取1.66g KI固体,溶于水中配成混合溶液。为了验证上述假设,通入的Cl2体积最多不能超过________L(标准状况)。
[思考与交流]
(5)有同学质疑,上述实验中Cl2量很难控制,无法验证Fe2+和I-反应的先后顺序。于是提出另一方案:往KI溶液中滴入________溶液,如果能发生反应,即可证明I-的还原性强于Fe2+。
-
(4分)某研究性学习小组准备探究氯气与溴化亚铁溶液反应的氧化先后问题。
[提出假设]
假设1:Cl2具有氧化性,在溶液中先氧化Fe2+
假设2:Cl2具有氧化性,在溶液中先氧化Br―
[设计实验方案,验证假设]
(1)只要向通入少量氯气后的溴化亚铁溶液中加__________溶液,通过现象就可以验证是假设1成立,还是假设2成立。
(2)请写出溴化亚铁与等物质的量氯气反应的离子方程式__________
-
某探究学习小组用如下图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
Ⅰ.先向B中的FeCl2溶液(约10 mL)中通入Cl2,
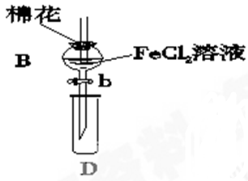
当B中溶液变黄时,停止通气。
Ⅱ.打开活塞b,使约2 mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO2气体。
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为__________,目的是______________________
(2)实验室制备氯气的化学方程式为_______________________________
(3)过程Ⅲ中一定发生反应的离子方程式为___________________过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是____________________
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是____________________
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是___________________。
| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
-
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
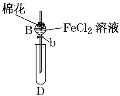
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气。
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO2气体。
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为____________,目的是________________。
(2)实验室制备氯气的化学方程式为______________________。
(3)过程Ⅲ中一定发生反应的离子方程式为______________________,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是_____________________。
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是_______________。
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是______________。
| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
-
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
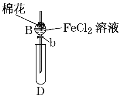
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气。
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO2气体。
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为____________,目的是________________。
(2)实验室制备氯气的化学方程式为______________________。
(3)过程Ⅲ中一定发生反应的离子方程式为______________________,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是_____________________。
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是_______________。
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是______________。
| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
-
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气。
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO2气体。
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
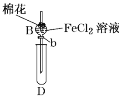
(1)棉花中浸润的溶液为____________,目的是____________________
(2)过程Ⅲ中一定发生反应的离子方程式为________________________________,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是______________________________________。
(3)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是___________________________。
(4)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是______________。
| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
-
Fe2O3和Cu2O都是红色粉末,常用作颜料。某校研究性学习小组通过实验探究一包红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O溶于稀硫酸后生成Cu和CuSO4
提出假设:假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂。
(1)若假设1成立,则实验现象是________。
(2)若滴加 KSCN 试剂后溶液无明显现象,则证明原固体粉末中一定不含Fe2O3。你认为这种说法合理吗?________。(填“合理”或“不合理”)
(3)若固体粉末完全溶解即溶液中无固体存在, 滴加KSCN 试剂时溶液无明显现象, 则证明原固体粉末是________,写出相关反应的离子方程式:________
________。
-
研究性学习小组进行CH4的性质探究实验。
(1)通入高锰酸钾酸性溶液,现象是_____。
(2)在无色玻璃集气瓶中与Cl2混合后光照,现象是____。
(3)为了验证CH4是否具有还原性,某小组设计了如下实验:
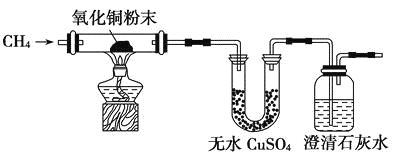
实验过程中还观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为______。
(4)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是_______。
请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图) _______。
-
某化学研究性学习小组设想探究铜的常见化学性质,过程设计如下:
【提出猜想】
问题1:在周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性吗?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性小于Fe3+,Cu+的稳定性也小于Cu2+?
问题3:氧化铜具有氧化性,能与H2、CO发生氧化还原反应,氧化铜能否与氮的氢化物发生氧化还原反应呢?
【实验探究】
I.解决问题1:
(l)需用到药品除 l mol•L-1 CuSO4溶液、稀H2SO4外还需______.
A.Na2SO4溶液 B.NaOH 溶液 C.CuO
(2)配制 l mol•L-1CuSO4溶液250mL,选用的仪器除烧杯、天平、玻璃棒、量筒、胶头滴管外,还有______(填仪器名称).
(3)为达到目的,你认为应进行哪些相关实验?(实验内容和步骤)
①用CuSO4溶液和NaOH溶液制Cu(OH)2; ②______.
II.解决问题2的实验步骤和现象如下:
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80℃~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸或盐酸,得到蓝色溶液,同时观察到试管底还有红色固体存在.根据以上实验及现象:
(l)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:______.
(2)从实验中可得出的结论是:在80℃~100℃时Cu2+稳定,1000℃以上Cu+稳定,在酸性溶液中______稳定(填:Cu2+或
Cu+).
(3)请根据所学的原子结构知识解释在高温下,Cu+稳定的原因?______.
III.解决问题3:
设计如下装置:(夹持装置未画出)
当某种氮的气态氢化物(X)缓缓通过灼热的氧化铜,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的气体Y;将X通入红热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到单质气体Y 0.28g;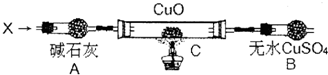
(l)研究小组同学确认燃烧管生成的红色物质是铜而不是氧化亚铜,你认为他们确认的简单方法、预期的现象和结论是:______.
(2)C中发生反应的化学方程式:______ 2Cu+N2+2H2O








