“宏观辨识与微观探析”是化学核心素养之一。
二氧化碳转化为甲醇(CH3OH)的反应微观示意图如下:
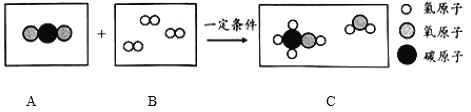
(1)B框中的物质属于_______(选填“混合物”、“化合物”、“氧化物”或“单质”)。
(2)参加反应的A、B分子个数比为_________。
(3)该反应的化学方程式为____________________________________________。
高一化学综合题中等难度题
“宏观辨识与微观探析”是化学核心素养之一。
二氧化碳转化为甲醇(CH3OH)的反应微观示意图如下:

(1)B框中的物质属于_______(选填“混合物”、“化合物”、“氧化物”或“单质”)。
(2)参加反应的A、B分子个数比为_________。
(3)该反应的化学方程式为____________________________________________。
高一化学综合题中等难度题
“宏观辨识与微观探析”是化学核心素养之一。
二氧化碳转化为甲醇(CH3OH)的反应微观示意图如下:

(1)B框中的物质属于_______(选填“混合物”、“化合物”、“氧化物”或“单质”)。
(2)参加反应的A、B分子个数比为_________。
(3)该反应的化学方程式为____________________________________________。
高一化学综合题中等难度题查看答案及解析
甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下。下列说法正确的是( )
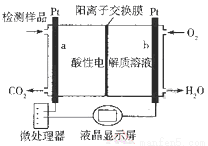
A.该装置为电能转化为化学能的装置
B.a电极发生的电极反应为CH3OH + H2O - 6e- ═ CO2↑ + 6H+
C.当电路中有1 mol e-转移时,正极区n(H+)增加1 mol
D.将酸性电解质溶液改为碱性电解质溶液该测试仪不可能产生电流
高一化学选择题极难题查看答案及解析
甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下。下列说法正确的是( )
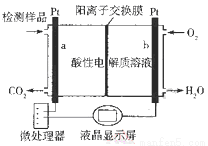
A.该装置为电能转化为化学能的装置
B.a电极发生的电极反应为CH3OH + H2O - 6e- ═ CO2↑ + 6H+
C.当电路中有1 mol e-转移时,正极区n(H+)增加1 mol
D.将酸性电解质溶液改为碱性电解质溶液该测试仪不可能产生电流
高一化学选择题中等难度题查看答案及解析
氨氮废水超标排放是水体富营养化的重要原因,可用以下流程处理:

下列说法正确的是
A.过程I中发生的化学反应属于氧化还原反应
B.过程Ⅱ中,每转化
转移的电子数为6NA
C.过程Ⅲ中CH3OH→CO2,甲醇作还原剂
D.过程Ⅲ中HNO3→N2,转移10mol e-时可生成N2 11.2L(标准状况)
高一化学单选题简单题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法正确的是
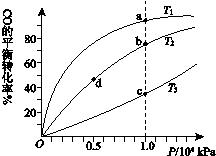
| A.温度: | T1>T2>T3 | |
| B.正反应速率: | υ(a)>υ(c) | υ(b)>υ(d) |
| C.平衡常数: | K(a)>K(c) | K(b)=K(d) |
| D.平均摩尔质量: | M(a)<M(c) | M(b)>M(d) |
高一化学选择题困难题查看答案及解析
高一化学选择题中等难度题查看答案及解析
从宏观现象探究微观本质是重要的化学学科素养。
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
(资料1)亚硫酸(H2SO3)易分解生成SO2和H2O。
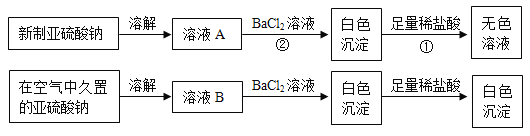
(1)写出上述实验中①、②的离子方程式_________________,_________________。
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有_____________(填化学式),亚硫酸钠在空气中变质体现了亚硫酸钠的_________________性。
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:
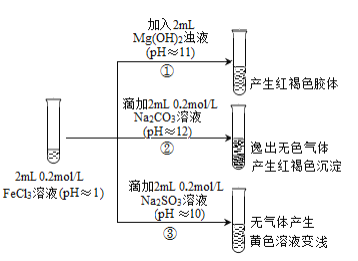
(资料2)含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是_____________________________。
(2)②中逸出的无色气体是_______________________________。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是_______________。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是_________。
(4)由上述实验可知,下列说法正确的是________(填字母)。
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
高一化学实验题困难题查看答案及解析
(6分)
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
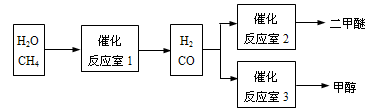
请填空:
(1)写出二甲醚完全燃烧生成二氧化碳和水的化学反应方程式:
__________________________________________________________________。
(2)写出用CO和H2合成甲醇的化学方程式:___________________________________。
(3)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g)CO(g)+3H2(g) 。
将1.0 molCH4和2.0 molH2O通人反应室1(容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率v(CH4)=_______________________。
高一化学填空题中等难度题查看答案及解析
“碳捕捉技术”常用于去除或分离气流中的二氧化碳。
Ⅰ.2017年,中国科学家在利用二氧化碳直接制备液体燃料领域取得了突破性进展,其中用二氧化碳制备甲醇(CH3OH)的反应如下图:
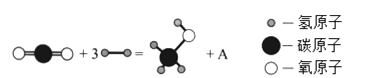
(1)A的化学式为_________。
(2)该反应说明CO2具有___________性(填“氧化”或“还原”)。若有1mol甲醇生成,转移电子的物质的量为_________________mol。
Ⅱ.利用NaOH溶液“捕提"CO2的基本过程如下图(部分条件及物质已略去):
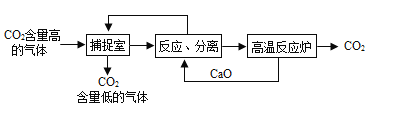
(1)反应分离室中,发生反应的化学方程式分别为CaO+H2O=Ca(OH)2和__________________
(2)高温反应炉中,涉及反应的化学反应类型为_______________________。
(3)整个过程中,可以循环利用物质的化学式为__________________。
高一化学综合题中等难度题查看答案及解析
“碳捕捉技术”常用于去除或分离气流中的二氧化碳。
Ⅰ.2017年,中国科学家在利用二氧化碳直接制备液体燃料领域取得了突破性进展,其中用二氧化碳制备甲醇(CH3OH)的反应如下图:
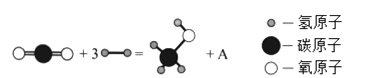
(1)A的化学式为_________。
(2)该反应说明CO2具有___________性(填“氧化”或“还原”)。若有1mol甲醇生成,转移电子的物质的量为_________________mol。
Ⅱ.利用NaOH溶液“捕提"CO2的基本过程如下图(部分条件及物质已略去):
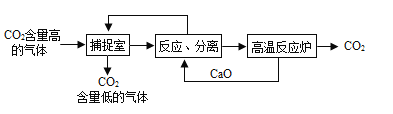
(1)反应分离室中,发生反应的化学方程式分别为CaO+H2O=Ca(OH)2和__________________
(2)高温反应炉中,涉及反应的化学反应类型为_______________________。
(3)整个过程中,可以循环利用物质的化学式为__________________。
高一化学综合题中等难度题查看答案及解析