-
按要求写出下列化学方程式或离子方程式:
(1)硫酸酸化的高锰酸钾与草酸反应的化学方程式:_____________________________。
(2)硫代硫酸钠与稀硫酸反应的化学方程式:____________________________________。
(3)硫酸酸化的碘化钾溶液与氧气反应的离子方程式:________________________。
(4)K2Cr2O7的溶液中K2Cr2O7与K2CrO4转化的离子方程式:____________________。
高二化学填空题中等难度题查看答案及解析
-
Ⅰ.课本中通过向草酸(H2C2O4)溶液中滴加用硫酸酸化高锰酸钾中研究浓度对化学反应速率的影响,请你写出该反应的化学方程式________,该反应不需使用指示剂的原因是________;
Ⅱ.某同学根据课本外界条件对化学反应速率的影响原理,设计了硫代硫酸钠与硫酸反应有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题:
实验
序号 反应温度
(℃) 参加反应的物质
Na2S2O3 H2SO4 H2O
V/mL c/mol•L-1 V/mL c/mol•L-1 V/mL
A 20 10 0.1 10 0.1 0
B 20 5 0.1 10 0.1 5
C 20 10 0.1 5 0.1 5
D 40 5 0.1 10 0.1 5
(1)写出上述反应的离子方程式________
(2)根据你所掌握的知识判断,在上述实验中反应速率最快的可能是________(填实验序号)
(3)在利用比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有 关的各项反应条件.其中:
①能说明温度对该反应速率影响的组合比较是________;(填实验序号)
②A和B、A和C的组合比较所研究的问题是________
③B和C的组合比较所研究的问题是________
(4)教材是利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小的可能原因:
高二化学填空题困难题查看答案及解析
-
某研究小组为了验证反应物浓度对反应速率的影响,选用硫酸酸化的高锰酸钾溶液与草酸H2C2O4溶液在室温下进行反应。实验中所用的草酸为稀溶液,视为强酸。
(1)写出硫酸酸化的高锰酸钾氧化稀草酸溶液的离子方程式__________。
(2)该小组进行了实验I,数据如下。
H2SO4溶液
KMnO4溶液
H2C2O4溶液
褪色时间(分:秒)
1mL 2mol/L
2mL 0.01mol/L
1mL 0.1mol/L
2:03
1mL 2mol/L
2mL 0.01mol/L
1mL 0.2mol/L
2:16
一般来说,其他条件相同时,增大反应物浓度,反应速率___________(填“增大”或“减小”)。但分析该实验数据,得到的结论是在当前实验条件下,增大草酸浓度,反应速率减小。
(3)该小组欲探究出现上述异常现象的原因,在实验I的基础上,只改变草酸溶液浓度进行了实验II,获得实验数据并绘制曲线图如下。
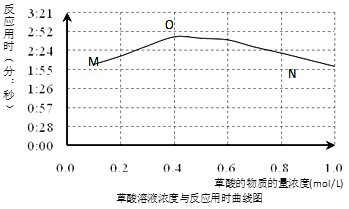
该小组查阅资料获取如下信息,其中能够解释MO变化趋势的是___________。
a
KMnO4与H2C2O4反应是分步进行的,反应过程中生成Mn(VI)、Mn(III)、Mn(IV),最终变为无色的Mn(II)。(括号中罗马数字表示锰的化合价)
b
草酸根易与不同价态锰离子形成较稳定的配位化合物。
c
草酸稳定性较差,加热至185℃可分解。
(4)该小组为探究ON段曲线变化趋势的原因,又进行了实验III,所得数据如下。
H2SO4溶液
Na2SO4固体
KMnO4溶液
H2C2O4溶液
褪色时间(分:秒)
1mL 0.1mol/L
1.9×10-3mol
2mL 0.01mol/L
1mL 0.2mol/L
16:20
1mL 0.5mol/L
1.5×10-3mol
2mL 0.01mol/L
1mL 0.2mol/L
8:25
1mL 1.0mol/L
1.0×10-3mol
2mL 0.01mol/L
1mL 0.2mol/L
6:15
1mL 2.0mol/L
0
2mL 0.01mol/L
1mL 0.2mol/L
2:16
该小组进行实验III的目的是____________________________________________。
(5)综合实验I、II、III,推测造成曲线MN变化趋势的原因________________。
a.当草酸浓度较小时,C2O42-起主要作用,草酸浓度越大,反应速率越小
b.当草酸浓度较小时,H+起主要作用,草酸浓度越大,反应速率越大
c.当草酸浓度较大时,C2O42-起主要作用,草酸浓度越大,反应速率越小
d.当草酸浓度较大时,H+起主要作用,草酸浓度越大,反应速率越大
高二化学实验题中等难度题查看答案及解析
-
某研究小组为了验证反应物浓度对反应速率的影响,选用硫酸酸化的高锰酸钾溶液与草酸溶液在室温下进行反应。实验中所用的草酸为稀溶液,可视为强酸。
(1)将高锰酸钾氧化草酸的离子方程式补充完整。
2MnO4- +_______C2O42- +_____ _____=2Mn2+ +______CO2↑ +_______H2O
(2)该小组进行了实验I,数据如下。
H2SO4溶液
KMnO4溶液
H2C2O4溶液
褪色时间(分:秒)
1mL 2mol/L
2mL 0.01mol/L
1mL 0.1mol/L
2:03
1mL 2mol/L
2mL 0.01mol/L
1mL 0.2mol/L
2:16
一般来说,其他条件相同时,增大反应物浓度,反应速率______。但分析实验数据,得到的结论是______。
(3)该小组欲探究出现上述异常现象的原因,在实验I的基础上,只改变草酸溶液浓度进行了实验II,获得实验数据并绘制曲线图如下。

①用文字描述曲线图表达的信息______。
②该小组查阅资料获取如下信息,其中能够解释MO变化趋势的是______。
a
KMnO4与H2C2O4反应是分步进行的,反应过程中生成Mn(VI)、Mn(III)、Mn(IV),最终变为无色的Mn(II)。(括号中罗马数字表示锰的化合价)
b
草酸根易与不同价态锰离子形成较稳定的配位化合物。
c
草酸稳定性较差,加热至185℃可分解。
(4)该小组为探究ON段曲线变化趋势的原因,又进行了实验III,所得数据如下。
H2SO4溶液
Na2SO4固体
KMnO4溶液
H2C2O4溶液
褪色时间(分:秒)
1mL 0.1mol/L
1.9×10-3mol
2mL 0.01mol/L
1mL 0.2mol/L
16:20
1mL 0.5mol/L
1.5×10-3mol
2mL 0.01mol/L
1mL 0.2mol/L
8:25
1mL 1.0mol/L
1.0×10-3mol
2mL 0.01mol/L
1mL 0.2mol/L
6:15
1mL 2.0mol/L
0
2mL 0.01mol/L
1mL 0.2mol/L
2:16
该小组进行实验III的目的是______。
(5)综合实验I、II、III,推测造成曲线MN变化趋势的原因______。为验证该推测还需要补充实验,请对实验方案进行理论设计______。
高二化学实验题中等难度题查看答案及解析
-
下列离子方程式正确的是
A.硫氰化钾溶液与氯化铁溶液反应:3SCN-+Fe3+
Fe(SCN)3↓
B.氧气通入稀硫酸酸化的KI溶液:O2+2 H2O+4I-=2I2+4OH-
C.酸性高锰酸钾溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+==2Mn2++8H2O+10CO2↑
D.向盐酸中逐滴加入等体积等浓度的碳酸钠溶液:CO32-+2H+==CO2↑+H2O
高二化学选择题简单题查看答案及解析
-
草酸(H2C2O4,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。
(1)硫酸酸化的KMnO4能与Na2C2O4溶液反应生成Mn2+和CO2,该反应的离子方程式为__________;
(2)分别使10 mL pH=3的H2C2O4溶液和100 mL pH=4的H2C2O4溶液全部转化为Na2C2O4,所需等浓度的NaOH溶液的体积为V1和V2,则V1_____V2(填“>”“<”或“=”)
(3)常温下,用0.1000 mol/L NaOH溶液滴定20.00 mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:

①该草酸溶液的物质的量浓度为__________;
②a点所示溶液中各离子的浓度由大到小的顺序为_________________;
(4)已知:某温度时,Ksp(FeC2O4)=2.0×10-7,Ksp(CaC2O4)=2.5×10-9。
①此温度下,CaC2O4饱和溶液的物质的量浓度为________;
②此温度下,向Na2C2O4溶液中加入FeCl2与CaCl2,当两种沉淀共存时,溶液中c(Fe2+):c(Ca2+)=_____。
高二化学综合题中等难度题查看答案及解析
-
下列反应的离子方程式不正确的是( )
A.草酸与酸性高锰酸钾溶液反应:2MnO4-+5C2O42- +16H+= 2Mn2++10CO2↑+8H2O
B.硫代硫酸钠与硫酸的离子方程式: S2O32- + 2H+ = SO2 ↑+ S↓ + H2O
C.稀硝酸中加入少量亚硫酸钠:2H+ + 2NO3- +3 SO32- = 3 SO42-+ NO↑+ 2H2O
D.处理工业废水时Cr(Ⅵ)的转化:Cr2O72—+ SO32-+8H+ = 3 SO42- +2 Cr3++4H2O
高二化学单选题中等难度题查看答案及解析
-
草酸与酸性高锰酸钾反应方程式为2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H20 ,下列说法正确的是( )
A、草酸是氧化剂
B、高锰酸钾是还原剂
C、硫酸可以换成盐酸
D、1molH2C2O4完全反应转移2NA电子
高二化学选择题中等难度题查看答案及解析
-
某实验小组用硫酸酸化的高锰酸钾溶液与草酸溶液反应测定单位时间内生成CO2的量来探究影响反应速率的因素。设计实验方案如表:
实验序号
A溶液
B溶液
①
20mL0.1mol·L-1H2C2O4溶液
30mL0.02mol·L-1酸性KMnO4溶液
②
20mL0.2mol·L-1H2C2O4溶液
30mL0.02mol·L-1酸性KMnO4溶液
(1)图1装置中盛放A溶液的仪器名称是_____,检验如图1装置气密性的方法为_____。
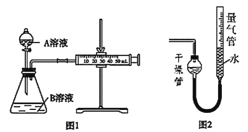
(2)硫酸酸化的高锰酸钾溶液与草酸溶液反应的化学反应方程式为_____。
(3)此实验探究的是_____因素对化学反应速率的影响,若实验②在40s末收集了22.4mLCO2(标准状况下),则在40s内,v(MnO4-)=_____(忽略溶液混合前后体积的变化)。
(4)小组同学将图1的气体收集装置改为图2,实验完毕冷却后,读数时发现量气管液面高于干燥管液面,为得到准确数据,采取的操作是:____。
(5)除了通过测定单位时间内生成CO2的体积来比较反应速率,本实验还可以通过测定____来比较化学反应速率。
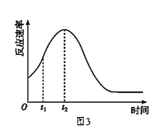
(6)同学们在实验中发现反应速率总是如图3所示,探究t1~t2时间内速率变快的主要原因可能是:____。
A.该反应放热 B.生成的Mn2+起催化作用 C.K2SO4浓度增大
高二化学实验题中等难度题查看答案及解析
-
写出下列反应的离子方程式,并回答相关问题:
(1)草酸使酸性高锰酸钾溶液褪色的离子方程式为____________________________________;紫色溶液的褪色速率先慢后快,然后又变慢,褪色速率加快的原因是__________________________________。
(2)0.1 mol/L硫代硫酸钠与0.1mol/L稀硫酸反应的离子方程式为_____________________________,实验现象为_______________________________。
(3)①H2O2在常温下分解比较慢,但在MnO2催化下可以剧烈分解,并且剧烈放热。写出反应的化学方程式:________________________________。
②实验室常用过氧化钡与稀硫酸反应制取H2O2,写出反应的化学方程式:_______________________。
③Na2O2与水的反应历程实际上是Na2O2先和水反应生成H2O2,然后H2O2再分解产生氧气。②和③的实验说明H2O2保存在酸性溶液中比在碱性溶液中_________(填“稳定”“不稳定”或“一样稳定”),说明_________(填离子符号)能够催化H2O2分解。
高二化学填空题中等难度题查看答案及解析