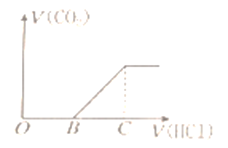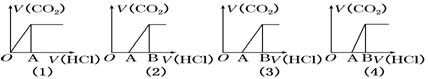-
向某 NaOH 溶液中通入 CO2 气体后得到溶液 M,因 CO2 通入的量不同, 溶液 M 的组成也不同,若向溶液 M 中逐滴加入盐酸,产生的气体体积 V(CO2)与加入盐酸的体积 V(HCl)的关系如图所示。则下列分析与判断 不正确的是(不计CO2溶解)

A. 若 OB=0,则形成溶液的过程中所发生反应的离子方程式为OH-+CO2=HCO3-
B. 若 OB=BC,则溶液 M 为Na2CO3 溶液
C. 若 OB>BC,则溶液 M 中大量存在的阴离子为 CO32-和HCO3-
D. 若 3OB=BC,则溶液 M 中 c(NaHCO3)=2c(Na2CO3)
-
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断不正确的是(不计CO2溶解)

A. 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
-
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断不正确的是(不计CO2溶解)
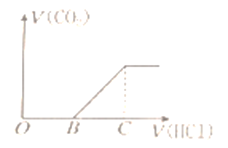
A. 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
-
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断不正确的是(不计CO2溶解)
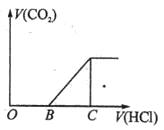
A. 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
-
向某NaOH溶液中通入CO2气体后 得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断正确的是(不计CO2溶解)
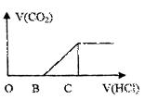
A.若OB=0,则溶液M为Na2CO3溶液
B.若OB=BC,则形成溶液M所发生反应的离子方程式为OH-+CO2 HCO3-
HCO3-
C.若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
D.若OB>BC,则溶液M中大量存在的阴离子为CO32-和HCO3-
-
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如下图所示。则下列分析与判断正确的是(不计CO2的溶解)

A.若OB=0,则溶液M为Na2CO3溶液
B.若OB=BC,则形成溶液M所发生的离子反应方程式为:OH-+CO2=HCO3-
C.若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
D.若OB>BC,则溶液M中大量存在的阴离子为CO32-和HCO3-
-
向NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图。则下列分析正确的是(不计CO2溶解)
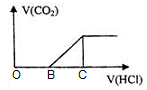
A.若OB=0,则溶液M为Na2CO3溶液
B.若OB=BC,则形成溶液M所发生反应的离子方程式为OH-+CO2 → HCO3-
C.若溶液M中c(NaHCO3)=2c(Na2CO3),则3OB=BC
D.若溶液M中大量存在的阴离子为CO32-和HCO3-,则OB>BC
-
向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(盐酸)的关系有如图所示四种情况,且(2)、(3)、(4)图中分别有OA<AB, OA=AB,OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)( )
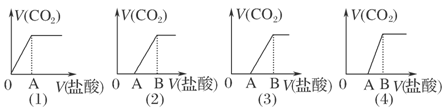
A.M中只有一种溶质的有(1)和(3) B.M中有两种溶质的有(2)和(4)
C.(2)图显示M中c(NaHCO3)>c(Na2CO3) D.(4)图显示M中c(NaHCO3)>c(Na2CO3)
-
向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(盐酸)的关系有如图所示四种情况,且(2)、(3)、(4)图中分别有OA<AB, OA=AB,OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)( )
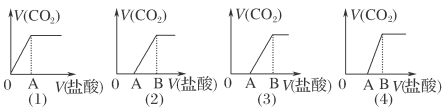
A.M中只有一种溶质的有(1)和(3) B.M中有两种溶质的有(2)和(4)
C.(2)图显示M中c(NaHCO3)>c(Na2CO3) D.(4)图显示M中c(NaHCO3)>c(Na2CO3)
-
向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA﹕AB=2﹕3, OA=AB, OA﹕AB=3﹕2,则下列分析与判断不正确的是(忽略CO2的溶解) ( )
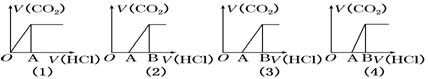
A.M中只有一种溶质的有(1)和(3)
B.M中有两种溶质的有(2)和(4)
C.(2)图显示M中的溶质为NaHCO3和Na2CO3,二者的物质的量之比为2:1
D.(4)图显示M中的溶质为NaOH和Na2CO3,二者的物质的量之比为1:2