-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知 W 的一种核素的质量数为 18,中子数为 10;X 和 Ne 的核外电子数相差 1; 在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。 请回答下列问题:
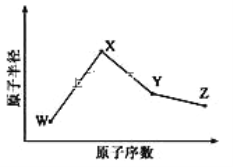
(1)X 元素位于元素周期表中位置为_____________。
(2)X 的单质和 Y 的单质相比,熔点较高的是____________(写化学式) 。 Z 所在族的简单氢化物中,沸点最高的是________(写化学式),原因为_________________________。
(3)W、X、Z 三种元素形成的化合物中化学键类型为________;X2W2的电子式为___________________。
(4)Y 与 Z 形 成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为__________________________。
(5)Z 的氧化物很多,其中一种黄绿色气体 M,其氧含量为 47.41%,可用于水处理, M 在液态和浓缩气态时具有爆炸性 。 M 的化学式为_____________。 M 可与 NaOH 溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,该反应的化学方程式为___________________。
(6)在 25°C、101kPa 下,已知 Y 的简单气态氢化物在氧气中完全燃烧后恢复至原状态, 平均每转移 1mol 电子放热 190kJ, 该反应的热化学方程式为__________________________________。
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化趋势如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期中金属性最强的元素;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法正确的是( )
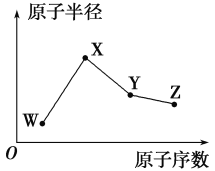
A.对应气态氢化物的稳定性:Y>W
B.对应简单离子的半径:W>Z
C.化合物XZW中既含离子键也含共价键
D.Y的氧化物能与Z的最高价氧化物对应的水化物反应
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化趋势如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期中金属性最强的元素;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法正确的是( )
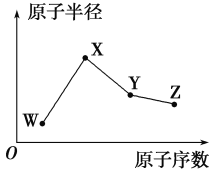
A.对应气态氢化物的稳定性:Y>W
B.对应简单离子的半径:W>Z
C.化合物XZW中既含离子键也含共价键
D.Y的氧化物能与Z的最高价氧化物对应的水化物反应
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知 W 的一种核素的质量数为18,中子数为10;X 和 Ne 的核外电子数相差1; 在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。 请回答下列问题:

(1)X 元素位于元素周期表中位置为____________。
(2)Z 的同族简单氢化物中,稳定性最好的是________(写化学式),原因__________________。
(3)W、X、Z 三种元素形成的化合物中化学键类型为___________;X2W2的电子式为________。
(4)Y 与 Z 形成的化合物YZ4在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为__________________________。
(5)Z 的氧化物很多,其中一种黄绿色气体M,其氧含量为 47.41%,可用于水处理, M 在液态和浓缩气态时具有爆炸性。 M 可与 NaOH 溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,该反应的化学方程式为____________________。
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是( )
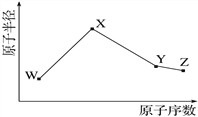
A. 对应简单离子半径:X>W
B. 对应简单气态氢化物的稳定性:Y<Z
C. Y的氧化物能与X的最高价氧化物对应的水化物反应
D. 化合物X2W2既含离子键也含共价键
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是( )

A.对应的简单离子的半径:X<W
B.对应的简单气态氢化物的稳定性:Y<Z
C.元素X、Z和W能形成多种化合物
D.Y的最高价氧化物对应的水化物具有强酸性
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是

A.对应简单离子半径:X<W
B.对应简单气态氢化物的稳定性:Y<Z
C.化合物XZW既含离子键也含共价键
D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子数变化如图所示 已知W的一种核素的质量数为18,中子数为10,X和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强
已知W的一种核素的质量数为18,中子数为10,X和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强 下列说法正确的是( )
下列说法正确的是( )
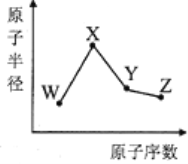
A. 对应简单离子半径:
B. 对应气态氢化物的稳定性
C. 化合物XZW既含离子键,又含共价键
D. Y的氧化物与Z和X的最高价氧化物对应的水化物均能反应
-
(10分)X、Y、W、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10,Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。
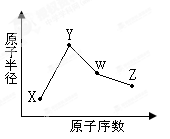
(1)W位于元素周期表中第________周期第________族画出X的阴离子的结构示意图________。
(2)Z的氢化物和溴化氢相比,较稳定的是________(写化学式);Z的氢化物与氟化氢相比,沸点较高的是________(写化学式)。
(3)Y的金属性与Mg的金属性相比,________(写化学式)的金属性强,请用实验证明它们金属性的相对强弱:________。
(4)写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学反应方程式________。
-
(10分)X、Y、W、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10,Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。

(1)W位于元素周期表中第 周期第 族画出X的阴离子的结构示意图 。
(2)Z的氢化物和溴化氢相比,较稳定的是 (写化学式);Z的氢化物与氟化氢相比,沸点较高的是 (写化学式)。
(3)Y的金属性与Mg的金属性相比, (写化学式)的金属性强,请用实验证明它们金属性的相对强弱: 。
(4)写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学反应方程式 。









