-
“氢能”是未来最理想的新能源。
(1)实验测得,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则氢气燃烧的热化学方程式为_____。(填序号)
A.2H2(g)+O2(g)=2H2O(l) ΔH =-142.9 kJ·mol−1
B.H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol−1
C.2H2+O2=2H2O(l) ΔH= 571.6 kJ·mol−1
D.H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ·mol−1
(2)某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤:
① CaBr2+H2O CaO+2HBr
CaO+2HBr
② 2HBr+Hg HgBr2+H2↑
HgBr2+H2↑
③ HgBr2+_______ ________
________
④ 2HgO 2Hg+O2↑
2Hg+O2↑
⑤2H2+O2 2H2O
2H2O
请你根据“原子经济”的思想完成上述步骤③的化学方程式:___________。并根据“绿色化学”的思想评估该方法制H2的主要缺点_________。
(3)利用核能把水分解制氢气,是目前正在研究的课题。如图是其中的一种流程,其中用了过量的碘。

完成下列反应的化学方程式:反应①______________;反应②____________。此法制取氢气的最大优点是______________________。
-
“氢能”是未来最理想的新能源。
(1)实验测得,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则氢气燃烧的热化学方程式为_________。(填序号)
A.2H2 (g)+ O2 (g) 2H2O(l) ΔH =−142.9 kJ • mol−1
2H2O(l) ΔH =−142.9 kJ • mol−1
B.H2 (g)+ O2 (g)
O2 (g) H2O(l) ΔH=−285.8 kJ • mol−1
H2O(l) ΔH=−285.8 kJ • mol−1
C.2H2 + O2 2H2O (l) ΔH= −571.6 kJ • mol−1
2H2O (l) ΔH= −571.6 kJ • mol−1
D.H2 (g)+ O2 (g)
O2 (g) H2O(g) ΔH=−285.8 kJ • mol−1
H2O(g) ΔH=−285.8 kJ • mol−1
(2)某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤:
① CaBr2 +H2O CaO+2 HBr
CaO+2 HBr
② 2HBr+Hg HgBr2 + H2↑
HgBr2 + H2↑
③ HgBr2 +_________ _________
_________
④ 2HgO 2Hg+O2↑
2Hg+O2↑
⑤2H2 + O2 2H2O
2H2O
请你根据“原子经济”的思想完成上述步骤③的化学方程式:___________。并根据“绿色化学”的思想评估该方法制H2的主要缺点:_________。
(3)利用核能把水分解制氢气,是目前正在研究的课题。如图是其中的一种流程,其中用了过量的碘。

完成下列反应的化学方程式:反应①____________________;反应②______________________。此法制取氢气的最大优点是______________________。
-
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为_________。 ③该反应的热化学方程式为___________________。
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________kJ·mol-1
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________kJ·mol-1
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
-
氢气是人类最理想的能源。已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是
A.2H2+O2 2H2O;△H =142.9kJ/mol
B.2H2(g)+O2(g) 2H2O(l);△H =-142.9kJ/mol
C.2H2(g)+O2(g) 2H2O(l);△H =-571.6kJ/mol
D.2H2(g)+O2(g) 2H2O(l);△H = +571.6kJ/mol
-
氢气是人类最理想的能源。已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是:
A.2H2 + O2=2H2O △H= –142.9 kJ/mol
B.2H2(g) + O2(g)=2H2O(l) △H= – 142.9 kJ/mol
C.2H2(g) + O2(g)=2H2O(l) △H= – 571.6 kJ/mol
D.2H2(g) + O2(g)=2H2O(l) △H = + 571.6 kJ/mol
-
氢气是一种理想的绿色能源。
(1)在101kPa下,1 g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为_________________;②写出氢气燃烧热的热化学方程式__________________;
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,己知:
Mg(s)+H2(g)=MgH2(s) △H1=-74.5kJ•mol-1
Mg2Ni (s)+2H2(g)=Mg2NiH4(s) △H2;
Mg2Ni(s)+2MgH2(s)==2Mg(s)+ Mg2NiH4(s) △H3=+84.6 kJ•mol-1。
则△H2=______ kJ•mol-1;
(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的装置(其中电解质溶液为KOH溶液),被称为氢氧燃料电池。该电池的正极是____ (填a或b),负极反应式为________。该电池反应后溶液的pH将________(填“增大”“减小”或“不变”)
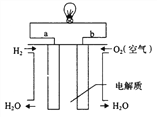
(4)若将上图中的氢氧燃料电池用固体金属氧化物陶瓷作电解质(能够传导O2-),己知正极上发生的电极反应式为:O2+4e-=2O2-则负极上发生的电极反应式为_______;电子从______极(填a或b)流出。该电池工作时,外电路每流过1 mol e-,消耗标况下氧气_____L。
-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是: ( )
A. 2H2(g)+O2(g)===2H2O(l) ΔH =-571.6 kJ/mol
B. 2H2(g)+O2(g)===2H2O(l) ΔH =-142.9 kJ/mol
C. 2H2+O2===2H2O ΔH =-142.9 kJ/mol
D. 2H2(g)+O2(g)===2H2O(l) ΔH =+571.6 kJ/mol
-
氢气是人类最理想的能源。已知在25 ℃、101 kPa下,1 g氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A. 2H2+O2 === 2H2O; ΔH=142.9 kJ·mol-1
B. 2H2(g)+O2(g)===2H2O(l); ΔH=-142.9 kJ·mol-1
C. 2H2(g)+O2(g)===2H2O(l); ΔH=-571.6 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(l); ΔH=571.6 kJ·mol-1
CaO+2HBr
HgBr2+H2↑
________
2Hg+O2↑
2H2O


