-
(1)已知下列热化学方程式:
H2(g)+1/2O2(g)==H2O(l) ΔH=−285.8 kJ·mol−1
H2(g)+1/2O2(g)==H2O(g) ΔH=−241.8 kJ·mol−1
C(s)+ 1/2O2(g)==CO(g) ΔH=−110.5 kJ·mol−1
C(s)+O2(g)==CO2(g) ΔH=−393.5 kJ·mol−1
回答下列问题:
①燃烧10gH2生成液态水,放出的热量为________。
②CO的燃烧热为________。
(2)0.3mol乙硼烷气体(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量,则其热化学方程式为________________________。
(3)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出稀H2SO4溶液与稀NaOH溶液反应的热化学方程式__________________。
(4)已知:2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6 kJ·mol–1
2NO(g)+O2(g)
2NO2(g) ΔH=-113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式____________________。
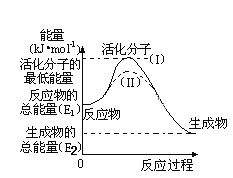
(5)研究活化能对于能源技术的革新有非常重大的实际意义。请认真观察下图,回答问题:
①图中反应的ΔH=_____________kJ/mol(用含有E1、E2代数式表示)。
②已知热化学方程式:H2(g)+1/2O2(g) = H2O(g) ΔH=-241.8kJ/mol,该反应的活化能为167.2kJ/mol,则H2O(g)=H2(g)+1/2O2(g)的活化能为________kJ/mol。
高二化学综合题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l) ΔH =-285.8 kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH =-241.8 kJ/mol
③C(s)+1/2O2(g)=CO(g) ΔH =-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ/mol
回答下列问题:
(1)H2的燃烧热ΔH=_______;C的燃烧热为__________。
(2)燃烧1 g H2生成液态水,放出的热量为_________。
(3)已知CO的燃烧热为283.0 kJ/mol,现有CO、H2和CO2组成的混合气体116.8 L(标准状况),完全燃烧后放出总热量为867.9 kJ,且生成18 g液态水,则混合气体中H2为_________L,CO在混合气体中的体积分数约为_________(精确至小数点后一位)。
高二化学填空题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s) +1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s) +O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,
回答下列问题:(1)上述反应中属于放热反应的是____________。
(2)H2的燃烧热为________________;C的燃烧热为________________。
(3)燃烧10 g H2生成液态水,放出的热量为________________。
(4)写出CO燃烧的热化学方程式__________________________________。
高二化学填空题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+1/2O2(g)
H2O(l) ΔH=−285.8 kJ·mol−1
②H2(g)+1/2O2(g)
H2O(g) ΔH=−241.8 kJ·mol−1
③C(s)+ 1/2O2(g)
CO(g) ΔH=−110.5 kJ·mol−1
④C(s)+O2(g)
CO2(g) ΔH=−393.5 kJ·mol−1
回答下列各问题:
(1)上述反应中属于放热反应的是_______________________。
(2)H2的燃烧热为________
(3)燃烧10 g H2生成液态水,放出的热量为________。
(4)CO的燃烧热为________;其热化学方程式为______________。
高二化学填空题简单题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,
回答下列问题:
(1)上述反应中属于放热反应的是____________。
(2)H2的燃烧热为____________ kJ·mol-1;C的燃烧热为____________ kJ·mol-1。
(3)燃烧10 g H2生成液态水,放出的热量为____________ kJ。
(4)写出CO燃烧的热化学方程式__________________________________。
高二化学填空题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2O(l)=H2(g)+
O2(g) △H=+285.8 kJ/mol
②H2(g)+
O2(g)=H2O(g) △H=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol
④C(s)+
O2(g)=CO(g) △H=-110.5 kJ/mol
⑤C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于吸热反应的是____________________ 。
(2)C的燃烧热为____________________。
(3)燃烧10g H2生成液态水,放出的热量为______________。
(4)写出表示CO燃烧热的热化学方程式:__________________;写出制水煤气的热化学方程式:______________________。
高二化学填空题中等难度题查看答案及解析
-
(10分)已知下列热化学方程式:
①H2O(l)===H2(g)+
O2(g) ΔH=+285.8 kJ/mol
②H2(g)+
O2(g)===H2O(g) ΔH=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ/mol
④C(s)+
O2(g)===CO(g) ΔH=-110.5 kJ/mol
⑤C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于吸热反应的是_____ ___。
(2)C的燃烧热ΔH为______ __。
(3)燃烧10 g H2生成液态水,放出的热量为______ __。
(4)写出CO燃烧的热化学方程式________________________________
写出制水煤气的热化学方程式_____________________________________
高二化学填空题中等难度题查看答案及解析
-
下列热化学方程式或离子方程式正确的是
A.已知H2的标准燃烧热ΔH=-285.8 kJ·mol-1,则用热化学方程式可表示为:H2(g)+1/2O2(g)===H2O(g)ΔH=-285.8 kJ·mol-1
B.NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O===Fe(OH)2↓+2HClO
C.NH4HSO3溶液与足量NaOH溶液共热:NH4++H++2OH-
NH3↑+2H2O
D.用足量KMnO4溶液吸收SO2气体:2MnO4-+5SO2+2H2O===2Mn2++5SO42-+4H+
高二化学单选题困难题查看答案及解析
-
(2015秋•长春校级期末)已知下列热化学方程式:
①H2(g)+
O2(g)═H2O(l)△H=﹣285.8kJ/mol
②H2(g)+
O2(g)═H2O(g)△H=﹣241.8kJ/mol
③C(s)+
O2(g)═CO(g)△H=﹣110.5kJ/mol
④C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)燃烧10g H2生成液态水,放出的热量为
(3)表示CO燃烧热的热化学方程式为
高二化学填空题困难题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+
O2(g)===H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+
O2(g)===H2O(g) ΔH=-241.8 kJ/mol
③C(s)+
O2(g)===CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_____________(填序号)。
(2)H2的燃烧热为_____________,C的燃烧热为_____________。
(3)燃烧10 g H2生成液态水,放出的热量为________。
(4)CO的燃烧热为______________,其热化学方程式为_______________________。
(5)在某温度时,测得0.01 mol•L-1的NaOH溶液的pH为11。该温度下,水的离子积常数Kw =________。
高二化学综合题简单题查看答案及解析