-
Fe2O3与FeS2混合后在无氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2)∶n(Fe2O3)是
A. 1∶2 B. 2∶35 C. 3∶8 D. 1∶16
高二化学单选题简单题查看答案及解析
-
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3.
(1)已知1g FeS2完全燃烧放出7.1kJ热量,则表示FeS2完全燃烧反应的热化学方程式为:______ 2Fe2O3(s)+8SO2(g)△H=-3408kJ/mol高二化学解答题中等难度题查看答案及解析
-
聚合硫酸铁(PFS)是一种高效的无机高分子絮凝剂。某工厂利用经浮选的硫铁矿烧渣(有效成分为Fe2O3 和Fe3O4)制备PFS,其工艺流程如下图所示。
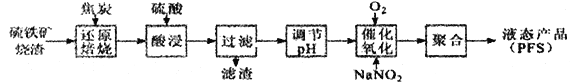
(1)还原焙烧过程中,CO还原Fe3O4生成FeO的热化学方程式为________________________。
已知: Fe3O4(s)+C(s)= 3FeO(s)+CO(g) ΔH1=+191.9kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ·mol-1
C(s)+CO2(g)=2CO(g) ΔH3=+172.5kJ·mol-1
(2)CO是还原焙烧过程的主要还原剂。下图中,曲线表示4个化学反应a、b、c、d达到平衡时气相组成和温度的关系,I、Ⅱ、Ⅲ、Ⅳ分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域。a属于_________(填“吸热反应”或“放热反应”);570℃时,d反应的平衡常数K= ____________。

(3)工业上,还原焙烧的温度一般控制在800℃左右,温度不宜过高的理由是___________________。
(4)若“酸浸”时间过长,浸出液中Fe2+含量反而降低,主要原因是___________________________。
(5)FeSO4溶液在空气中会缓慢氧化生成难溶的Fe(OH)SO4,该反应的离子方程式为_____________________________。“催化氧化”过程用NaNO2作催化剂(NO起实质上的催化作用)时,温度与Fe2+转化率的关系如右图所示(反应时间相同),Fe2+转化率随温度的升高先上升后下降的原因是___________________________________________________。

高二化学综合题中等难度题查看答案及解析
-
(12分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

回答下列问题:
(1)硫铁矿高温焙烧的化学方程式为________; 少量的SO2与NaOH溶液反应的离子方程式为________。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率和________ ,
题问所涉及反应的离子方程式为________。
(3)通氯气氧化时,发生的主要反应的离子方程式为________ ;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________________________(写化学式)。
高二化学填空题中等难度题查看答案及解析
-
以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列叙述不正确的是
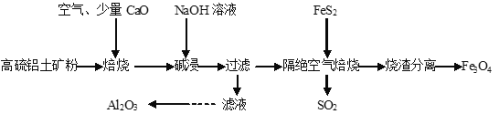
A.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
B.向滤液中通入过量HCl气体、过滤、洗涤、灼烧沉淀可制得Al2O3
C.隔绝空气焙烧时理论上反应消耗的n(FeS2):n(Fe2O3)=1:5
D.烧渣分离可用磁选法
高二化学多选题中等难度题查看答案及解析
-
黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:SO2 + 2Fe3+ + 2H2O→SO
+ 2Fe2+ + 4H+
Cr2O
+ 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O
(1)样品中FeS2的质量分数是(假设杂质不参加反应)________。
(2)若灼烧6 g FeS2产生的SO2全部转化为SO3气体时放出9.83 kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,写出SO3气体转化为H2SO4的热化学方程式:________。
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为,制得98%的硫酸质量为________ t ,SO2全部转化为H2SO4时放出的热量是________ kJ。
高二化学填空题困难题查看答案及解析
-
将a mol氢气和b mol乙烯混合,在一定条件下使它们部分反应生成c mol乙烷,将反应后的混合气体完全燃烧,消耗氧气的物质的量为 ( )
A.(3b+0.5a) mol B.(4b+0.5a) mol
C.(3b+1.5a) mol D.无法判断
高二化学选择题简单题查看答案及解析
-
黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000g样品在空气中充分燃烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00ml。已知:
SO2+Fe3++2H2O=SO42-+Fe2++4H+ Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)样品中FeS2的质量分数 (假设杂质不参加反应)。
(2)若燃烧6gFeS2产生的SO2全部转化为SO3气体时放出9.83kJ热量,产生的SO3与水全部化合生成H2SO4放出13.03kJ热量,写出SO3气体转化为H2SO4的热化学方程式 。
(3)煅烧10t上述黄铁矿,理论上产生SO2的体积(标准状况)为 L,制得98%的硫酸的质量为 t,SO2全部转化为SO3时放出的热量是 kJ。
高二化学填空题简单题查看答案及解析
-
将a mol氢气和b mol乙烯混合,在一定条件下使它们部分反应生成c mol乙烷,将反应后的混合气体完全燃烧,消耗氧气的物质的量为( )
A.(3b+0.5a)mol B.(4b+0.5a)mol C.(3b+1.5a)mol D.无法判断
高二化学选择题中等难度题查看答案及解析
-
把M mol H2和N mol C2H4混合, 在一定条件下使它们一部分发生反应生成W mol C2H6, 将反应后所得的混合气体完全燃烧, 消耗氧气的物质的量为( )
A.M + 3N mol
B.
+ 3N mol
C.
mol D.
mol
高二化学选择题中等难度题查看答案及解析