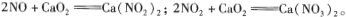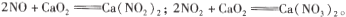-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料。某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。回答下列有关问题。
(背景素材)Ⅰ.NO+CaO2=Ca(NO2)2;2NO2+CaO2=Ca(NO3)2;
II.亚硝酸具有一定的氧化性和还原性,酸性条件下:Ca(NO2)2能将I-氧化为I2;
Ⅲ.I2+2S2O32—=2I-+S4O62—
(制备Ca(NO2)2)该小组设计的制备装置如图所示(夹持装置略去)。
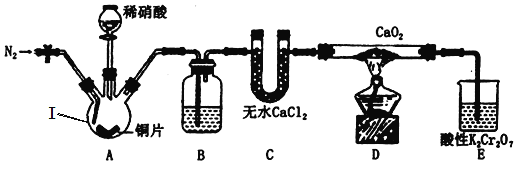
(1)仪器Ⅰ的名称是___________________;B中盛装的试剂是____________________。
(2)制备过程有关操作如下,正确顺序为_______、c、_______、_______、_______、_______。
a.向装置中通入N2 b.向仪器Ⅰ中滴加稀硝酸 c.点燃酒精灯 d.熄灭酒精灯 e.停止通入N2 f.关闭分液漏斗旋塞
(3)装置E中,酸性K2Cr2O7溶液可将剩余的NO氧化成NO3—,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为__________________________。
(4)整个过程持续通N2的作用是______________、_____________、____________。
(测定Ca(NO2)2的纯度)该小组测定产品中Ca(NO2)2纯度的方法如下:a.称取mg产品、溶解、定容至250mL;b.移取25.00mL溶液于锥形瓶中,加入过量的V1 mLc1mol/L的KI溶液并酸化;c.以淀粉为指示剂,用c2mol/L的Na2S2O3溶液滴定。进行三次平行实验,消耗标准液体积平均值为V2 mL。
(5)测定过程所需仪器在使用前必须检查是否漏液的有______________________。
(6)该产品中Ca(NO2)2的质量分数为_____________________。
-
亚硝酸钙[ Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝
酸钙,实验装置如图所示(夹持装置略去)。
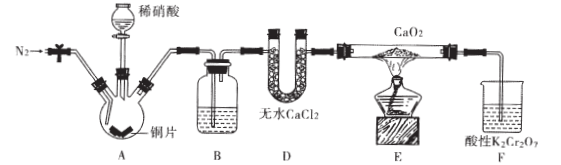
已知: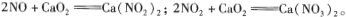
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因是____。
(2)仪器D的名称是_;B中盛放的试剂是____。
(3)装置F中,酸性K2Cr2O7溶液可将剩余的NO氧化成NO3-,溶液由橙色变为绿色
(Cr3+),发生反应的离子方程式是____。
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体。设计
实验证明E中有亚硝酸钙生成____。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、N02)反应,既能净化尾气,又能获得
应用广泛的Ca(NO2)2,反应原理为Ca(OH)2+NO +N02=Ca(N02)2+H2O。
①若n( NO):n(NO2)>l:l,则会导致 :
②若n( NO):n( NO2)<l l,则会导致 。
-
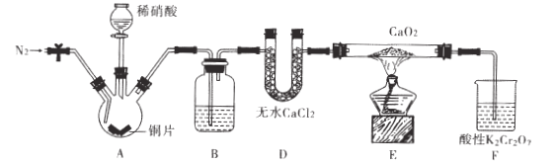
亚硝酸钙[ Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝
酸钙,实验装置如图所示(夹持装置略去)。
已知: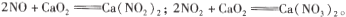
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因是____。
(2)仪器D的名称是_;B中盛放的试剂是____。
(3)装置F中,酸性K2Cr2O7溶液可将剩余的NO氧化成NO3-,溶液由橙色变为绿色
(Cr3+),发生反应的离子方程式是____。
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体。设计
实验证明E中有亚硝酸钙生成____。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、N02)反应,既能净化尾气,又能获得
应用广泛的Ca(NO2)2,反应原理为Ca(OH)2+NO +N02=Ca(N02)2+H2O。
①若n( NO):n(NO2)>l:l,则会导致 :
②若n( NO):n( NO2)<l l,则会导致 。
-
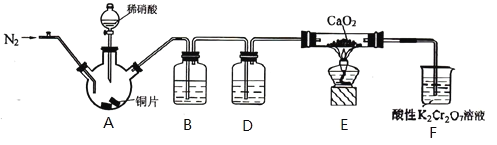
亚硝酸钙[Ca(NO2 )2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备 Ca(NO2 )2,实验装置如图所示(夹持装置已略去)。已知:2NO +CaO2 ═ Ca (NO2)2; 2NO2 +CaO2═Ca(NO3)2。
下列说法不正确的是
A. 实验开始时,先通一会儿氮气再加入稀硝酸
B. 装置 B、D 中的试剂可分别为水和浓硫酸
C. 装置 F 中酸性 K2Cr2O7 溶液的作用是吸收多余的、未反应的氮氧化物
D. 将铜片换成木炭也可以制备纯净的亚硝酸钙
-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去)。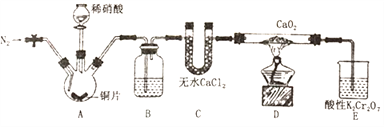
已知:2NO+CaO2=Ca(NO2)2;2NO2+CaO2 =Ca(NO3)2。
请回答下列问题:
a.向装置中通入N2;b.向三颈烧瓶中滴加稀硝酸;c.点燃酒精灯;d.熄灭酒精灯;e.停止通入氮气;f.关闭分液漏斗旋塞
(1)上述操作的正确排序为____、c、____ f、____、______。
(2)B中盛放的试剂是_____________,作用是除去________(填化学式)。
(3)装置E中,酸性K2Cr2O7溶液的作用:可将刺余的NO氧化成NO3-,溶液由橙色变为绿色(Cr3+),反应的离子方程式是_____________________________________。
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体。设计实验证明D中有亚硝酸钙生成__________________________________________________。
(5)整个过程持续通入氮气的作用______________________________________。
-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去)。
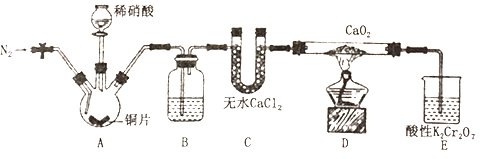
已知:2NO+CaO2=Ca(NO2)2;2NO2+CaO2 =Ca(NO3)2。
请回答下列问题:
a.向装置中通入N2;b.向三颈烧瓶中滴加稀硝酸;c.点燃酒精灯;d.熄灭酒精灯;e.停止通入氮气;f.关闭分液漏斗旋塞
(1)上述操作的正确排序为_________________________。
(2) B中盛放的试剂是_____,作用是除去________(填化学式)。
(3)装置E中,酸性K2Cr2O7溶液的作用:可剩余的NO氧化成NO3-,溶液由橙色变为绿色(Cr3+),反应的离子方程式是____________。
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体。设计实验证明D中有亚硝酸钙生成_____________。
(5)整个过程持续通人氮气的作用_______________。
-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):
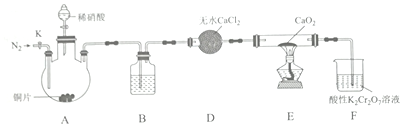
已知:2NO+CaO2 =Ca(NO2)2;2NO2+CaO2=Ca(NO3)2。
请回答下列问题:
(1)将分液漏斗中的稀硝酸滴入三颈烧瓶中的操作为______________。
(2)向三颈烧瓶中加入稀硝酸之前,应向装置中通入 一段时间的N2,原因为_________________。
(3)装置D中的仪器名称为_______________。装置B所加试剂为_______________。
(4)装罝F中,酸性K2Cr2O7溶液可将剩余的NO氧化为NO3-,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为_________________。
(5)已知:Ca(NO2)2溶液遇酸会产生NO气体。设计实验证明装置E中有亚硝酸钙生成:____________。
(6)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化空气,又能获得应用广泛的 Ca(NO2)2,反应原理为Ca(OH)2 + NO+NO2=Ca(NO2)2 + H2O。
①若n(NO):n(NO2)>l:l,则会导致_________________。
②若n(NO):n(NO2)<1:1,则会导致_________________。
-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去)。
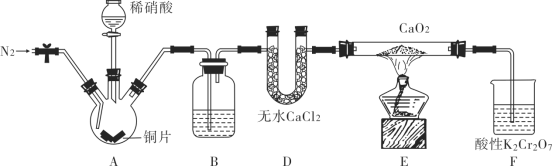
已知:2NO+CaO2=Ca(NO2)2 ;2NO2+CaO2=Ca(NO3)2 。
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因是_____________。
(2)仪器D的名称是______________;B中盛装的试剂是__________。
(3)装置F中,酸性K2Cr2O7溶液可将剩余的NO氧化成NO ,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为____________________________________________________________。
,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为____________________________________________________________。
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体。设计实验证明E中有亚硝酸钙生成_____________________________________________________________。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,反应原理为Ca(OH)2+NO+NO2=Ca(NO2)2+H2O。
①若n(NO)∶n(NO2)>1∶1,则会导致______________________________________________;
②若n(NO)∶n(NO2)<1∶1,则会导致______________________________________________。
-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去)。
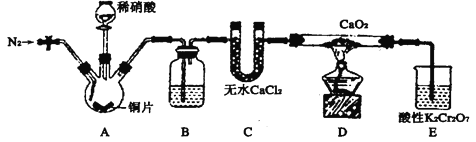
已知:2NO+CaO2=Ca(NO2)2;2NO2+CaO2=Ca(NO3)2。
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因为(用方程式表示)_________。
(2)装置B所加试剂是__________,作用是除去__________(填化学式)。
(3)装置E中,酸性K2Cr2O7溶液可将剩余的NO氧化成 ,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式是__________。
,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式是__________。
(4)已知:Ca(NO2)2溶液遇酸会产生NO气体。设计实验证明装置D中有亚硝酸钙生成:_________。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,反应原理为Ca(OH)2+NO+NO2=Ca(NO2)2+H2O。
①若n(NO) :n(NO2)>1 :1,则会导致_______________;
②若n(NO) :n(NO2)<1 :1,则会导致________________。
-
亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示。(夹持装置略去)

已知:2NO+CaO2 Ca(NO2)2;2NO2+CaO2
Ca(NO2)2;2NO2+CaO2 Ca(NO3)2。
Ca(NO3)2。
Ca(OH)2+NO+NO2=Ca(NO2)2+H2O
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因是______________________。
(2)装置D的名称是__________;装置B中盛装的试剂是___________。
(3)装置F中的酸性K2Cr2O7溶液可将剩余的NO氧化成NO3-,溶液由橙色(Cr2O72-)变为绿色(Cr3+),发生反应的离子方程式为_______________________________。
(4)已知Ca(NO2)2溶液显弱碱性,其对应的酸容易分解,产生NO气体,设计实验证明装置F中有亚硝酸钙生成:_________________________________。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2。
①若n(NO)∶n(NO2)>1∶1,则会导致____________________________________;
②若n(NO)∶n(NO2)<1∶1,则会导致____________________________________。