-
安全性是汽车发展需要解决的重要问题,安全气囊设计的基本思路是在汽车发生碰撞时,迅速在乘员和汽车内部结构之间打开一个充满气体的袋子,使乘员扑在气袋上,避免或减缓人与汽车的二次碰撞,从而达到保护乘员的目的。气囊中的气体是由化学反应产生的,选择或设计化学反应时需要考虑下列哪些角度
①反应速率 ②反应限度 ③气体的量 ④气体毒性 ⑤反应的能量变化
A. ①③④ B. ①②③④ C. ①②③④⑤ D. ①③④⑤
高一化学单选题简单题查看答案及解析
-
(7分)汽车发生强烈碰撞时,安全气囊内的NaH发生化学反应生成金属钠与氢气,所产生的气体快速充满气囊,可以达到保护车内人员的目的。
(1)请写出上述反应方程式: 它的基本反应类型是
(2)若安全气囊内含有96g NaH,其物质的量为 .
(3)若96g NaH完全分解,在标况下,气囊膨胀的体积约为
高一化学填空题中等难度题查看答案及解析
-
汽车发生强烈碰撞时,安全气囊内的NaN3发生化学反应生成氯化钠(Na3N)与氮气,所产生的气体快速充满气囊,可以达到保护车内人员的目的。
(1)请写出上述反应方程式: ;它的基本反应类型是 。
(2)若安全气囊内含有195gNaN3,其物质的量为 。
(3)若195gNaN3完全分解,在标准状况下,气囊膨胀的体积约为 。
(4)28gKOH固体必须溶解在 g水中,才能使每200个水分子中有1个K+。
(5)Mg能在O2、N2、CO2 中燃烧,写出镁在CO2 中燃烧的化学方程式 。
高一化学填空题困难题查看答案及解析
-
汽车安全气囊是在发生撞车时、产生二次碰撞前能够自动膨胀保护乘员的装置,碰撞时发生反应为:10NaN3+2KNO3═K2O+5Na2O+16N2↑。下列判断正确的是( )
A. N2既是氧化剂又是还原剂
B. 还原产物与氧化产物质量之比为1:15
C. 每生成16molN2转移30mole﹣
D. NaN3中N元素被还原
高一化学单选题中等难度题查看答案及解析
-
汽车安全气囊是在发生撞车时、产生二次碰撞前能够自动膨胀保护乘员的装置,碰撞时发生反应为:10NaN3+2KNO3═K2O+5Na2O+16N2↑。下列判断正确的是
A. N2既是氧化剂又是还原剂
B. NaN3中N元素被还原
C. 每生成16molN2转移30mole﹣
D. 还原产物与氧化产物质量之比为1:15
高一化学单选题简单题查看答案及解析
-
汽车安全气囊是在发生撞车时、产生二次碰撞前能够自动膨胀保护乘员的装置,碰撞时发生反应为:10NaN3+2KNO3═K2O+5Na2O+16N2↑。下列判断正确的是
A.N2既是氧化剂又是还原剂
B.NaN3中N元素被还原
C.每生成16molN2转移30mole﹣
D.还原产物与氧化产物质量之比为1:15
高一化学选择题中等难度题查看答案及解析
-
汽车安全气囊是在发生撞车时,能自动膨胀保护乘员的装置,碰撞时发生的反应为:10NaN3+ 2KNO3 =K2O+ 5Na2O+16N2,下列有关这个反应的说法中正确的是 ( )
A. 该反应中,每生成16mol N2转移30mole-
B. 该反应中氧化剂与还原剂的物质的量之比为1:5
C. 该反应中KNO3被氧化
D. 该反应中N2既是氧化剂又是还原剂
高一化学单选题中等难度题查看答案及解析
-
钠、碳及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
① KClO4中氯元素的化合价是_______,具有_______(填“还原性”或“氧化性”)。
② Fe2O3可处理产生的Na,反应为6Na + Fe2O3 =3Na2O + 2Fe,反应中Na做______(填“还原剂”或“氧化剂”)。
③ NaHCO3是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式是_______。
(2)Na2O2可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究Na2O2与CO2的反应。请回答下列问题:
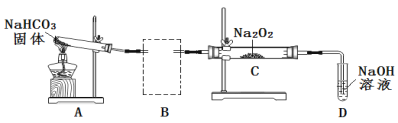
① 根据实验目的,将虚线框中的装置补充完整并标出所用的试剂_______。
② 装置C中观察到的现象是_______,反应的化学方程式是_______。
③ 装置D的作用是吸收未反应的CO2便于O2的检验。吸收CO2的离子方程式是_____。
高一化学综合题中等难度题查看答案及解析
-
钠、铁及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。KClO4中氯元素的化合价是_________,具有_________(填“还原性”或“氧化性”);Fe2O3可处理产生的Na,反应为6Na + Fe2O3 =3Na2O + 2Fe,反应中Na做_________(填“还原剂”或“氧化剂”)。
(2)甲、乙两同学欲制取纯净的Fe(OH)2 ,根据如图所示的装置进行试验。A管中是Fe粉和稀H2SO4 , B管中是NaOH溶液,请回答下列问题:
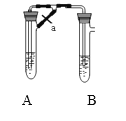
①同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是____________写出B中发生反应的所有离子方程式:___________________
②同学乙:打开a,使A管中反应一段时间再夹紧止水夹a,实验中在B管中观察到的现象是__________ ;
③同学乙打开a的目的______________,根据以上实验判断___________(填甲或乙)同学可成功。
高一化学实验题中等难度题查看答案及解析
-
(1)汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应:2NaN3=2Na+3N2↑,所产生的气体快速充满气囊,可以达到保护车内人员的目的。
①若130gNaN3完全分解,在标准状况下,气囊膨胀的体积约为___。
②该反应中的氧化剂是___,氧化产物是___。
(2)O3能与KI溶液反应,生成一种能使带火星木条复燃的气体,向反应后溶液中滴入酚酞变为红色,若滴入淀粉溶液则变为蓝色。为测定大气中O3的含量,将0℃、1.01×105Pa、33.6m3的空气通入KI溶液,使之完全反应,再向所得溶液中滴加0.01mol/L的Na2S2O3溶液60mL恰好与之完全反应。(I2与Na2S2O3的反应式:2NaS2O3+I2=Na2S4O6+2NaI)
①写出并配平O3与KI溶液反应的化学方程式___;
②计算大气中O3的体积分数(即O3的体积与空气体积的比值,用科学记数法表示)___。
高一化学综合题中等难度题查看答案及解析