-
海水是巨大的资源宝库,下列说法正确的是
A.碘元素又称“海洋元素”
B.镁是海水中含量最多的金属元素
C.从海水中提取食盐和碘的过程都是物理变化
D.氯碱工业的主要原料是食盐
高一化学选择题中等难度题查看答案及解析
-
海洋是巨大的资源宝库,从其中提取食盐和溴的过程如图所示。下列描述错误的是( )
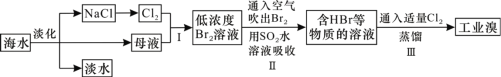
A.淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B.以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C.SO2水溶液吸收Br2的离子反应方程式为Br2+SO2+2H2O=4H++SO42-+2Br-
D.步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
高一化学单选题简单题查看答案及解析
-
海洋是一个巨大的物质资源和能量宝库,世界各国都在研究如何充分利用海洋资源。
Ⅰ. 从海水中可以提取食盐。
Ⅱ.从海水中提取镁。已知MgO、MgCl2的熔点分别为2800℃、604℃,从海水中提
取镁,最合理的方法是 。
A.海水
Mg(OH)2
Mg
B.海水
MgCl2溶液→MgCl2熔融
Mg
C.海
水
Mg(OH)2
MgO
Mg
D.海水
Mg(OH)2
MgCl2溶液→MgCl2熔融
Mg
Ⅲ.从海水中提溴。其工业方法有:空气吹出纯碱吸收法、空气吹出SO2吸收法、溶
剂萃取法等。
(1)空气吹出纯碱吸收法。将氯气通入富含溴离子的海水中,再用空气将溴吹出,
用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及的反应有:
① (写出离子方程式);
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3C
O2↑;
③BrO3﹣+5Br﹣+6H+═3Br2+3H2O
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,
然后再用氯气氧化即得单质溴。
写出溴与二氧化硫反应的化学
方程式: 。
高一化学填空题困难题查看答案及解析
-
浩瀚的海洋是一个巨大的宝库,含有80多种元素,可供提取利用的有50多种,我国十分重视海水资源的开发.下列物质不需要通过化学变化就能够从海水中获得的是( )
A.氢气、氯气
B.金属钠、镁
C.烧碱、液溴
D.食盐、淡水高一化学选择题中等难度题查看答案及解析
-
(12分)海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
已知:①海水中溴元素(以Br-表示)的浓度0.068g/L;
②Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。
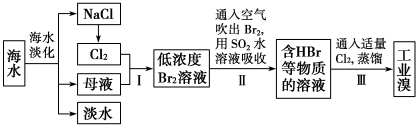
(1)请写出一种海水淡化的方法:_____________。
(2)海水中溴离子的物质的量浓度为_____________ 。
(3)步骤Ⅰ中已获得低溶度的含Br2溶液,步骤Ⅱ中又将Br2还原为Br-,步骤Ⅲ又得到Br2,其目的为________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 。
(5)工业溴提纯可用蒸馏法,蒸馏时加热方法最好采用 ,蒸馏装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_________________________________。
高一化学填空题中等难度题查看答案及解析
-
浩瀚的海洋是一个巨大的物质宝库,工业上常用浓缩海水提取溴。

下列说法不正确的是
A. 海水的淡化方法主要有蒸馏法、电渗析法、离子交换法等
B. 步骤②中体现了溴易挥发的性质
C. ①—④目的是为了富集溴元素
D. 步骤③反应的离子方程式为Br2+SO2+2H2O=2HBr+2H++SO42-
高一化学单选题困难题查看答案及解析
-
浩瀚的海洋是一个巨大的物质宝库,工业上常用浓缩海水提取溴。

下列说法不正确的是
A. 海水的淡化方法主要有蒸馏法、电渗析法、离子交换法等
B. 步骤②中体现了溴易挥发的性质
C. ①—④目的是为了富集溴元素
D. 步骤③反应的离子方程式为Br2+SO2+2H2O=2HBr+2H++SO42-
高一化学单选题困难题查看答案及解析
-
海水是巨大的资源宝库。从海水中提取食盐和溴的过程如下:
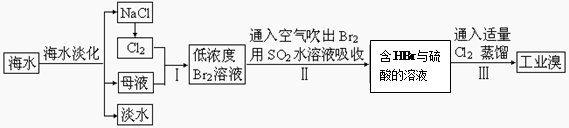
(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅱ的化学方程式,并用双线桥法标出电子转移的方向与数目。(4分)
________
(2)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下装置简图:
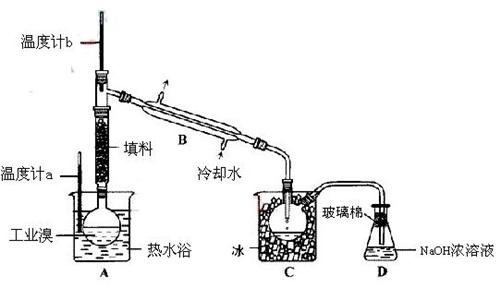
请你参与分析讨论:
①图中仪器B的名称: 。(1分)
②
实验装置气密性良好,要在C中获得纯净的液溴即达到提纯溴的目的,操作中如何控制关键条件: 。(2分)
③为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,则发生的反应方程式为
(2分)
充分反应后,再进行的分离操作是 。(1分)
高一化学填空题简单题查看答案及解析
-
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是
A. 海水中含有镁元素,只需经过物理变化就可以得到镁单质
B. 目前工业上直接由海水提取I2
C. 海水蒸发制海盐的过程中只发生了化学变化
D. 从海水中可以得到NaCl,电解熔融NaCl可制备Na
高一化学单选题简单题查看答案及解析
-
我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库。目前,世界各国都在研究如何充分利用海洋资源。全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65 mg·L-1。其工业提取法有:
(1)空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴。该方法涉及的反应有:
①_______________________________________ (写出离子方程式);
②3Br2+3CO32—=BrO3—+5Br-+3CO2↑;
③_______________________________________ (写出离子方程式);
(2)空气吹出SO2吸收法。该方法基本同(1),只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴。写出溴与二氧化硫反应的化学方程式____________。
(3)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上
可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。下图为“硫化氢-水双温交换法”所发生的两个反应中涉及的四种物质在反应体系中的物质的量随温度的变化曲线。写出100℃时所发生的反应的化学方程式______;工业上富集HDO的生产过程中,可以循环利用的一种物质是____。
高一化学填空题简单题查看答案及解析