-
某小组实验探究葡萄糖、二氧化硫分别与新制氢氧化铜的反应。
实验I 新制Cu(OH)2与葡萄糖反应
(1)将1.5mL1.0mol/LCuSO4溶液滴入5mLl.0mol/LNaOH溶液中制得Cu(OH)2悬浊液。相关反应的离子方程式为___________。
(2)在制得的Cu(OH)2悬浊液中加入稍过量葡萄糖溶液,加热煮沸,产生红色沉淀。
①该实验现象说明_______________;
②该原理可用于检测糖尿病患者血液中的______含量。
实验II 新制Cu(OH)2与二氧化硫反应
按上述方法重新制取氢氧化铜悬浊液,通入足量二氧化硫,先产生红色沉淀,然后红色沉淀逐渐变为紫红色固体,最终溶液呈无色。
(1)探究红色沉淀转变为紫红色的原因。
将实验I产生的红色沉淀过滤、洗涤,洗涤方法是_____。
将所得固体分成两等份于试管中并加入少量蒸馏水进行对比实验。
| 实验装置图 | 
| 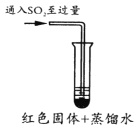
|
| 操作及现象 | 红色固体很快转变为紫红色固体,溶液呈蓝色。 | 开始红色固体缓慢变为紫红色固体,溶液呈蓝色。试管内紫红色固体逐渐增多,最后溶液变无色。 |
| 解释及结论 | ①该反应的离子方程式 _________________。 | ②开始时红色固体颜色变化缓慢的原因是_________。 ③所得无色溶液中主要阴离子为___________________。 |
(2)通过上述探究,写出新制氢氧化铜与过量SO2反应的总化学方程式______________。
反思:将表中SO2换为NO2是否能观察到相同现象? 回答并解释:__________。
-
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 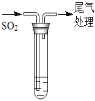
| 实验Ⅰ | 1.5 mL1 mol/L CuSO4溶液和3.5 mL 1mol/L NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL1 mol/L CuCl2溶液和3.5 mL 1 mol/L NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为__________________________________。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:__________________,检验Cu(OH)2洗涤干净的方法是____________________________________________。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、____________________________。
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
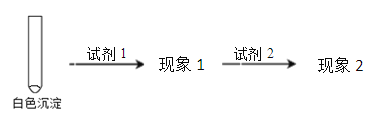
填写下表空格:
| 试剂1 | _________________ | 试剂2 | 蒸馏水 |
| 现象1 | _________________ | 现象2 | _________________ |
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:_________________。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,_________________________________,则说明砖红色沉淀是Cu2O。
-
某实验小组探究过量甲醛与新制氢氧化铜的反应,探究过程如下:
(一)提出猜想
(1)甲同学通过查阅资料,提出猜想1和猜想2。
猜想1:HCHO + Cu(OH)2 Cu + CO↑+ 2H2O
Cu + CO↑+ 2H2O
猜想2:HCHO + 4Cu(OH)2 + 2NaOH 2Cu2O + Na2CO3 + 6H2O
2Cu2O + Na2CO3 + 6H2O
猜想1和猜想2均体现了甲醛的________性。
(2)乙同学类比乙醛与新制氢氧化铜的反应,提出猜想3。
用化学方程式表示猜想3:________。
(二)进行实验,收集证据
已知:可用银氨溶液检测CO,反应为CO + 2Ag(NH3)2OH  2Ag↓+ (NH4)2CO3 + 2NH3。实验在如下装置中进行。反应结束后,A中生成紫红色固体沉淀物,C中银氨溶液无明显变化,气囊略鼓起。
2Ag↓+ (NH4)2CO3 + 2NH3。实验在如下装置中进行。反应结束后,A中生成紫红色固体沉淀物,C中银氨溶液无明显变化,气囊略鼓起。
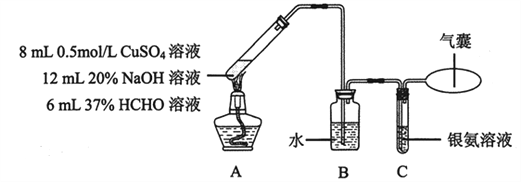
(3)配制银氨溶液所需的试剂是________。
(4)装置B中水的作用是________。
(5)甲同学取A中反应后溶液加入到足量稀盐酸中,无明显现象。乙同学另取该溶液加入到BaCl2溶液中,产生大量白色沉淀。
实验方案明显不合理的是________(填“甲”或“乙”),理由是________。
(6)已知Cu2O Cu + CuSO4。
Cu + CuSO4。
丙同学通过实验证明生成的紫红色固体沉淀物是Cu,其实验方案为________。
(三)得出结论
(7)写出过量甲醛与新制氢氧化铜可能发生反应的化学方程式________。
-
(15分)
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 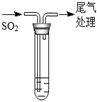
| 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O === Cu(NH3)2+ + Cl- + 2H2O 、 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
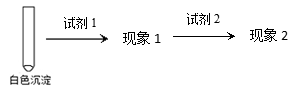
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, ,则说明砖红色沉淀是Cu2O。
-
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
| 装置 | 序号 | 试管中的药品 | 现象 |
| 持续通入 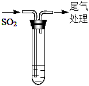
| 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3)2+ + Cl- + 2H2O 、 ____________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
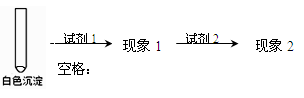
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, _______________ ,则说明砖红色沉淀是Cu2O。
-
(13分)某校化学兴趣小组对课本实验结论“葡萄糖与新制氢氧化铜共热生成红色的Cu2O沉淀”提出质疑,认为红色沉淀不一定就是氧化亚铜。为了确定红色沉淀的成分,开展了相关探究。
(4)方案Ⅲ中,若要测定红色粉末的成分,需要测定下列哪些物理量________(填序号)。
①反应前红色粉末与硬质玻璃管的总质量 ②实验前干燥管的质量 ③实验后干
燥管的质量 ④硬质玻璃管的质量 ⑤锌粒质量 ⑥稀硫酸的物质的量浓度
-
已知乙醛(CH3CHO)和新制氢氧化铜的反应如下:
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
CH3COONa+Cu2O↓+3H2O
某实验小组做上述反应时,发现NaOH的用量对反应产物有影响,于是他们采用控制变量的方法,均使用0.5 mL 40%的乙醛溶液进行下列实验。
| 编号 | 2%CuSO4溶液的体积 | 10%NaOH溶液的体积 |  振荡后 振荡后
的现象 | pH | 加乙醛水浴加热后的沉淀颜色 |
| 1 | 2 mL | 3滴 | 浅蓝绿色沉淀 | 5~6 | 浅蓝绿色沉淀 |
| 2 | a | 15滴 | 浅蓝色沉淀 | 7~8 | 黑色沉淀 |
| 3 | 1 mL | 1 mL | 蓝色悬浊沉淀较少 | 9~10 | 红褐色沉淀 |
| 4 | b | 2 mL | 蓝色悬浊沉淀较多 | 11~12 | 红色沉淀 |
| 5 | 1 mL | 3 mL |  蓝紫色溶液 蓝紫色溶液
| 12~13 |  ———— ————
|
(1)上表中a、b应为 (填字母序号)。
A.15滴,1 mL B.2 mL,1 mL C.15滴,2 mL D.2 mL,2 mL
(2)查阅资料可知,实验1中的浅蓝绿色沉淀主要成份为Cu2(OH)2SO4,受热不易分解。写出生成Cu2(OH)2SO4反应的化学方程式 。基于实验1、2的现象可以得出结论:NaOH用量较少时, 。
(3)小组同学推测实验3中的红褐色沉淀可能是CuO和Cu2O的混合物,其理论依据是 。
(4)为了进一步证明实验4中红色沉淀的成分,该小组同学查阅资料得知:Cu2O在碱性条件下稳定,在酸性溶液中可转化为Cu2+、Cu。并进行了以下实验。
ⅰ.将实验4反应后的试管静置,用胶头滴管吸出上层清液。
ⅱ.向下层浊液中加入过量稀硫酸,充分振荡、加热 ,应观察到的现象是 。
,应观察到的现象是 。
(5)小组同学继续查阅资料得知:Cu(OH)2可与OH-继续反应生成蓝紫色溶液([Cu(OH)4] 2-),由此提出问题:[Cu(OH)4] 2-能否与乙醛发生反应,生成红色沉淀?设计实验解决这一问题,合理的实验步骤是 。基于上述实验,该小组同学获得结论:乙醛参与反应生成红色沉淀时,需控制体系的pH>10。
-
已知乙醛(CH3CHO)和新制氢氧化铜的反应如下:
CH3CHO + 2Cu(OH)2 + NaOH  CH3COONa + Cu2O↓+ 3H2O
CH3COONa + Cu2O↓+ 3H2O
某实验小组做上述反应时,发现NaOH的用量对反应产物有影响,于是他们采用控制变量的方法,均使用0.5 mL 40%的乙醛溶液进行下列实验。
| 编号 | 2%CuSO4溶液的体积 | 10%NaOH溶液的体积 | 振荡后 的现象 | pH | 加乙醛水浴加热后的沉淀颜色 |
| 1 | 2 mL | 3滴 | 浅蓝绿色沉淀 | 5~6 | 浅蓝绿色沉淀 |
| 2 | a | 15滴 | 浅蓝色沉淀 | 7~8 | 黑色沉淀 |
| 3 | 1 mL | 1 mL | 蓝色悬浊沉淀较少 | 9~10 | 红褐色沉淀 |
| 4 | b | 2 mL | 蓝色悬浊沉淀较多 | 11~12 | 红色沉淀 |
| 5 | 1 mL | 3 mL[ | 蓝紫色溶液 | 12~13 | ———— |
(1)上表中a、b应为 (填字母序号)。
A.15滴,1 mL B.2 mL,1 mL C.15滴,2 mL D.2 mL,2 m L
L
(2)查阅资料可知,实验1中的浅蓝绿色沉淀主要成份为Cu2(OH)2SO4,受热不易分解。写出生成Cu2(OH)2SO4反应的化学方程式 。基于实验1、2的现象可以得出结论:NaOH用量较少时, 。
(3)小组同学推测实验3中的红褐色沉淀可能是CuO和Cu2O的混合物,其依据是 。
(4)为了进一步证明实验4中红色沉淀的成分,该小组同学查阅资料得知 :Cu2O在碱性条件下稳定
:Cu2O在碱性条件下稳定 ,在酸性溶液中可转化为Cu2+、Cu。并进行了以下实验。
,在酸性溶液中可转化为Cu2+、Cu。并进行了以下实验。
ⅰ.将实验4反应后的试管静置,用胶头滴管吸出上层清液。
ⅱ.向下层浊液中加入过量稀硫酸,充分振荡、加热,应观察到的现象是 。
(5)小组同学继续查阅资料得知:Cu(OH)2可与OH-继续反应生成蓝紫色溶液([Cu(OH)4] 2-),由此提出问题:[Cu(OH)4] 2-能否与乙醛发生反应,生成红色沉淀?设计实验解决这一问题,合理的实 验步骤是 。
验步骤是 。
基于上述实验,该小组同学获得结论:乙醛参与反应生成红色沉淀时,需控制体系的pH>10。
-
某课题组同学受葡萄糖与新制氢氧化铜悬浊液反应实验的启示,拟设计实验利用氧化铜探究乙醛的还原性。
【提出猜想】 猜想 1: CH3CHO+2CuO  CH3COOH+Cu2O;
CH3COOH+Cu2O;
猜想 2:_______________________ (写出化学方程式)。
【定性实验】(1)甲同学设计下图装置进行实验(部分夹持装置已略去):
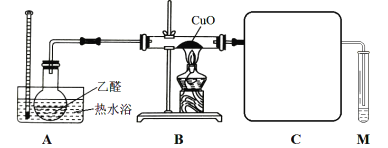
已知: 乙醛和乙酸的沸点分别为 20.8℃、 117.9℃。
按上述装置进行实验,当氧化铜完全反应后停止实验。
①为达到良好的冷凝效果,方框中 C 装置应选用_________(填仪器名称);实验中先通入乙醛蒸气,后点燃装置 B 处酒精灯,这样操作的目的是_________。
②已知: Cu2O 呈红色,在酸性条件下发生反应 Cu2O+2H+=Cu+Cu2++H2O。 请你设计实验证明猜想 1 成立。
实验操作:____________________________________ 。
实验现象:____________________________________ 。
【定量实验】(2)乙同学设计了如下图所示实验方案定量探究红色固体的成分。
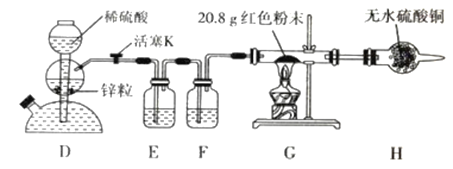
已知:醋酸亚铬[Cr(CH3COO)2]溶液可以吸收少量的 O2。
①下列有关说法正确的是(填标号)_______ 。
a. 装置 D 可以控制反应的发生与停止
b. 装置 F 中盛装醋酸亚铬溶液
c. 向装置 D 中加入少量硫酸铜固体可加快反应
d. 实验中观察到装置 G 中有明显现象
②装置 G 中红色粉末完全反应后,称得固体粉末质量为 19.2 g;装置 H 净增质量为2.0 g。请选择合理数据计算,确定红色粉末的成分及物质的量: _______。
-
某实验探究小组根据乙醛还原新制Cu(OH)2的实验操作和实验现象。对反应方程式“CH3CHO+2Cu(OH)2 CH3COOH+Cu2O↓+2H2O”提出了质疑,并进行如下探究:
CH3COOH+Cu2O↓+2H2O”提出了质疑,并进行如下探究:
(一)查阅资料
(1)质量分数为10%的NaOH溶液密度为1.1g·cm-3,该溶液的c(NaOH)=________mol/L;质量分数为2%的CuSO4溶液密度为1.0g·cm—3,其c(CuSO4)=0.125mol/L。
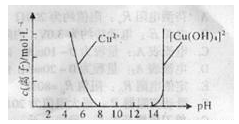
(2)Cu(OH)2可溶于浓的强碱溶液生成深蓝色
的[Cu(OH)4]2-溶液,CuSO4溶液与NaOH
溶液反应过程中Cu2+与[Cu(OH)4]2—浓度
变化如右图所示:
(3)Cu2O、CuO均可溶于CH3COOH;在溶液中
可发生2Cu+==Cu+Cu2+反应。
(二)实验操作及实验现象
(1)在2mL 10%的NaOH溶液中滴加4~6滴(约0.2mL)2%CuSO4溶液,经测定混合溶液中c(OH-)约为2.5mol/L。
(2)若对上述混合物进行过滤,可得到浅蓝色的________(填化学式)固体,滤液呈深蓝色,则显深蓝色的离子是________(填离子符号)。
(3)在第(1)步所得的混合物中加入0.5mL 乙醛,加热至沸腾,产生砖红色沉淀。
(三)对“CH3CHO+2Cu(OH)2 CH3COOH+Cu2O↓+2H2O”质疑的理由:
CH3COOH+Cu2O↓+2H2O”质疑的理由:
(1)________;(2)________。
(四)结论:根据上述探究,乙醛与新制Cu(OH)2反应的离子方程式为
________。











