-
有A、B、C、D四种同周期元素,元素E与 C不同周期。A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D的最高价氧化物的水化物是酸,且C比D的酸性强, E是这五种元素中原子半径最大的,则它们的原子序数由小到大的顺序是
A.E、C、D、B、A B.B、A、D、C、E
C.E、B、A、D、C D.A、B、C、D、E
高一化学选择题中等难度题查看答案及解析
-
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A依次减小,B和E同主族.
下列推断不正确的是( )
A.A、B、E一定在不同周期
B.C的最高价氧化物的水化物可能显碱性
C.A、D可能在同一主族
D.C和D的单质可能化合形成离子化合物高一化学选择题中等难度题查看答案及解析
-
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A依次减小,B和E同主族.下列推断不正确的是
A.A、B、E一定在不同周期 B.C的最高价氧化物的水化物可能显碱性
C.A、D可能在同一主族 D.C和D的单质可能化合形成离子化合物
高一化学选择题困难题查看答案及解析
-
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族,下列推断不正确的是
A.A、B、E一定在不同周期
B.C的最高价氧化物的水化物可能显碱性
C.C和D的单质可能化合形成离子化合物
D.A、D可能在同一主族
高一化学选择题简单题查看答案及解析
-
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族,下列推断不正确的是
A.A、B、E一定在不同周期
B.C的最高价氧化物的水化物可能显碱性
C.C和D的单质可能化合形成离子化合物
D.A、D可能在同一主族
高一化学选择题简单题查看答案及解析
-
(16分)图是元素周期表的框架,依据元素周期表回答下列问题:
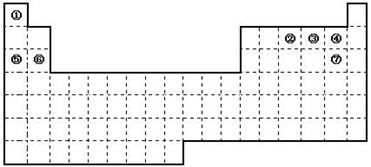
(1)周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是________(用化学式表示),周期表中的元素④和元素⑦的氢化物的沸点高低顺序是________(用化学式表示)。
(2)①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是________(填写化学式)。
(3)①和②的单质在一定条件下转化为化合物A,请写出该反应的化学方程式________,及A的结构式________。
(4)②和硅形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是________, 与该化合物晶体类型相同的是______(请用相应的编号填写)。
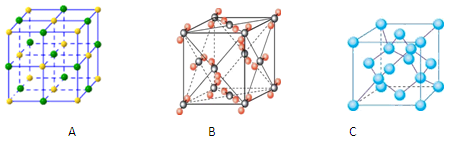
(5)请写出工业上用电解饱和食盐水制备⑦单质的化学方程式。
高一化学填空题简单题查看答案及解析
-
(16分)图是元素周期表的框架,依据元素周期表回答下列问题:

(1)周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是________(用化学式表示),周期表中的元素④和元素⑦的氢化物的沸点高低顺序是________(用化学式表示)。
(2)①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是________(填写化学式)。
(3)①和②的单质在一定条件下转化为化合物A,请写出该反应的化学方程式________,及A的结构式________。
(4)②和硅形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是________, 与该化合物晶体类型相同的是______(请用相应的编号填写)。
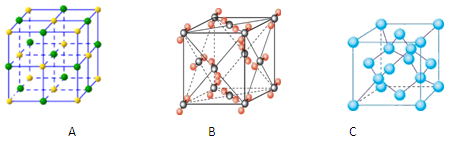
(5)请写出工业上用电解饱和食盐水制备⑦单质的化学方程式。
高一化学填空题简单题查看答案及解析
-
图是元素周期表的框架,依据元素周期表回答下列问题:
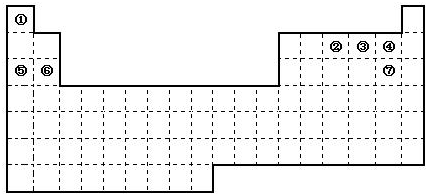
(1)周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是______(用化学式表示),周期表中的元素④和元素⑦的氢化物的沸点高低顺序是______(用化学式表示).
(2)请写出②的氢化物的电子式______,③的氢化物的结构式______.
(3)①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是______(填写分子式).
(4)请写出工业上制备⑦单质的化学方程式______ 2NaOH+H2↑+Cl2↑高一化学解答题中等难度题查看答案及解析
-
(20分)下图是元素周期表的框架
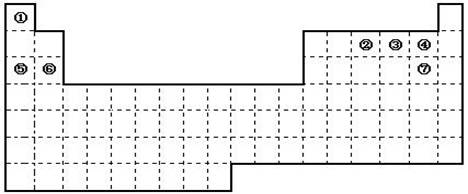
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)依据元素周期表回答下列问题:
A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是________(用化学式表示)。
B.周期表中的元素④和元素⑦的氢化物的熔、沸点高低顺序是________(用化学式表示)。
C.①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是________(填写结构式)。
D.在上面元素周期表中全部是金属元素的主族是________;全部是非金属元素的主族是________(填写字母a、b、c、d)。
a.ⅠA族 b. ⅡA族 c. ⅥA 族 d.ⅦA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式________ ________;
(4)请写出仅用①②④三种元素形成离子化合物的电子式_________。若用球棍模型表示①和③形成的化合物的分子结构,应该是________。
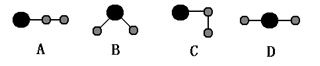
⑸ 在120℃下1g①的单质在足量③的单质中完全燃烧,放出的热量为a kJ;请写出此条件下①的单质燃烧的热化学方程式________ ________ ________;
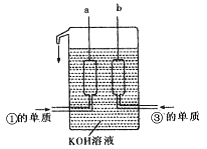
①、③两种元素的单质已被应用于字宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电。
请回答:b是电池的________极;a电极上的电极反应式是 。
高一化学填空题简单题查看答案及解析
-
应用元素周期律分析,下列推断正确的是
A.第3周期金属元素最高价氧化物对应的水化物,其碱性随原子序数的增大而减弱
B.砹(At)是第VIIA族元素,其氢化物的稳定性大于HCl
C.第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
D.铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
高一化学选择题中等难度题查看答案及解析