-
己知室温时Ksp[Mg(OH)2] = 1.8×l0-11,则此温度下Mg(OH)2在pH = 12的NaOH溶液中的最大溶解浓度为
A. 1.8×l0-7mol/L B. 1.0×l0-5mol/L C. 1.0×l0-7mol/L D. 1.8×l0-9mol/L
高三化学选择题中等难度题查看答案及解析
-
己知25℃时,Mg(OH)2的Ksp=1.8×l0-11,若要使0.18mol/L的MgCl2溶液生成Mg(OH)2沉淀,则至少需要将溶液的pH调至
A.5 B.5.5 C. 9 D.11
高三化学选择题中等难度题查看答案及解析
-
已知25℃时,Mg(OH)2的Ksp=1.8×l0-11,若要使0.18mol/L的MgCl2溶液生成Mg(OH)2沉淀,则至少需要将溶液的pH调至
A.5 B.5.5 C.9 D.11
高三化学单选题简单题查看答案及解析
-
下列说法不正确的是
A. 化学键的断裂和形成是化学反应中能量变化的主要原因
B. 已知常温下Ksp[Mg(OH)2]=1.8×10-11,则Mg(OH)2在pH=12的NaOH溶液中的溶解度约为1.044×10-6g
C. 水能,风能、生物质能是可再生能源,煤、石油、天然气是不可再生能源
D. 用酚醛树脂制成的塑料可反复加热熔融加工
高三化学单选题中等难度题查看答案及解析
-
(1)已知Ksp(AgCl)=1.8×10-10,则将AgCl放在蒸馏水中形成饱和溶液,溶液中的c(Ag+)是________?
(2)已知Ksp[Mg(OH)2]=1.8×10-11,则将Mg(OH)2放入蒸馏水中形成饱和溶液,溶液的pH为________?
(3)在0.01 mol·L-1的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的pH是________?当Mg2+完全沉淀时,溶液的pH为________?
高三化学计算题中等难度题查看答案及解析
-
(1)已知Ksp(AgCl)=1.8×10-10,则将AgCl放在蒸馏水中形成饱和溶液,溶液中的c(Ag+)是________?
(2)已知Ksp[Mg(OH)2]=1.8×10-11,则将Mg(OH)2放入蒸馏水中形成饱和溶液,溶液的pH为________?
(3)在0.01 mol·L-1的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的pH是________?当Mg2+完全沉淀时,溶液的pH为________?
高三化学计算题中等难度题查看答案及解析
-
①25℃,难溶电解质的溶度积常数:Ksp[CaF2]=1.5×10-10,Ksp[Mg(OH)2]=1.8×10-11,Ksp [Cu(OH)2]=2.2×10-20
②弱电解质在水溶液中存在电离常数:例如一元弱酸HA
H++A-,其电离常数表达式 Ka= c(H+)·c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5
③25℃时,2.0×10-3mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到
c(HF)、c(F-)与溶液pH的变化关系,如下图所示:

请根据以上信息回答下列问题:
(1)25℃时,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为________。
(2)25℃时,HF电离常数的数值Ka
________,列式并说明得出该常数的理由。
(3)25℃时,向浓度均为0.1 mol·L-1的相同体积的HF和醋酸两种溶液中分别加入相同的足量锌粒,初始时产生氢气的速率关系为________ (填“>”“=”或“<”,下同)。反应结束后,产生氢气的物质的量的关系为________,两溶液中c (F-)________ c (CH3COO-)。
(4)25℃时,4.0×10-3mol·L-1HF溶液与4.0×10-4 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。
高三化学填空题中等难度题查看答案及解析
-
Ⅰ.室温下,已知Ksp[Mg(OH)2]=1.0×10-11,现用MgSO4溶液制备[Mg(OH)2。若MgSO4溶液中c(Mg2+)=1.0×10-3mol/L,那么,向其中加入等体积的KOH溶液的浓度为__________________mol/L,可使Mg2+恰好完全沉淀(溶液体积变化可忽略不计,但溶液中残留的Mg2+不能忽略)。
Ⅱ.钼酸钠晶体(Na2MoO4·2H2O)是一种无公害型冷却水系统的金属缓蚀剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:

(1) 钼和锆同属过渡金属, 锆还是核反应堆燃料棒的包裹材料, 锆合金在高温下与水蒸气反应产生氢气, 二氧化锆可以制造耐高温纳米陶瓷。下列关于锆合金、二氧化锆的说法中正确的是_____(填序号)
a. 锆合金比纯锆的熔点高,硬度小
b.二氧化锆陶瓷属于新型无机非金属材料
c.将一束光线通过纳米级二氧化锆会产生一条光亮的通路
(2) 途径I碱浸时发生反应的化学反应方程式为_________________
途径Ⅱ氧化时发生反应的离子方程式为______________________
(3)分析纯的钼酸钠常用钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与途径I所产生的尾气一起通入水中,得到正盐的化学式是______________。
(4) 钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀
速率实验结果如下图:

①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为____。
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是___________________。
高三化学填空题困难题查看答案及解析
-
以水氯镁石(主要成分为
)为原料生产碱式碳酸镁的主要流程如下:
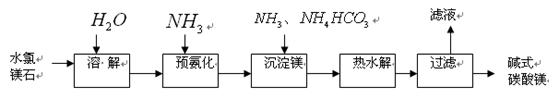
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的KSP=1.8×10-11,若溶液中c(OH-)=3.0×10-6mol·mol·L-1,则溶液中_____。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为_____。
(3)高温煅烧碱式碳酸镁得到
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有
,则产品中镁的质量分数_____(填 “升高”、“降低”或“不变”)。
高三化学填空题极难题查看答案及解析
-
以水氯镁石为原料生产碱式碳酸镁的主要流程如下:

(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6mol•L-1,则溶液中c(Mg2+)=______.
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为______.
(3)高温煅烧碱式碳酸镁得到MgO.取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L,通过计算确定碱式碳酸镁的化学式.
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数 (填“升高”、“降低”或“不变”).高三化学解答题中等难度题查看答案及解析