-
碳、氮、锌、汞的相关化合物在化工、医药、材料方面有着广泛的应用
(1)画出基态Zn原子的价电子排布图_________;
(2)在基态N原子中,核外电子占据的最高能层符号为________,占据该能层电子的电子云轮廓图形状为____________;
(3)Zn,Cd,Hg均为第ⅡB族元素,根据相对论收缩效应致,全满的6s壳层非常稳定,已知Hg原子的核外电子排布式为[Xe]4f145d106s2,请解释Hg在常温下为液态的原因_________________________;
(4)碳酸盐的热分解是由于晶体中阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果。已知
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
请解释碱土金属元素碳酸盐热分解温度的变化规律:________________________________;
(5)纳米氧化锌是稳定的化合物,可以提供广谱的紫外保护(UVA和UVB),同时还有抗菌和抗炎的作用,一种氧化锌晶体具有ZnS型结构,边长为 a=0.446nm,求:
①Zn和O之间最短的距离为________nm;
②与Zn紧邻的O的个数为_______.
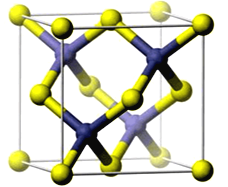
晶胞内部原子为Zn,顶点和面心原子为O
-
磷和砷的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态As原子的核外电子排布式为[Ar]_________;As 原子的逐级电离能(kJ/mol)数据如下:
| 第一电离能 | 第二电离能 | 第三电离能 | 第四电离能 | 第五电离能 | 第六电离能 |
| 947.0 | 1798 | 2735 | 4837 | 6043 | 12310 |
第五电离能与第六电离能相差显著的原因:_____________________________________。
(2)红磷是巨型共价分子,无定型结构。能证明红磷是非晶体的最可靠方法是__________。
A.质谱 B.原子发射光谱 C.核磁共振谱 D.X 射线衍射
(3)黑磷是新型二维半导体材料,具有类似石墨一样的片层结构(如图),层与层之间以_____结合。从结构上看,单层磷烯导电性优于石墨烯的原因是____________________________。
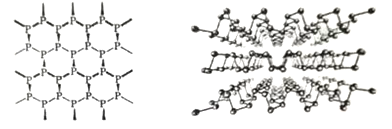
(4)白磷(P4) 分子是正四面体结构,3.1g 白磷中σ键的数目为________;白磷(P4)易溶于二硫化碳,难溶于水,其原因是_____________________________________________。
(5)GaAs 的熔点为1238℃,其晶胞结构如图所示。该晶体的类型为_________,Ga 原子的杂化方式为______________,每个 As原子周围最近的As原子数目为________。已知GaAs的密度为dg/cm3,摩尔质量为M g/mol,则晶胞中最近的As 和Ga原子核间距为_____(阿伏加德罗常数值用NA表示,列出算式即可)nm。

-
碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为[Ar]______________________;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________(填角度)。
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与____________个B相连,As的杂化形式为_______________;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有____________(填字母)。
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于________________________________(填晶体类型)。
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___________(填字母)。
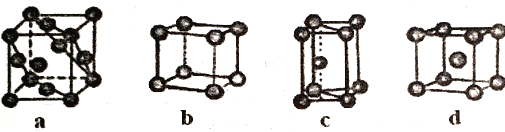
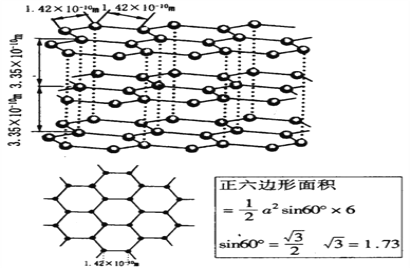
(6)石墨晶体的结构如下图,石墨的密度为________________________________(只列式不化简不计算)
-
氮、磷、砷、硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。回答下列问题:
(1)基态As原子的电子排布式为__________。N、P、As的第一电离能的大小顺序为 _______。
(2)氮化硼(BN)有多种晶体,其中立方氮化硼与金刚石的构型类似,则其晶胞中B-N-B之间的夹角是_________(填角度)。
(3)砷化硼(BAs)是Ⅲ-V族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与_____个B相连,As的杂化形式为______;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有_______(填字母)。
A.离子键 B. 金属键 C.极性键 D.氢键 E.配位键F.  键G.
键G.  键
键
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,这种陶瓷材料可作为金属表面的保护薄膜,它是通过在高温(T>750℃)氢气氛围下BBr3和PBr3反应制得的,BBr3的空间构型为______,BP晶胞的结构如图所示,当晶胞晶格参数为478pm(即图中立方体的每条边长为478pm)时,BP中B和P之间的最近距离为_____。

-
钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
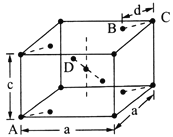
①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
-
钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。

①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
-
钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
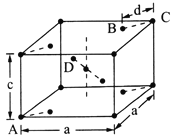
①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
-
钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。
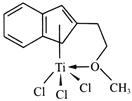
①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
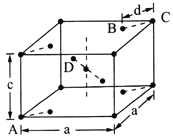
①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
-
第四周期中某些元素的相关化合物在化工、医药、材料等领域有着广泛应用
(1)现代化学中,常利用_________上的特征谱线来鉴定元素。Ga的外围电子排布式为:_____________________,基态Ga原子核外有______种运动状态不同的电子。
(2)锗、砷、硒、溴的第一电离能由大到小的顺序为____________(用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维掺杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为_________,中心原子的杂化类型为________;砷酸的酸性弱于硒酸,从分子结构的角度解释原因_______________________。
(3)铁能形成[Fe(Bipy)2C12]ClO4等多种配合物(Bipy结构如下图A)。
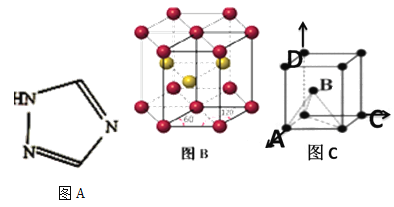
①该配合物中中心原子的化合价为________;与中心原子形成配位键的原子是________。
②与ClO4-互为等电子体的一种非极性分子是_______(举1例)。
③1 mol Bipy中所含σ键______mol。
(4)钛(Ti)被誉为“21世纪金属”,Ti晶体的堆积方式是六方最密堆积如图B所示,晶胞可用图C表示。设金属Ti的原子半径为a cm,空间利用率为__________。设晶胞中A点原子的坐标为(1,0,0),C点原子的坐标为(0,1,0),D点原子的坐标为(0,0,1),则B点原子的坐标为________________。
-
N、F、Cu及其化合物在化工、医药、材料等方面应用十分广泛。回答下列有关问题:
(1)N原子中最高能级的电子的电子云轮廓图为___________;基态Cu+的核外电子排布式为____________。
(2)化合物(CH3)3N可用于制备医药、农药。分子中N原子杂化方式为________,该物质能溶于水的原因是_____________________。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,其阳离子的空间构型为_____________,写出一种与[H2F]+互为等电子体的分子______________(写化学式)。
(4)氮、铜形成的一种化合物的晶胞结构如图所示。与每个Cu原子紧邻的Cu原子有____个,令阿伏加德罗常数的值为NA,该晶体的密度为______g/cm3。(列出计算式)
















